酚醛树脂基球形活性炭的制备及其吸附性能
2020-07-23尹纪伟杜洁王旭明张芳华李雪李玮张红蕾
尹纪伟,杜洁,王旭明,张芳华,李雪,李玮,张红蕾
(河北大学 化学与环境科学学院,药物化学与分子诊断教育部重点实验室,河北 保定 071002)
活性炭是一种常见的多孔碳质材料,具有发达且丰富的孔隙结构、比表面积大,理化性质稳定、吸附性能强的特性,是一种优良的吸附剂[1].根据其形状的差异,可将其分为粉末状、纤维状、颗粒状和球形活性炭等[2].球形活性炭除了具有一般活性炭优良的吸附特性外,还具备一些独特的性质,如表面均匀光滑,粒径大小均一,孔径分布易控,纯度高灰分低,填充密度高,具有良好的滚动性和耐磨性,使用过程中掉屑少,吸脱附速率高,生物相容性优良[3].鉴于球形活性炭具备独特的优势,近年来球形活性炭已广泛应用于能源、环保、电子、化学防护、军事防护、制药和催化剂载体等领域,特别是在血液净化材料领域日益受到关注[4-7],具有广阔的发展前景.
目前,已有很多学者在研究酚醛树脂制备活性炭的工艺条件以及吸附性能.张玺等[8]将酚醛树脂作为原料、采用水蒸气活化法合成的酚醛树脂基活性炭对二氧化碳表现出良好的吸附性能.黄婧等[9]制备的酚醛树脂基球形活性炭表面富含有含氧基团,且具有发达的微孔结构,可以很好地选择性吸附氮化物.包燕君[10]等制备的聚苯乙烯基球形活性炭比表面积可达到1 454 m2/g,对DL-β氨基异丁酸的吸附率可达51.74%.20世纪80年代日本吴羽化学公司[11]就在球形活性炭口服吸附剂方面进行了研制.该吸附剂能对肌酐等多种有害毒物进行有效吸附,极大程度降低了其在人体血浆中的浓度,被当作尿毒症辅助疗法的一种保守疗法.酚醛树脂基球形活性炭是目前较为理想的生物医学吸附材料.作为优良的生物医学吸附材料,不仅要考虑其在生理环境下,对有毒分子(如DL-β氨基异丁酸)的吸附脱除效率,还要考虑其对有益分子(如α-淀粉酶)的吸附能力.因此,需要通过对制备过程的研究与优化,获得对有毒分子尽可能大的脱除效果,而对有益分子尽可能起到屏蔽作用.
本文优化了酚醛树脂基球形活性炭的制备过程,并对制得的活性炭吸附性能进行了研究.首先,采用悬浮聚合法以苯酚、甲醛和三乙烯四胺为原料制备出球形酚醛树脂.其次,在氮气保护下对酚醛树脂进行炭化处理,并采用水蒸气活化法,分别在不同活化温度和活化时间下制备酚醛树脂基球形活性炭.并对球形活性炭进行氮气吸附-脱附等温曲线、孔径分布和比表面积进行了测定.最后考察了酚醛树脂基球形活性炭对尿毒症毒素DL-β氨基异丁酸的吸附效果,以及对人体有益分子α-淀粉酶的吸附情况.
1 实验部分
1.1 主要仪器
全自动快速比表面积与孔隙度分析仪(BET)(康塔仪器公司);傅里叶变换红外光谱仪(赛默飞世尔科技有限公司);冷场扫描电子显微镜(日本电子);恒温震荡培养器(上海智城分析制造有限公司);紫外分光光度仪(安捷伦);荧光分光光度计(安捷伦);开启式真空管式电炉(天津中环电炉股份有限公司).
1.2 酚醛树脂的合成
向500 mL烧杯中加入苯酚110.0 g,质量分数37%的多聚甲醛溶液或37%的甲醛溶液,搅拌溶解.溶解后加入质量分数2%的羟乙基纤维素水溶液55.0 g.慢慢滴加质量分数16.53%的三乙烯四胺的水溶液,反应液慢慢变乳白色浑浊.将反应液倒入高压釜,补加150 mL水,升温至130 ℃,调整转速到500~800 r/min,反应1 h.反应完成后,待物料温度降至室温后,加入100 mL水,将产品抽出,静置10 min,倾去上层清液.用500 mL的水洗涤固体,静置后倾去上层清液,重复4次,然后抽滤,200 mL水加少量甲醇淋洗滤饼2次,抽干后115 ℃鼓风干燥5 h.
1.3 球形活性炭的制备
称取球形酚醛树脂30.0 g,置于石英舟中,将其置于管式炉炉管中部,通入流量为600 mL/min的氮气30 min以排除空气,分别于400、500和600 ℃下,将样品进行炭化.炭化完成后,在氮气氛围下,冷却 降温.当温度低于100 ℃后取出炭化样品,静置冷却至室温保存.
称取3.0 g的炭化样品,放入管式炉炉管中,先通入流量为600 mL/min的氮气30 min排除空气,然后通入水蒸气,分别在500、600、700、800 ℃下,将炭化样品进行活化.活化完成后,在氮气氛围保护下,自然降温,温度低于100 ℃后,取出样品,制得的球形活性炭于室温静置冷却并保存.
1.4 活性炭对DL-β氨基异丁酸吸附性能考察
1.4.1 DL-β氨基异丁酸标准曲线的建立
称取DL-β-氨基异丁酸0.10 g,用pH 7.4的磷酸盐缓冲液溶解,并将其定容到1 000 mL(原液),取DL-β-氨基异丁酸原液0、25、50、75、100 mL于100 mL容量瓶中,加入pH 7.4的磷酸盐缓冲溶液定容至100 mL,取样品溶液0.1 mL于试管中,精确加入pH 8.0磷酸盐缓冲液5.0 mL并混合后,再加入1.0 g/L的荧光胺溶液1 mL混匀.静置15 min后,使用荧光分光光度计对该溶液进行分析,测定激发波长390 nm及荧光波长为475 nm下的荧光强度,制成标准曲线.
1.4.2 活性炭对DL-β氨基异丁酸的吸附
将球形活性炭样品100 ℃减压(真空度为0.1 MPa)干燥4 h后,精确称取干燥样品0.5 g,并置于带塞三角烧瓶中.从DL-β-氨基异丁酸原液中取50 mL精确加入上述球形活性炭的三角烧瓶中.将样品置于摇床上,在(37±1)℃、150 r/min条件下震荡3 h.震荡完成后,将三角烧瓶中的溶液以0.45 μm滤头过滤,取10 mL滤液当作样品溶液.
取样品溶液0.1 mL于试管中,加入pH 8.0的磷酸盐缓冲液5 mL,混合均匀后,再加入1.0 g/L的荧光胺溶液1 mL并混匀,静置15 min.应用上述荧光分光光度计检测方法,计算最后DL-β氨基异丁酸残余量.
1.5 活性炭吸附α-淀粉酶的性能
1.5.1α-淀粉酶标准曲线的绘制
取α-淀粉酶0.10 g,加入pH 7.4的磷酸盐缓冲液溶解,定容至1 000 mL(原液),标准曲线是精确取a-淀粉酶原液0、25、75、100 mL置于100 mL容量瓶中,然后用pH 7.4磷酸盐缓冲液将其定容至100 mL,并测定波长282 nm下的吸光度,绘制标准曲线.
1.5.2 活性炭对α-淀粉酶的吸附
取100 ℃真空(真空度为0.1 MPa)干燥活性炭样品0.5 g于带塞的三角烧瓶中.精确量取α-淀粉酶原液50 mL加入三角烧瓶中,放置在150 r/min,(37±1)℃的恒温摇床振荡混匀3 h.将此烧瓶内溶液以滤孔0.45 μm滤头过滤,弃去最初的约20 mL滤液,取剩余的约10 mL滤液作为样品溶液.
于pH 7.4的磷酸盐缓冲液中进行相同的操作,将其滤液当作校正液.样品溶液与校正液以吸光度测定法进行实验,以pH 7.4磷酸缓冲液作为对照,对282 nm波长下的吸光值进行检测,样品溶液吸光度与校正液吸光度的差即为实验组吸光度.以上述标准曲线计算最终溶液中a-淀粉酶的残余量.
1.6 球形活性炭分析方法
1.6.1 热重分析
使用德国耐驰/布鲁克公司的STA449C/QMS403C/TENSOR27型热重分析仪,准确称取一定质量的酚醛树脂,在氮气流下,酚醛树脂由室温35 ℃经1.5 h升温至350 ℃,再经6 h升温至800 ℃,测定热重曲线.
1.6.2 红外分析
利用傅里叶转换红外光谱仪检测活性炭样品,样品和KBr以一定比例混匀,研细后压成片,于500~4 000 cm-1内进行扫描,扫描精度为4 cm-1,扫描频率为32.
1.6.3 孔径及比表面积测定
利用美国康塔仪器公司Autosorb-iQ2型全自动气体吸附分析仪于77 K条件下检测氮气在活性炭样品上的吸附/脱附等温线,依据BET方程对活性炭比表面积进行计算.
2 结果与讨论
2.1 酚醛树脂的合成
2.1.1 原料对制备酚醛树脂的影响
原料对合成酚醛树脂的颜色和形状有着重要的影响.因此,首先对酚醛树脂合成的原料进行了摸索.研究了以多聚甲醛或甲醛为原料对酚醛树脂合成的影响.分别配制苯酚、多聚甲醛-甲醛和三乙烯四胺物质的量比为1∶1.13∶0.04的溶液,使用机械搅拌并油浴加热至回流,可得到固体产物,产物形态见表1.用苯酚、多聚甲醛为原料制备的球形酚醛树脂,干燥后为黄色,且有白色斑点,透明性差.而使用苯酚、甲醛为原料制备的酚醛树脂为黄色球形颗粒,大小均一,透明度好.故此,选择苯酚、甲醛作为合成球形酚醛树脂的原料来进行后续的研究.

表1 不同原料对酚醛树脂合成的影响
2.1.2 转速对球形酚醛树脂粒径大小的影响
在酚醛树脂合成过程中,转速的高低决定了合成酚醛树脂粒径的大小.随搅拌速度增大,反应体系的剪切作用变大,对反应的分散作用显著提高,树脂的粒径变小;当搅拌速度过小时,酚醛树脂容易结块,收率低.因此,为了合理的控制酚醛树脂的粒径大小,对转速条件进行了优化,分别考察了不同转速对球形酚醛树脂粒径大小的影响.从表2的数据可以看出,转速越高,合成的酚醛树脂,粒径在0.35 mm以下的比例越大,粒径在0.50 mm以上的比例越小.在600 r/min转速下获得的产品,粒径在0.35~0.50 mm的比例最大,合格产品所占的比例较高.故此,将获得粒径大小合适产品的最佳条件选定为600 r/min.

表2 转速对粒径的影响
2.2 酚醛树脂的表征
2.2.1 热重分析
对制备好的球形酚醛树脂进行了表征.首先对其进行了热重分析.在氮气流下,自制球形酚醛树脂由室温35 ℃经1.5 h升温至350 ℃,又经6 h升温到800 ℃,35~800 ℃内的热重(TG)和失重速率(DTG)曲线如图1.由图1中失重以及失重速率曲线可知,在127.8 ℃样品失重1%,299.1 ℃样品失重5%,在室温至299.1 ℃可能是树脂球内水分的蒸发以及树脂球内残余的苯酚溢出,导致树脂球质量的下降.在300~600 ℃内,球形树脂快速失重.其中,温度达到370 ℃时,有刺鼻性气味逸出,由失重速率曲线可知,温度达到397.8 ℃时,失重速率达到最大.温度在800.3 ℃时,样品碳化后质量为最初的46.60%,由此推断出该样品残炭率较高.
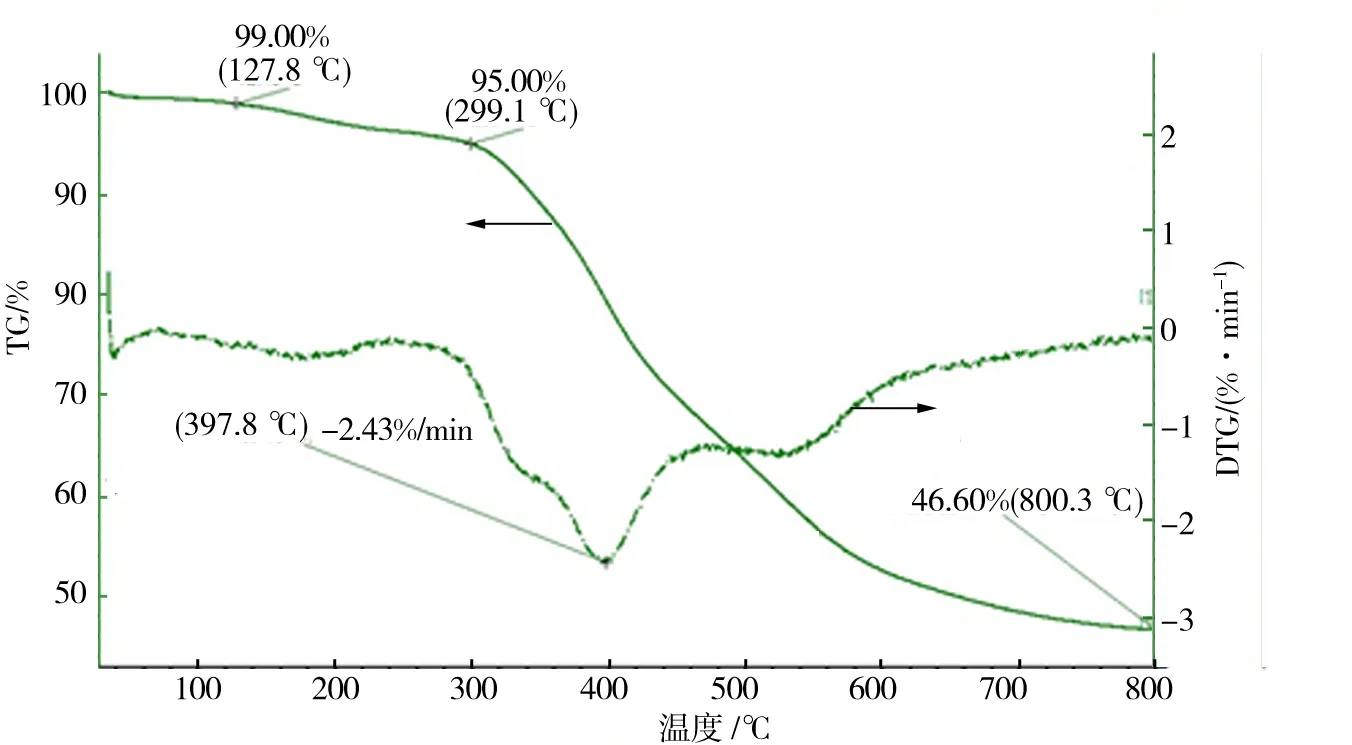
图1 酚醛树脂失重及失重速率曲线Fig.1 Curves of weight loss and weight loss rate of phenolic resin
2.2.2 红外分析
对球形树脂进行红外分析得结果如图2,如曲线所示,在3 600~3 200 cm-1内的宽吸收峰为球形树脂中酚羟基的吸收峰.而1 204 cm-1处的吸收峰是酚羟基C-O的伸缩振动,这是因为合成酚醛树脂的缩合过程中,酚羟基不参与反应进程,故此在产物中得以保留. 2 917 cm-1出现的吸收峰判定为亚甲基(CH2),即在球形树脂合成过程中甲醛中羰基(C=O)形成亚甲基桥连的吸收峰,特征峰在1 500~1 400 cm-1出现.1 593 cm-1处的强尖吸收峰,是苯环骨架上碳碳伸缩振动,由此验证了苯环的存在.而814 cm-1和752 cm-1处分别是苯环对位取代和邻位取代的吸收特征峰.由此推断出,814 cm-1和752 cm-1波长处分别对应的是苯环对位取代和邻位取代的吸收,并且酚醛树脂主要由酚羟基、苯环、亚甲基组成.

图2 球形酚醛树脂红外谱Fig.2 Infrared spectra for spherical phenolic resin
2.2.3 酚醛树脂表面形貌的观测
通过SEM对合成的酚醛树脂表面形貌进行了分析.由图3可知,酚醛树脂的球形较好,球形酚醛树脂表面有少量气孔,并且球形树脂的表面有少量附着的物质.电镜显示球形酚醛树脂的粒径大小在350 μm左右.

图3 酚醛树脂的SEM图Fig.3 SEM image for phenolic resin
2.3 活性炭的合成及其对DL-β氨基异丁酸和α-淀粉酶的吸附
酚醛树脂再分别经过碳化和活化过程就可制备出活性炭.活化过程中需要添加活化剂以提高对样品的活化作用.目前工业上制备活性炭主要包括磷酸法、氯化锌法、氢氧化钾法等化学活化法,其中,化学试剂会对生态环境造成污染,且产品易残留化学药剂,难以满足生产应用的需求.而水蒸气活化法被认为是一种清洁无污染的物理活化方式,广泛应用于活性炭的清洁化生产中.鉴于此,本研究将以水蒸气为活化剂制备活性炭材料.为了获得吸附性能好的活性炭,笔者分别对其合成过程中关键的炭化温度及活化温度进行了优选.
首先,研究了不同的炭化、活化温度对DL-β氨基异丁酸吸附的影响.由图4可知,活性炭随活化温度的提高,对DL-β氨基异丁酸的吸附率不断提高,在600 ℃炭化、800 ℃活化条件下,达到最大的吸附率63.41%.继续提高活化温度到900 ℃时,由于温度过高,使球形活性炭变成粉末状.由此可以看出,在较低温度的活化条件下,活化剂H2O活化作用较低,不能完全活化活性炭,而伴随活化温度逐渐升高,活化剂H2O的活化能力不断增强,当活化温度过高时,活化能力过强,反而对活性炭的合成不利.故此,选择600 ℃炭化、800 ℃活化为活性炭吸附有毒物质DL-β氨基异丁酸的最佳条件.
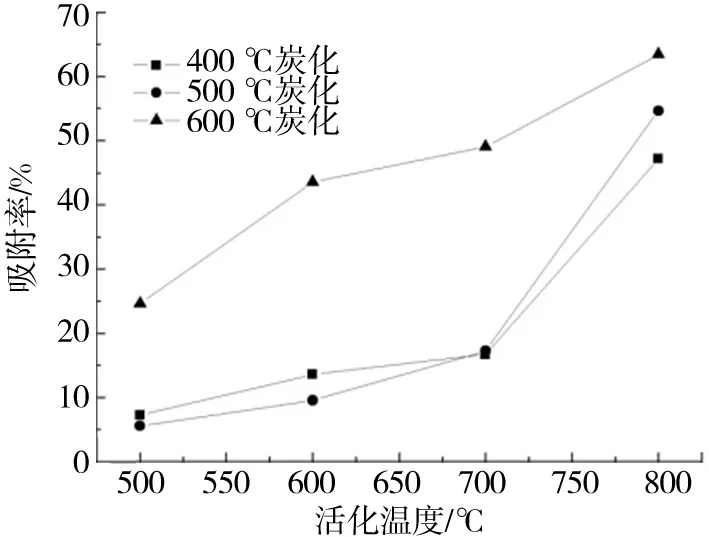
图4 球形活性炭吸附DL-β氨基异丁酸的性能Fig.4 Adsorption rate of DL-β aminoisobutyric acid by spherical activated carbon
将上述最佳条件下制得的活性炭用于对α-淀粉酶进行吸附测定,由图5可知,球形活性炭对α-淀粉酶吸附率仅为19.77%,与相等条件下其对DL-β氨基异丁酸的吸附率(63.41%)相比,吸附率明显低.

图5 球形活性炭吸附有益分子α-淀粉酶的性能Fig.5 Adsorption rate of α- amylase by spherical activated carbon
2.4 球形活性炭的表征
对上述在炭化温度600 ℃、活化温度800 ℃条件下制得的球形活性碳,进行了氮气吸附-脱附等温线、孔径及比表面积进行了分析.
由球形活性炭在77 K下的氮气吸附-脱附等温线可知(图6),活性炭的氮气吸附-解吸等温曲线符合IUPAC定义的I型吸附曲线,此类吸附情况常出现在微孔吸附剂吸附过程中.由于孔壁邻近效应,使得吸附作用大幅提高,在相对压力(p/p0)较小的情况下,吸附量快速增长,即在相对压力很小范围内,微孔就逐渐填满,以后随相对压力的增加,吸附量增加量很少,这种微孔吸附逐渐达到饱和.

图6 球形活性炭氮气吸附-脱附等温线Fig.6 Nitrogen adsorption-desorption isotherm of phenolic resin-loased activated carbon
由上述活性炭性质可以推测,α-淀粉酶具有较大分子质量(约为55 000 ku),存在一定空间构象和空间位阻,因此,小于2 nm的微孔对其吸附几乎不起作用,球形活性炭对其吸附量较小.而DL-β氨基异丁酸分子较小,更容易被吸附在微孔表面,因此活性炭对其显示出较高吸附率.
依据IUPAC对孔径分类的标准,定义r<2 nm为微孔,2 nm
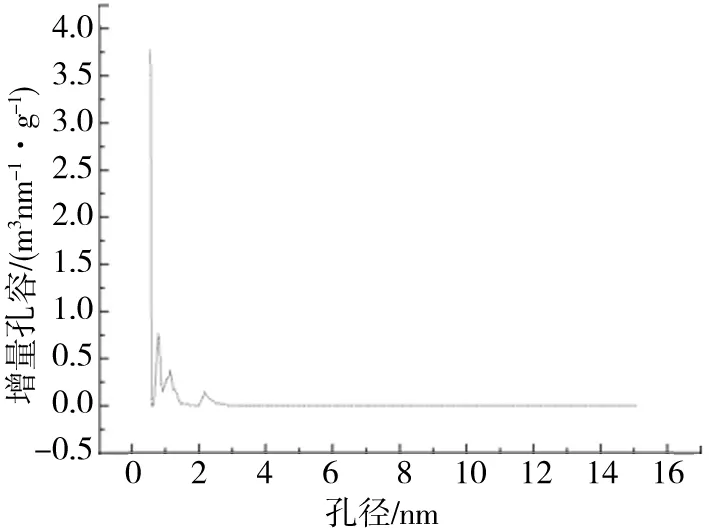
图7 球形活性炭的孔径分布Fig.7 Pore size distribution of spherical activated carbon

表3 球形活性炭比表面积及孔径体积测试分析
3 结论
研究了以苯酚、甲醛和三乙烯四胺为原料合成酚醛树脂的过程,通过优化转速(600 r/min)制备出球型度均一的球形酚醛树脂.并对其进行了炭化和水蒸气活化处理.制备得到的酚醛树脂基球形活性炭符合IUPAC定义的Ⅰ型吸附曲线,孔径分布以微孔(0.5~2 nm)为主,比表面积达到1 431.89 m2/g,对DL-β氨基异丁酸和α-淀粉酶的吸附效率分别为63.41%和19.77%.该研究优化制备得到的酚醛树脂基球形活性炭对有毒分子的吸附脱除效果高,对有益分子的吸附能力低,有潜力作为优良的生物医学吸附材料.
