合并慢性肾功能不全的冠状动脉粥样硬化性心脏病患者冠状动脉搭桥手术的预后及其影响因素
2020-07-21芮宏亮刘韬帅郑居兵徐晓宇宋邦荣
李 扬 董 然* 芮宏亮 刘韬帅 郑居兵 徐晓宇 赵 洋 宋邦荣 张 魁
(1. 首都医科大学附属北京安贞医院心脏外科,北京 100029; 2. 首都医科大学附属北京安贞医院肾内科,北京 100029; 3. 首都医科大学附属北京安贞医院药事部,北京 100029)
合并慢性肾功能不全(chronic kidney disease,CKD)的冠状动脉粥样硬化性心脏病(以下简称冠心病)发病率呈现逐年上升的趋势,心血管疾病是引起CKD患者死亡的主要原因[1-2],两种疾病同时存在增加了冠状动脉搭桥手术的围术期死亡风险[3-4]。对于此类患者的血运重建策略无论是选择经皮冠状动脉支架置入术(percutaneous transluminal coronary intervention,PCI)还是冠状动脉旁路移植术(coronary artery bypass grafting,CABG),肾小球滤过率(estimated glomerular filtration rate,eGFR)的降低都可以导致中远期随访不良事件的升高[5-6]。国内尚缺乏大规模关于CABG治疗合并CKD的冠心病患者的临床效果及中远期预后观察结果。本研究通过对首都医科大学附属北京安贞医院CKD 3~5期患者CABG术后的随访观察,评估治疗效果及其影响预后的因素,为降低手术风险、改善预后提供依据。
1 对象与方法
1.1 研究对象
选择2007年1月至2018年12月1 056例行冠状动脉搭桥手术的冠心病合并CKD患者为研究对象。慢性肾功能不全诊断标准[7]为: eGFR<60 mL·min-1·1.73 m-2。入选患者平均术前肌酐浓度为(184.56±145.93) mmol/L,eGFR (34.57±12.61) mL·min-1·1.73 m-2,CKD 3期患者739例、4期226例、5期91例,术前长期透析患者137例。男性896例(84.8%),左主干病变183例(17.3%),平均冠状动脉病变支数(3.02±0.73)支。
1.2 资料收集
包括术前基本资料、手术相关情况、围术期合并症及病死率、死亡原因,术后恢复情况、住院费用并完成术后中长期随访。术前基线资料主要包括性别、年龄、体质量指数(body mass index,BMI)、eGFR、高血压史、糖尿病史、心肌梗死(以下简称心梗)史、脑梗死史、房颤史、PCI史、颈动脉狭窄、左室射血分数(left ventricular ejection fraction,LVEF)、冠状动脉狭窄情况、血液生物化学指标(血清肌酐、尿素氮、血红蛋白、转氨酶、三酰甘油、胆固醇)等。
1.3 治疗方法
非体外循环下行搭桥手术者占全部患者的88.6%,体外循环手术者占11.4%。术前常规B超检查乳内动脉、左锁骨下动脉及大隐静脉,所有患者均行气管插管静脉复合麻醉,开胸后获取左乳内动脉及大隐静脉备用。不停跳冠状动脉旁路移植术(off-pump coronary bypass grafting,OPCABG)术式:打开心包后肝素化(1 mg/kg),首先使用心表固定器固定左前降支,游离暴露后以7-0/8-0 Prolene吻合左乳内动脉-左前降支。再使用近端吻合器或侧壁钳以6-0 Prolene将静脉远端吻合于升主动脉,然后依次完成对角支、回旋支及右冠状动脉再血管化,必要时采用分流栓技术。体外循环下搭桥术式:给予肝素3 mg/kg,常规建立体外循环后,降温后阻断升主动脉灌注停跳液, 先吻合桥血管与远端靶血管,并经桥血管灌注停跳液,然后行桥血管与升主动脉吻合。开放升主动脉,心脏复跳后,检查桥血管通畅情况及吻合口周围有无出血,充分辅助后撤机,鱼精蛋白中和肝素,彻底止血关胸。2种术式均使用流量仪测定桥血管流量,对于流量不满意者重新进行吻合。平均完成冠状动脉吻合桥数(2.92±0.82)支,OPCABG手术时间(4.16±0.84) h,停跳的冠状动脉旁路移植术(on-pump coronary bypass grafting,on-pump CABG)手术时间(5.89±1.39) h,其中体外循环时间(137±51) min、阻断时间(84±36) min。手术指标还包括了乳内动脉使用情况及全动脉化桥比例等。围术期指标包括呼吸机辅助通气时间、重症监护病房(intensive care unit,ICU)治疗时间,主动脉内球囊反搏(intra-aortic balloon pump,IABP)及体外膜肺氧合器(extracorporeal membrane oxygenation,ECMO)的使用情况,病死率及死亡原因,术后急性肾衰竭的发生率,二次开胸止血、围术期心梗、心律失常、脑梗、感染等合并症发生情况。
1.4 随访观察
所有患者术后通过电话或邮件方式随访,初级终点事件为全因死亡,次级终点事件为主要不良心脑血管事件(main adverse cardiovascular and cerebrovascular events,MACCE)及再次血运重建。随访内容包括全因死亡和MACCE事件(卒中、心绞痛、心肌梗死、再次住院、再次血运重建)及术后新发需要长期透析治疗情况。
1.5 统计学方法
2 结果
2.1 围术期及术后情况分析
围术期死亡64例(6.1%),死亡原因包括心功能衰竭19例、恶性心律失常13例、多器官功能衰竭6例、血流感染8例、肺部感染5例、呼吸衰竭3例、消化道出血3例、脑血管事件5例、其他原因2例。围术期发生急性肾功能衰竭需要透析患者83例, 二次开胸止血51例、 心肌梗死(肌钙蛋白CTnI>0.5 μg/L且合并心电图变化)134 例、新发房颤155例、IABP使用144例、 ECMO使用10例(表1)。
2.2 影响围术期死亡的多因素分析
以是否发生围术期死亡为因变量,以性别、年龄>70岁、术前透析史、BMI异常、高血压史、吸烟史、心梗史、PCI史、脑梗死史、糖尿病病史、房颤史、慢性阻塞性肺病 (chronic obstructive pulmonary disease, COPD)史、心力衰竭、急性心肌梗死、急诊手术、左主干病变、LVEF<35%、左室舒张末期内径(left ventricular end-diastolic dimension,LVEDD)>60 mm、体外循环、贫血及输血与否为自变量,进行多因素Logistic回归分析。结果显示,女性、急诊手术、术前透析史、脑梗史、左主干病变是围术期死亡的危险因素,非体外循环手术则为保护性因素(P<0.05),详见表2。
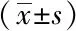
表1 全组患者围术期基线资料

表2 影响围术期死亡的多因素Logistic回归分析
2.3 随访观察结果分析
术后随访916例,随访率92.2%。中位随访时间6(1~11)年。全因死亡58例、病死率6.3%,死亡原因包括心力衰竭15例、心肌梗死11例、肾衰竭8例、脑梗死5例、脑出血4例、其他原因15例。MACCE事件232例,再次血运重建74例,其中PCI 60例、二次CABG 14例。术前无透析治疗,术后肾功能未恢复需要长期透析患者34例(表3)。

表3 主要心脑血管不良事件及再次血运重建
以随访期间是否发生MACCE事件为因变量,以性别、年龄>70岁、术前透析史、BMI异常、高血压史、吸烟史、心梗史、PCI史、脑梗史、糖尿病病史、房颤史、COPD史、心衰史、急性心肌梗死、急诊手术、左主干病变、LVEF<35%、LVEDD>60 mm、体外循环、术后输血、二次开胸止血、围术期心梗、新发房颤、新发透析、术前贫血、三酰甘油及胆固醇异常等为自变量,进行多因素Logistic回归分析,结果显示术前透析史、COPD史及三酰甘油异常是MACCE事件的危险因素(P<0.05),详见表4。
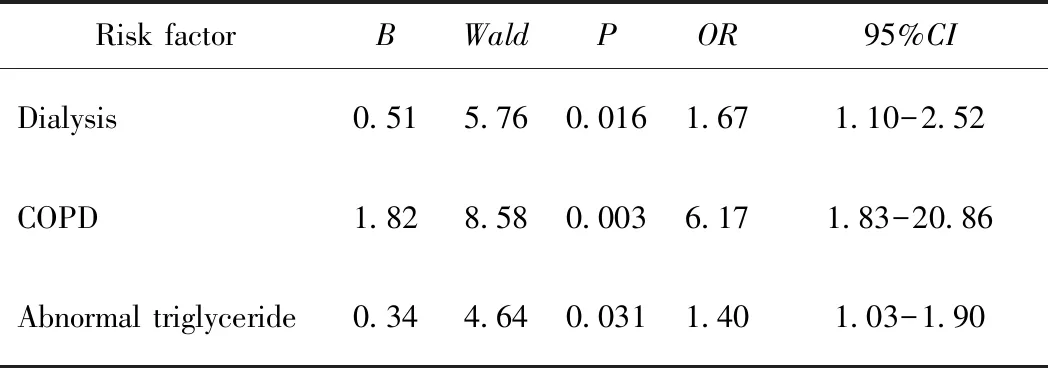
表4 主要心脑血管不良事件独立危险因素分析
3 讨论
冠心病合并CKD的患者行CABG的预后明显劣于肾脏功能正常者[8],这是由于CKD会加重冠状动脉钙化程度及全身动脉系统病变的复杂性,无论选择CABG还是PCI,术后血栓形成、围术期心梗、出血等手术合并症风险均明显高于肾功能正常者[9-11]。国内尚缺乏CABG治疗肾功能中到重度受损的冠心病患者的经验和大规模试验。本研究收集了这部分患者的临床资料,回顾性分析手术效果、围术期合并症、MACCE事件及长期的生存情况,均提示了其较高的手术风险。
目前对于CKD患者血运重建手术策略的选择以及外科手术风险的评估大多是参照先前国外相关研究[12-13],CKD处于3b-5期(eGFR<45 mL·min-1·1.73 m-2)的患者,整体血运重建风险显著提高。国外SYNTAX和FREEDOM 两个大型的冠心病研究[14-15]中CKD患者分别只占16%和7%,这是因为考虑了这部分患者较高的手术危险和手术难度所以纳入较少。有报道[16-17]显示CKD患者行CABG的围术期病死率、二次开胸、脑血管事件、胸骨感染等合并症明显高于正常患者。本研究围术期病死率6.1%,略低于国外报道的病死率12.2%[18]、9.3%[19]、8.9%[20];而术后二次开胸止血率、围术期心梗及脑梗等的发生率分别为6.9%、12.7%和2.6%。有文献[21]显示术前脑梗死史、心源性休克史、急诊手术、合并瓣膜手术、二次手术都是死亡的危险因素,术后脑卒中、输血和急性肾损伤(acute kidney injury,AKI)都与围术期死亡相关,因此减少此类合并症有利于降低病死率。CKD患者术前造血功能异常,常合并贫血状态,会增加术后出血的发生[22]。因此术前纠正贫血状态、减少术后血液制品使用,有利于降低手术风险。如果术前可以把患者按照肾功能不全的严重情况进行分层,选择合适的患者进行手术,会增加手术的安全性。
对于术前不依赖透析的CKD患者,术后发生AKI需要透析治疗的不良事件也是影响外科手术风险及长期预后的重要指标。CABG患者术后透析的发生率高于PCI,这可能与外科手术操作、血管活性药物的使用和体外循环的使用有关[23]。本研究长期随访中,新增长期透析患者34例,发生率较低。国外研究[18]显示对于术前不依赖透析的CKD患者搭桥术后约5%需要短暂的透析治疗,3年内9.3%的患者需要长期透析治疗。体外循环是否增加AKI的发生目前仍然存在争议,许多研究[24-25]显示不停跳搭桥可以减低围术期肾衰竭的发生,但是长期是否有影响还不确定,尤其是对于术前合并CKD的患者。国外研究[26-27]显示术前eGFR正常、30~60和<30的患者搭桥术后透析发生的概率分别为0.2%~1.2%、2.1%和14.5%,本研究围术期AKI的发生率为7.9%,与国外较为接近。
CKD是搭桥术后MACCE事件的危险因素之一[28-29],本研究CABG术后2年78.2%的患者免于MACCE事件,虽然围术期病死率较高、但是长期生存率较为满意[30]。Devbhandari等[31]研究386例CKD患者行CABG后2年的生存率为86.2%,Zakeri等[32]报道了458例患者行CKD术后3年的生存率为81%。本研究长期生存率高于国外的研究[31-32],可能与全组患者男性居多、术前透析较少、心脏功能基本正常、不停跳搭桥比例较高以及贫血状态相对较轻有关。
本研究不足之处在于缺乏有效对照组,此外未对全组患者按照肾功能的损害程度行亚组分析,且为单中心回顾性分析结果,患者的手术效果有待进一步证实。综上所述,合并慢性肾功能不全的冠心病患者行搭桥手术的风险高于普通患者,中长期随访结果较为满意。
