活性炭/氧化亚铜对聚乙烯醇废水的光催化效果研究*
2020-07-20车春波李文欣刘国兴李俊生
车春波 李文欣 刘国兴 谷 芳 李俊生 夏 至 聂 芊
(1.哈尔滨商业大学食品工程学院;2.中国石油哈尔滨石化公司)
0 引 言
聚乙烯醇(PVA)是一种具有多元醇结构的水溶性高分子聚合物,因其化学性能稳定、耐磨性好和黏附性强被广泛应用于纺织、造纸、涂料、医药、化工等行业[1]。PVA对酸、碱和一般微生物都很稳定,且可生化性差[2-3],同时由于PVA分子中带有尺寸较小的羟基,容易生成氢键,使得其具有较大的表面活性,排入水环境中会形成泡沫,影响水体复氧[4-6],PVA还会在水环境中逐渐累积,加快重金属迁移速度,导致更严重的环境问题[7-8]。
半导体材料在光的作用下,产生的电子-空穴对具有较强的还原和氧化能力,能够将有机物氧化直至完全矿化为CO2、H2O及其它简单的无机物,因此,光催化技术由于具有高效、稳定和氧化彻底等优点,在环境治理中具有广泛的应用前景[9-10]。氧化亚铜(Cu2O)是一种P型半导体,其禁带宽度约为2.0 eV左右,可吸收利用太阳光中大部分可见光。自1998年首次利用Cu2O作为光催化剂在可见光下将H2O分解以来[11],Cu2O因其具有可利用太阳光、催化活性较高和可重复使用等优点,在光催化降解有机物领域逐渐成为关注的热点。但是Cu2O粉末存在容易团聚、不易回收和容易造成二次污染等缺点,将粉体Cu2O负载在固态基体上可以有效地解决这些问题[12-14]。活性炭(AC)具有丰富的孔隙结构、大的比表面积和高的稳定性,是一种良好的载体材料[15-16]。
本文以活性炭为载体,采用液相还原法制备了AC/Cu2O光催化剂,并对模拟PVA废水进行光催化降解,考察AC/Cu2O对PVA的处理效果。
1 实 验
1.1 主要试剂
聚乙烯醇(PVA),天津光复精细化工研究所;AC,天津天昌活性炭有限公司;十六烷基三甲基溴化铵(CTAB)、水合肼(80%)、CuSO4、NaOH、H2SO4、H3BO3、I2、KI均为分析纯试剂。
1.2 AC/Cu2O粉末的制备
AC的预处理:取一定量粉末状活性炭,用蒸馏水煮沸30 min后加入浓H2SO4浸泡12 h,用蒸馏水洗至中性,抽滤后放入干燥箱烘干备用。
AC/Cu2O的制备:称取一定量预处理后的活性炭,加入盛有50 mL蒸馏水的烧杯中,超声15 min后得到溶液A,另取一500 mL烧杯加入0.3 g CTAB与50 mL蒸馏水混合后于50℃时磁力搅拌得到透明溶液B,把A与B两种溶液混合后于70℃下继续磁力搅拌,并缓慢加入100 mL浓度为0.1 mol/L的CuSO4溶液得到蓝色溶液,用2 mol/L的NaOH调节溶液pH值为9,老化10 min后得到深蓝色混合液,最后逐滴加入1 0 mL的2 mol/L的水合肼,此时溶液呈深红色,反应3 h后离心得到固体在80℃干燥箱中干燥,得到样品。
1.3 AC/Cu2O粉末对模拟PVA废水的光催化测试
取PVA水样100 mL,调节pH值后加入一定量催化剂,于暗处搅拌30 min以达到催化剂对PVA的吸附平衡,取样测定吸附达平衡后水样中PVA的含量,记为C光照前,再以20 W的白炽灯为可见光光源,照射距离为20 cm,磁力搅拌一定时间后离心取上清液测定光催化降解后水样中PVA的含量,记为C光照后。PVA的具体测定步骤为:取水样5 mL或10 mL转移至50 mL容量瓶中,加入40 g/L的H3BO3溶液15 mL,加入12.7 g/L的I225 g/L的KI溶液4 mL,加水定容至50 mL,显色5 min,用1 cm石英比色皿在波长为670 nm处测其吸光度,根据吸光度与PVA浓度的线性关系得出光照前后溶液浓度的变化,计算PVA的光催化去除率。
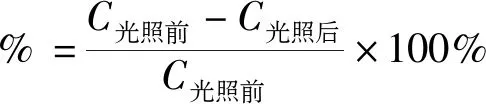
(1)
式中:C光照前为暗搅拌30 min后PVA溶液的浓度,g/L;C光照后为光照一定时间后PVA溶液的浓度,g/L。
1.4 分析测试方法
采用Spectrum100型傅立叶变换红外光谱仪(IR)对预处理前后的AC样品进行有机官能团变化情况分析,采用日本东芝S4700型扫描电子显微镜(SEM)对光催化剂样品进行形貌观察,采用日本理学D/max-γB型X射线衍射仪(XRD)进行光催化剂样品物相分析,PVA溶液的浓度采用PVA标准曲线间接测定[17]。
2 结果与讨论
2.1 AC的预处理结果分析
浓H2SO4处理后的AC表面更加粗糙,有利于Cu2O与AC的牢固负载。由图1可知,经浓H2SO4处理后的AC表面在3 433.37 cm-1处出现明显的—OH伸缩振动吸收峰,在1 623.30 cm-1处出现了C=O伸缩振动吸收峰,在1 038.59 cm-1处出现了C—O伸缩振动吸收峰,说明在AC表面形成了具有还原性的-COOH官能团,能够增强AC在水中的分散性能。

图1 浓H2SO4处理前后AC的红外光谱
2.2 AC/Cu2O粉体的结构分析
AC/Cu2O的XRD图谱见图2。由图2可知,其中29.5°,36.4°,42.3°,61.3°,73.5°的衍射峰分别是面心立方结构Cu2O的晶面特征衍射峰在晶面(111)存在优势取向生长;而在22.8°和33.5°处出现的衍射峰是活性炭特征衍射峰,这说明Cu2O负载在了AC上。随着AC添加量的增大,产物纯度明显提高,且衍射峰强度增强,Cu2O结晶度提高。Cu2O很好地分散在载体表面,Cu2O的形貌呈大小不规则多样性。
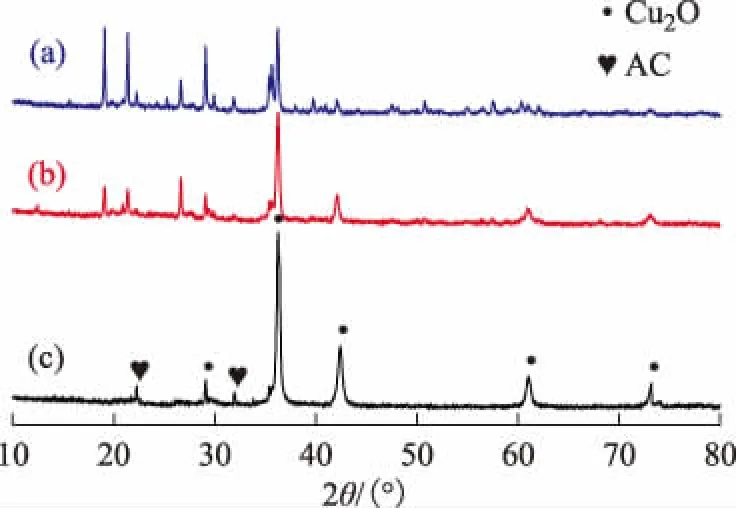
图2 AC/Cu2O的XRD图谱(a)AC含量为0.25 g;(b)AC含量为0.5 g;(c)AC含量为0.75 g
2.3 AC/Cu2O对PVA的催化氧化活性分析
2.3.1 AC/Cu2O光催化活性的单因素实验
实验条件为AC/Cu2O用量1 g/L、pH值为5、光催化反应时间30 min,不同PVA浓度时AC/Cu2O对PVA的去除情况见图3;实验条件为水样中PVA含量75 mg/L、pH值为5、光催化反应时间30 min,不同AC/Cu2O用量时AC/Cu2O对PVA的去除情况见图4;实验条件为水样中PVA含量75 mg/L、AC/Cu2O用量4 g/L、光催化反应时间30 min,不同初始pH时AC/Cu2O对PVA的去除情况见图5;实验条件为水样中PVA含量75 mg/L、AC/Cu2O用量4 g/L、pH值为5,不同光催化反应时间时AC/Cu2O对PVA的去除情况见图6。
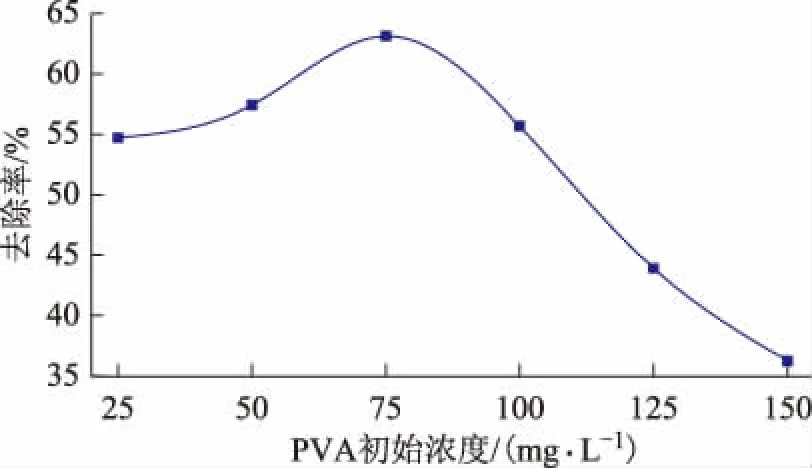
图3 PVA初始浓度对PVA去除效果的影响
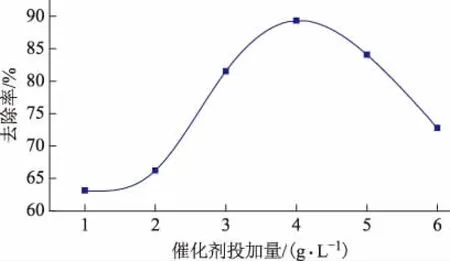
图4 催化剂投加量对PVA去除效果的影响
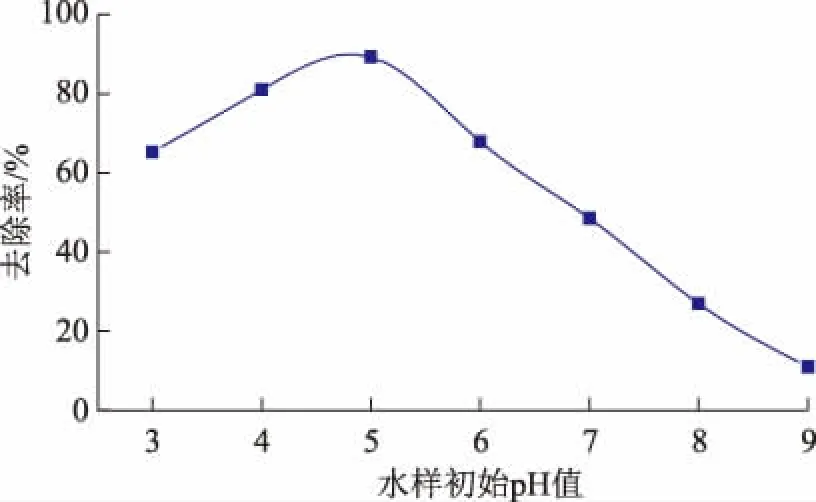
图5 反应初始pH值对PVA去除效果的影响
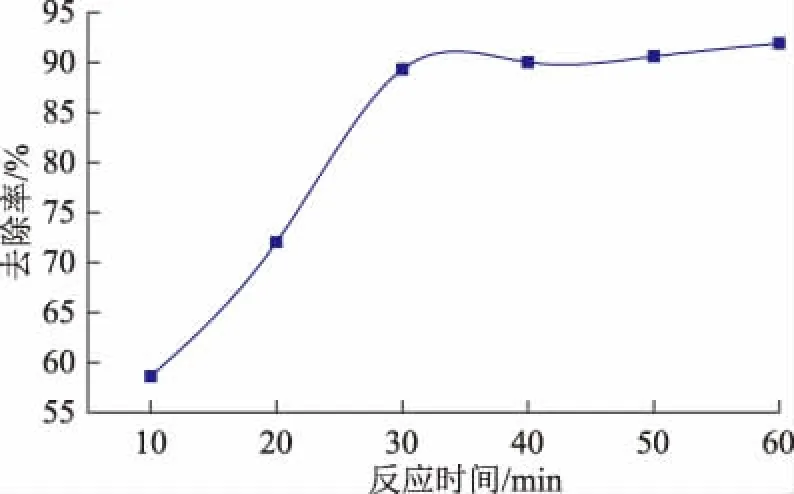
图6 反应时间对PVA去除效果的影响
由图3可知,PVA初始浓度对去除率的影响比较显著且呈先增后减的趋势,在催化剂用量和反应时间恒定时,在反应体系中生成的·OH浓度相同,随着PVA含量的增加,PVA与·OH接触的几率增大,从而使PVA的去除率增大,但是当PVA浓度超过75 mg/L时,体系中的·OH消耗殆尽,导致PVA的去除率降低。由图4可知,随着AC/Cu2O投加量的增大,体系中产生的光生电子-空穴对增多而致使PVA的去除率提高,而当AC/Cu2O投加量过高时,对光的散射作用增强,导致光的利用率下降,AC/Cu2O无法吸收光能而使催化效率降低。由图5可知,pH值对PVA去除效果影响最显著,根据Cu2O光催化机理可知[18],水中的H+和OH-都可参与自由基反应,生成·O2-及·OH,不同pH值的H+和OH-竞争优势不同,在PVA体系中弱酸性条件下催化效果更佳。由图6可知,自由基存在的时间比较短,延长反应时间会使自由基链反应终止,故对PVA的去除率并没有随着时间的延长而提高。根据单因素实验可得最佳处理条件为:PVA初始浓度75 mg/L、催化剂投加量4 g/L、初始pH值为5、反应时间30 min,此条件下的去除率为89.32%。
2.3.2 正交实验设计及结果
根据上述单因素实验所讨论的各因素对PVA去除率的影响,设计正交实验L9(34),各因素中,A为PVA初始浓度(mg/L)、B为催化剂投加量(g/L)、C为初始pH值、D为反应时间(min)。根据单因素实验结果确定各因素的水平,见表1。由L9(34)正交实验各条件得到的PVA去除率结果如表2所示。
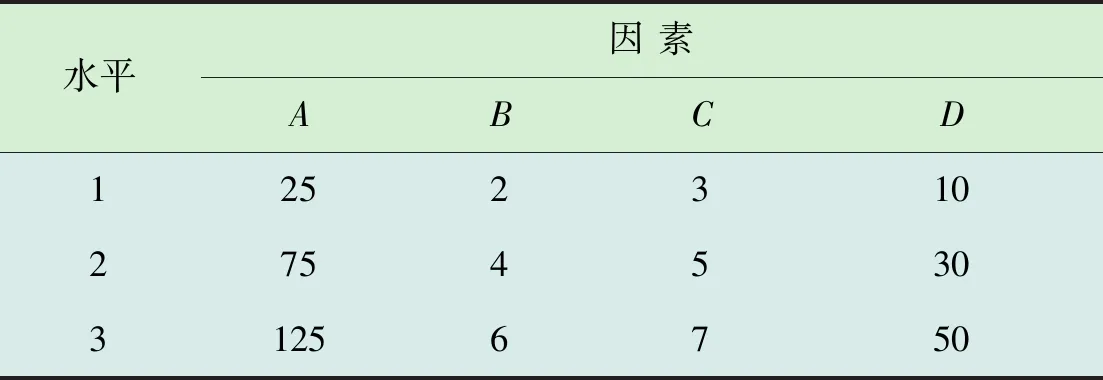
表1 L9(34)正交实验因素水平
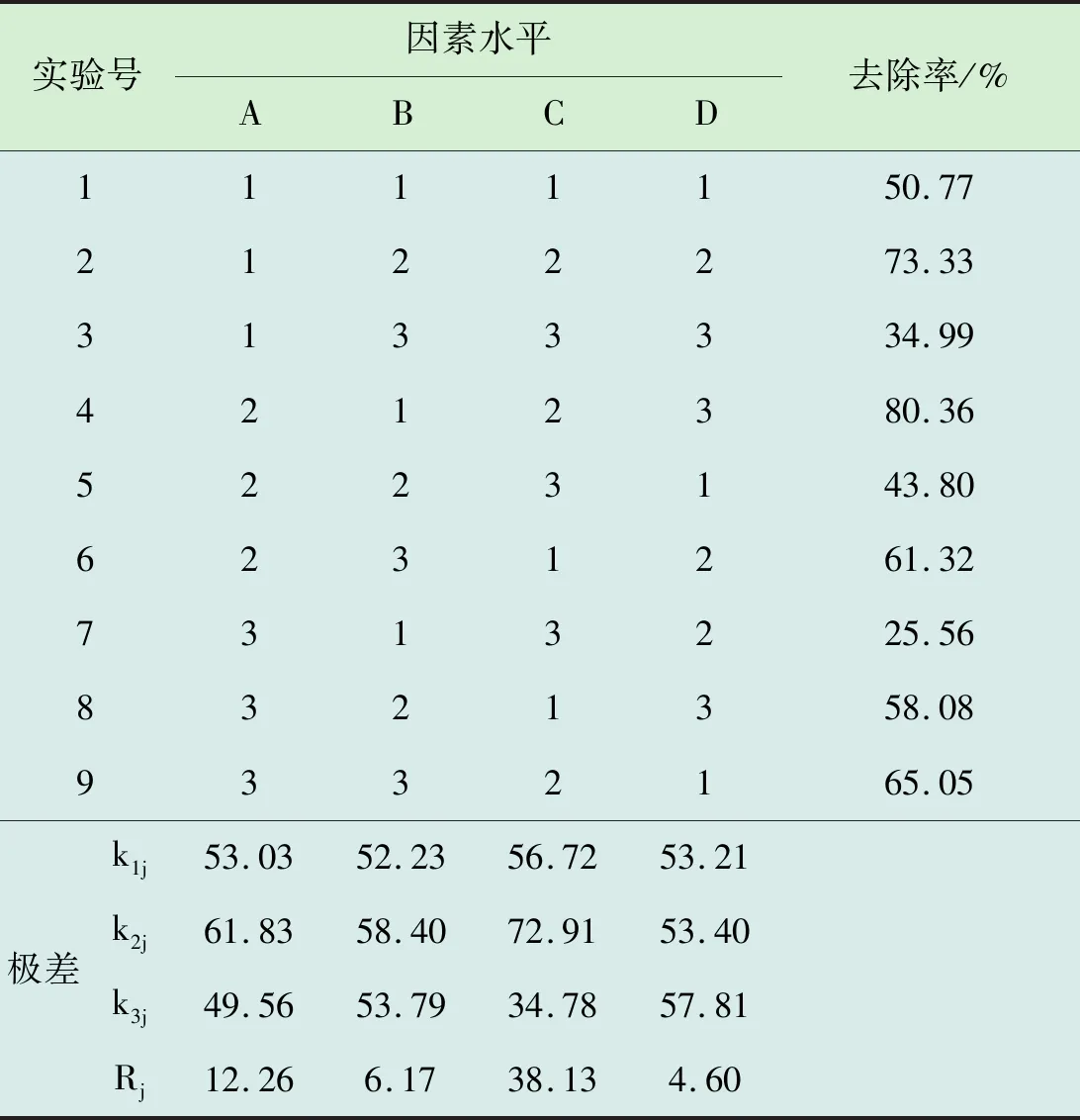
表2 AC/Cu2O催化氧化PVA的正交实验结果分析
由表2在各实验条件下测得的PVA去除率,计算出各因素在不同的水平所对应的去除率的平均值kij(i=1、2、3;j=A、B、C、D),由kij值的大小可以判断出各影响因素的优水平进而确定了最优组合为A2B2C2D3。根据Rj的极差分析可知,在实验中对PVA的去除率影响最大的是水样初始pH值;其次是水样PVA初始浓度;催化剂AC/Cu2O投加量和反应时间对实验结果的影响相对较小。根据对正交实验数据进行分析得出AC/Cu2O光催化降解PVA的条件为:初始pH值为5、PVA初始浓度75 mg/L、催化剂投加量4 g/L、反应时间50 min。在此条件下做三组平行实验测得PVA的去除率为90.60%。
3 结 论
1)以CuSO4为铜源,水合肼为还原剂,AC为载体,制备了AC/Cu2O可见光催化剂。在AC表面沉积的组分为形貌呈大小不规则多样性的Cu2O。
2)在考察AC/Cu2O对PVA的处理效果研究时发现,在可见光条件下AC/Cu2O能够有效地对模拟PVA废水中的PVA进行光催化降解,且效果显著,PVA去除率最高达到90.60%。
