超声造影在肝脏恶性肿瘤局部消融疗效评价中的应用价值及其有效性探讨
2020-07-17郑智文
郑智文
广东省中山市人民医院超声影像科,广东中山 528403
肝脏恶性肿瘤中发生率最高的为肝细胞肝癌,它是临床上常见且侵袭率较高的恶性肿瘤,在我国恶性肿瘤中排第二位[1]。手术切除、肝移植是临床首选方法,但是,大部分肝癌患者确诊时已处于晚期,已经错过了最佳的手术治疗时机[2]。肿瘤消融治疗需要通过影像引导进行,影像引导可以准确定位肿瘤位置、术中引导进针、实时监测治疗过程等,是临床评价局部治疗疗效的重要方法。肝癌局部消融治疗是一种原位灭活手段,对治疗后的效果进行判断非常重要。肿瘤组织不断生长的条件时有滋养血管,因此,对治疗后肿瘤的存活情况进行检查时观察病灶内是否有血流灌注非常重要[3]。临床相关研究显示,超声造影可以对肝脏局部病灶进行鉴别与诊断,对小病灶和消融治疗效果进行准确的检出与评价[4]。我院在肝脏恶性肿瘤局部射频消融疗效评价中,使用超声造影进行检查,结果准确,现报道如下。
1 资料与方法
1.1 一般资料
选取2017年5月~2019年6月我院收治的肝脏恶性肿瘤患者60例,所有患者射频消融术后均进行超声造影检查与增强CT/MRI检查,将病理检查作为金标准。纳入标准:(1)均符合肝脏恶性肿瘤相关诊断标准;(2)经临床病理检查、影像学检查、穿刺检查确诊,且没有肝外转移;(3)近期未接受过其他的局部治疗;(4)均知晓同意此次研究。排除标准:(1)对造影剂存在过敏反应;(2)严重冠状动脉疾病患者;(3)临床各项资料不全。60例患者中男42例,女18例,年龄34~75岁,平均(68.8±1.3)岁;均为原发性肝癌,36个病灶,36例单发结节;48个病灶、24例2个结节,共84个病灶;病灶直径:1.5~5.6cm,平均(3.7±1.5)cm。本研究经我院伦理委员会审批。
1.2 方法
1.2.1 超声仪器 2.5~5.0MHz变频探头超声仪(PHILIPS EPIQ5)。同时配有实时超声造影软件CPS进行低机械指数连续扫描,具备“剪影”成像显示功能,可以将结果自动储存到硬盘当中,可以进行动态或者是脱机逐帧回放。
1.2.2 造影软件 造影成像中根据声压不同可分为低连续成像、高机械指数断成像两种。重复给药前者对微泡破坏小,可以连续成像,简单方便,是较为理想的造影成像方法;后者对微泡破坏大,需要进行间断扫描。
1.2.3 超声造影检查 使用声诺维超声造影剂(意大利),在使用前将其与5mL生理盐水混合溶解,将溶液通过肘正中静脉快速输注后接着注入生理盐水,对患者进行超声造影检查,对血流分布进行记录,对消融治疗效果进行初步评价。继续进行检查,将对比剂注入后进行连续实时扫查(周围异常区、门脉期、动脉期病灶内部情况),延迟期是否有局部提前消退现象。
1.2.4 增强CT检查 使用256排CT螺旋扫描仪(飞利浦)进行检查,参数为:矩阵512×512,层厚/层间隔:10mm,扫描周期:0.8s,250~300ms,电流:150mA,电压:120kV。先进行平扫,后进行增强扫描,使用高压注射器注射(3.0 ~ 4.0mL/s)从肘静脉注射80~100mL对比剂碘海醇(300mg/mL),后进行增强扫描,分别为60s(静脉期)、25s(动脉期)、180s(延迟期)。
1.2.5 MRI检查 使用超导磁共振成像仪(3.0T,飞利浦)以及配套的相控阵列线圈进行检查,层间隔:1~2mm,层厚5mm,梯度场强度:45mT/m。先进性常规T1WI、T2WI加权检查,后进行动态增强扫描,通过高压注射器从肘静脉注射多它灵对比剂进行增强扫描,流速控制在1.52.0mL/s,检查范围为从膈顶至右肾下极。分别进行65s(静脉期)、25s(动脉期)、180s(延迟期)检查。
1.2.6 超声造影时相界定 根据相关标准[1],延迟相:120s以后直到微泡消失,通常为6min;门脉相:30~120s;动脉相:注入造影剂后开始-35s。由于肿瘤自身血供改变会有个体差异,部分患者的显影时间可能会延迟到7min。超声造影检查最终图像由两位临床影像学检查科经验丰富的医师独立进行判断,结果不一致进行讨论决定最终结果。
1.3 观察指标
(1)分析最终检查结果。(2)分析治疗1个月、3个月后的检查结果,主要为肿瘤大小、可疑残留。(3)检查准确性,准确性=(真阳性+真阴性)例数/总例数×100%。(4)分析消融术后超声造影表现。
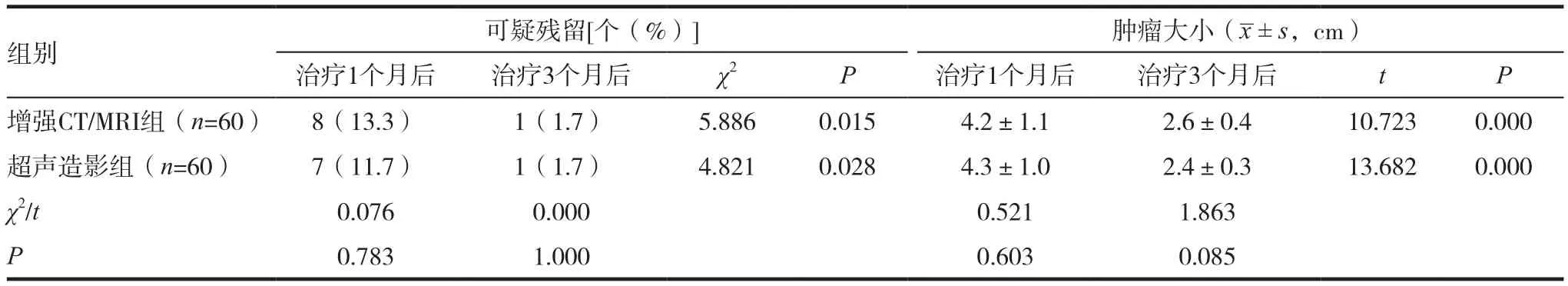
表2 治疗1个月后、3个月后结果比较
1.4 统计学方法
应用SPSS22.0统计学软件进行数据分析,计量资料以(x±s)表示,采用t检验;计数资料以率表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组检查结果比较
两组检查结果比较,差异无统计学意义(P>0.05),病理检查结果中阳性率为3.33%(2例),阴性率为96.67%(58例),超声造影检查结果与增强CT检查均与病理检查的符合率较高,见表1。
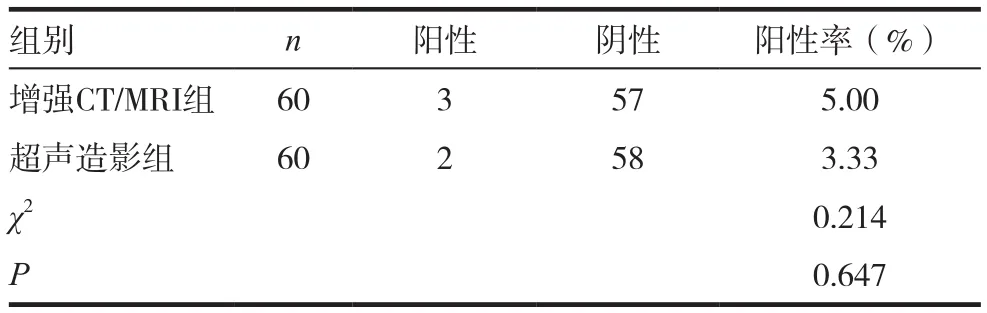
表1 两组检查结果比较
2.2 治疗1个月、3个月后结果比较
两组治疗1个月后、3个月的可疑残留比较,差异无统计学意义(P>0.05),两组治疗后1个月、3个月后肿瘤大小比较,差异无统计学意义(P>0.05),两组组内可疑残留、肿瘤大小1个月、3个月后比较,差异有统计学意义(P<0.05)。见表2。
2.3 两组检查准确性比较
两组的检查准确性比较,差异无统计学意义(P>0.05)。见表3。

表3 两组检查准确性比较[n(%)]
2.4 消融术后超声造影表现分析
消融术后立即行超声造影表现主要为:67个病灶延迟相、门脉相、动脉相无增强;13个病灶表现为延迟相、门脉相表现为低增强和无增强,早期动脉相病灶内部不规则高增强,这与消融治疗前超声造影检查的结果基本相同;4个病灶表现为延迟相、门脉相高增强或等增强,早期动脉相病灶”外周部分环状增强。对比增强CT/MRI检查表现与超声造影表现基本相同。术后超声造影检查见图1~2。
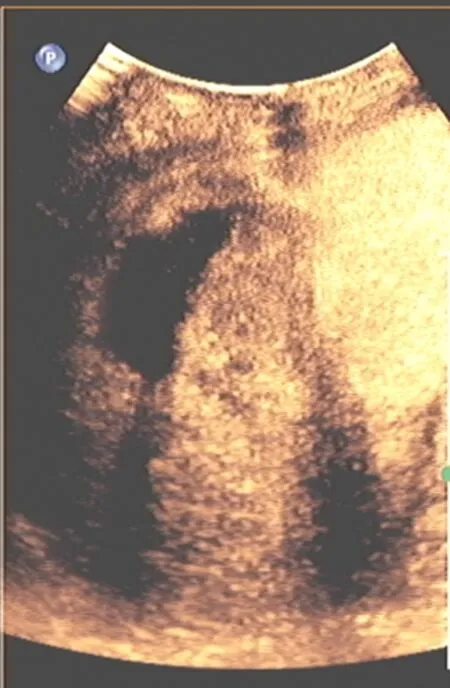
图1 术后超声造影检查
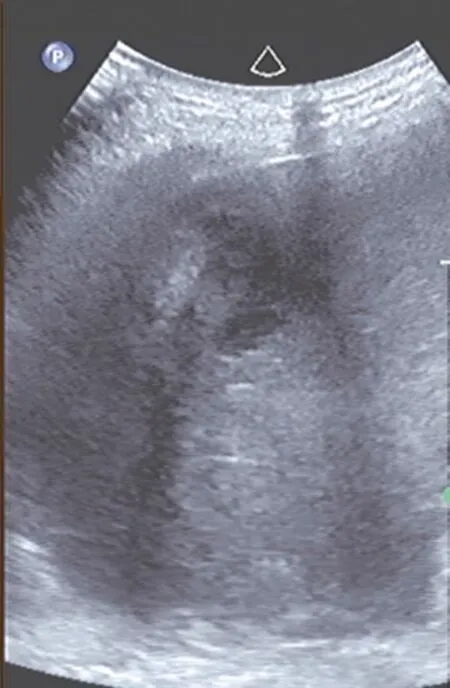
图2 术后超声二维检查
3 讨论
肝癌是临床上发生率较高的恶性肿瘤疾病,近年临床上常用非手术治疗方法。射频消融治疗属于原位灭活手段,但是在进行该方法治疗后对病灶存活情况进行判断对于评价治疗效果非常重要[5]。影像学在评价射频消融治疗后疗效中发挥着关键性作用,临床上通常通过CT/MRI增强,观察治疗后病灶内有无残存肿瘤血供作为治疗有效性的评价标准,这可以为临床进一步治疗残留提供科学依据[6]。射频消融技术需要在超声引导下进行,通过超声检查对疗效、残留情况进行评价有利于准确定位病灶并治疗。近年来临床使用的超声造影检查方法在肝脏恶性肿瘤局部消融治疗疗效评价中,发挥着重要的作用[7]。相关研究显示,超声造影可以对肿瘤治疗部位的微循环信息进行准确的获取,可以实时监测肿瘤强化的过程,可以用于肝脏恶性肿瘤的鉴别,同时也可以用于肝脏恶性肿瘤非手术治疗定位指导、实时监测、疗效评估[8]。
肝脏恶性肿瘤射频消融的疗效影响因素与有无彻底根治存在明显的联系,而根治彻底的主要点在于肿瘤消融范围,消融范围要比肿瘤边界略大(大约0.5~1.0cm),这是提高肿瘤消融疗效,消除肿瘤边缘的关键[9]。超声造影由于可以将低血流信号、低速血流信号检出与显示,且可以快速、直观、实时、动态的对患者情况进行观察,与常规的超声检查方法相比较,超声造影检查方法可以对消融治疗后的病灶内部残留进行有效地检出[10-11]。肝脏本身由于部位特殊、肿瘤体积比较小、硬化等原因使得肝癌病灶在常规的超声检查下无法很好的显示,定位不够准确,无法使临床医务人员准确的对病灶进行治疗[12-13]。而超声造影检查可以对动脉期多血供肿瘤病灶进行清楚的显示,同时可以引导射频消融治疗更加准确,最主要的是可以对射频消融治疗后的疗效进行准确的评估[14-15]。研究显示,两组检查结果比较,差异无统计学意义(P>0.05),病理检查结果中阳性率为3.33%(2例),阴性率为96.67%(58例),超声造影检查结果与增强CT检查均和病理检查的符合率较高,这就说明,肝脏恶性肿瘤局部消融疗效评价中,超声造影与增强CT/MRI检查效果基本相同,超声造影在射频消融后可以较准确的判断肝癌灭活、残留或复发情况,为评估射频消融疗效的有效方法,并可成为治疗早期随访的重要手段。
综上所述,肝脏恶性肿瘤局部消融疗效评价中,超声造影与增强CT/MRI检查效果基本相同,超声造影在射频消融后可以较准确的判断肝癌灭活、残留或复发情况,为评估射频消融疗效的有效方法,并可成为治疗早期随访的重要手段。
