脑转移瘤同期加量混合调强放疗与调强放疗的剂量学比较
2020-07-10曾嵘陈鹏王杰姜琦王尚虎闵旭红
曾嵘,陈鹏,王杰,姜琦,王尚虎,闵旭红
安徽省胸科医院肿瘤放疗科,安徽合肥230022
前言
约30%的癌症患者可能发生脑转移,过去几十年对脑转移瘤有效的放疗手段有全脑放疗(Whole-Brain Radiotherapy,WBRT)[1-2]、放疗手术(Stereotactic Radiosurgery,SRS)或者两者相结合[3-5]。研究表明对于脑转移瘤,WBRT+SRS 相比单独行WBRT 的患者可以获得更长的中位生存期及局部控制率[6]。但是,在完成SRS后进行WBRT之间会出现等待时间,在此间隙会出现亚致死肿瘤细胞的增值和修复,此外SRS 不具备多次分割中肿瘤细胞再氧合的优势[7]。
随着放疗技术的进步,三维适形放疗(Three-Dimensional Conformal Radiotherapy,3D-CRT)、调强放疗(Intensity-Modulated Radiotherapy,IMRT)、旋转调强放疗(Volumetric Modulate Arc Therapy,VMAT)等在全脑放疗联合局部同期加量(WBRT+SIB)方面已得到广泛应用[8-10]。WBRT+SIB 可以获得良好的局部控制率,较好地保护危及器官;相较WBRT+SRS,WBRT+SIB 可以缩短全程放疗时间,消除剂量叠加的不确定性[11]。尽管VMAT 在WBRT+SIB 的应用中相对于3D-CRT以及IMRT有更好的靶区均匀性和适形度[12],但是部分医疗机构并不具备开展VMAT 的条件,3D-CRT 和IMRT 依然是目前最经济有效的选择。IMRT 相较3D-CRT 有更好的靶区适形度,并能减少危及器官的受量[13],但是3D-CRT 的剂量投递效率更高[14],因此两者结合有望获得更好的治疗计划。目前3D-CRT与IMRT联合的混合调强技术(Hybrid-IMRT)已在乳腺放疗中取得了良好的效果[15]。本研究旨在探讨Hybrid-IMRT 在脑转移瘤WBRT+SIB 方面的应用,并对比分析其与IMRT 的剂量学差异。分别设计全脑使用3D-CRT、脑转移瘤使用IMRT 的Hybrid-IMRT 计划和单独使用IMRT 的同期加量计划,对两种计划的靶区适形度和均匀性、危及器官受量、机器跳数等方面进行对比分析,试图给出在技术条件受限的前提下更优的计划方案。
1 材料与方法
1.1 病例选择
随机选取2018年1月至2019年1月期间在安徽省胸科医院进行脑转移瘤放疗的20例患者。其中,男15例,女5例;年龄46~82 岁,平均年龄62.6 岁;体力状态评分(KPS)均大于80。原发灶均来源于肺,其中肺腺癌17例,鳞癌3例。所有患者均通过头颅磁共振扫描确诊,其中单发11例,多发9例(2 个转移灶6例,3 个转移灶3例);脑转移瘤平均体积为26.9 cm3(5.2~105.0 cm3);幕上13例,幕下3例,幕上加幕下4例。
1.2 体位固定及CT扫描
病人均采用仰卧位,双手手掌朝上平放于身体两侧,用热塑头膜加碳纤维板固定患者。采用西门子大孔径128 层螺旋CT 进行扫描,层厚2 mm。扫描后的CT 图像传至Varian Eclipse 计划系统,与MRI 图像进行融合。放疗医生逐层勾画靶区和危及器官。颅内可见转移病灶定义为肿瘤靶区(GTV),沿颅骨内缘至枕骨大孔的脑组织定义为临床靶区(CTV)。CTV 外扩3 mm 定义为计划靶区(PTV),GTV 外扩5 mm定义为计划肿瘤靶区(PGTV)。
1.3 放疗计划制定
处方剂量给予PTV3 600 cGy/20 F,PGTV5 000 cGy/20 F。Hybrid-IMRT计划使用3D-CRT技术两野对穿给予PTV 3 600 cGy/20 F,使用IMRT技术给予PGTV 同期加量1 400 cGy/20 F,两个计划进行叠加。IMRT计划按照PTV、PGTV处方剂量给量。两种计划均达到临床要求,危及器官均不超过正常限值。射线能量选择6 MV X线,剂量率400 MU/min,计划执行机器为Varian23EX直线加速器。Hybrid-IMRT计划中3D-CRT计划设置90°、270°对穿野,同时IMRT计划调整射野角度以达到计划最优。IMRT计划的射野设置为5野均分,角度分别为180°、108°、36°、324°、272°。
1.4 计划评价
两组计划均按处方剂量进行归一,然后分别对比靶区及危及器官的剂量学参数。
(1)靶区的剂量学参数包括靶区最大剂量(D2)、最小剂量(D98)、平均剂量(Dmean)、50%靶区体积剂量(D50)、靶区适形度指数(Conformity Index,CI)、均匀性指数(Homogeneity Index,HI)。CI 和HI 分别根据式(1)和式(2)计算。CI范围为0~1,数值越接近1,代表靶区适形度越好;HI 范围为0~1,数值越接近0,代表靶区均匀性越好。

其中,Vt,ref为处方剂量包绕的靶区体积;Vt为靶区体积;Vref为处方剂量包绕的体积;D2为2%靶区体积剂量;D98为98%靶区体积剂量;D50为50%靶区体积剂量。
(2)比较危及器官(脑干、视神经、晶体、视交叉、眼球)的最大剂量(Dmax)和平均剂量(Dmean)。
(3)根据机器跳数来评估治疗时间。机器跳数越少,治疗时间越短。
1.5 统计学分析
采用SPSS 25.0 软件进行统计学分析,数据用均数±标准差表示。组间采用配对t检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 靶区剂量评估
靶区相关的剂量学参数如表1所示,从表中可以看出两组计划均满足临床要求。图1和图2分别显示了同一例患者的剂量分布图和DVH 图。IMRT 计划的PTV、PGTV 适形度优于Hybrid-IMRT 计划(P<0.05)。Hybrid-IMRT 计划的PTV 的D2、Dmean、D50和PGTV 的D2、Dmean、D50均低于IMRT计划,而且PGTV的均匀性也优于IMRT计划(P<0.05)。其他参数比较均无显著差异(P>0.05)。
表1 靶区剂量学参数比较(± s)Tab.1 Comparison of dosimetric parameters of target areas(Mean±SD)
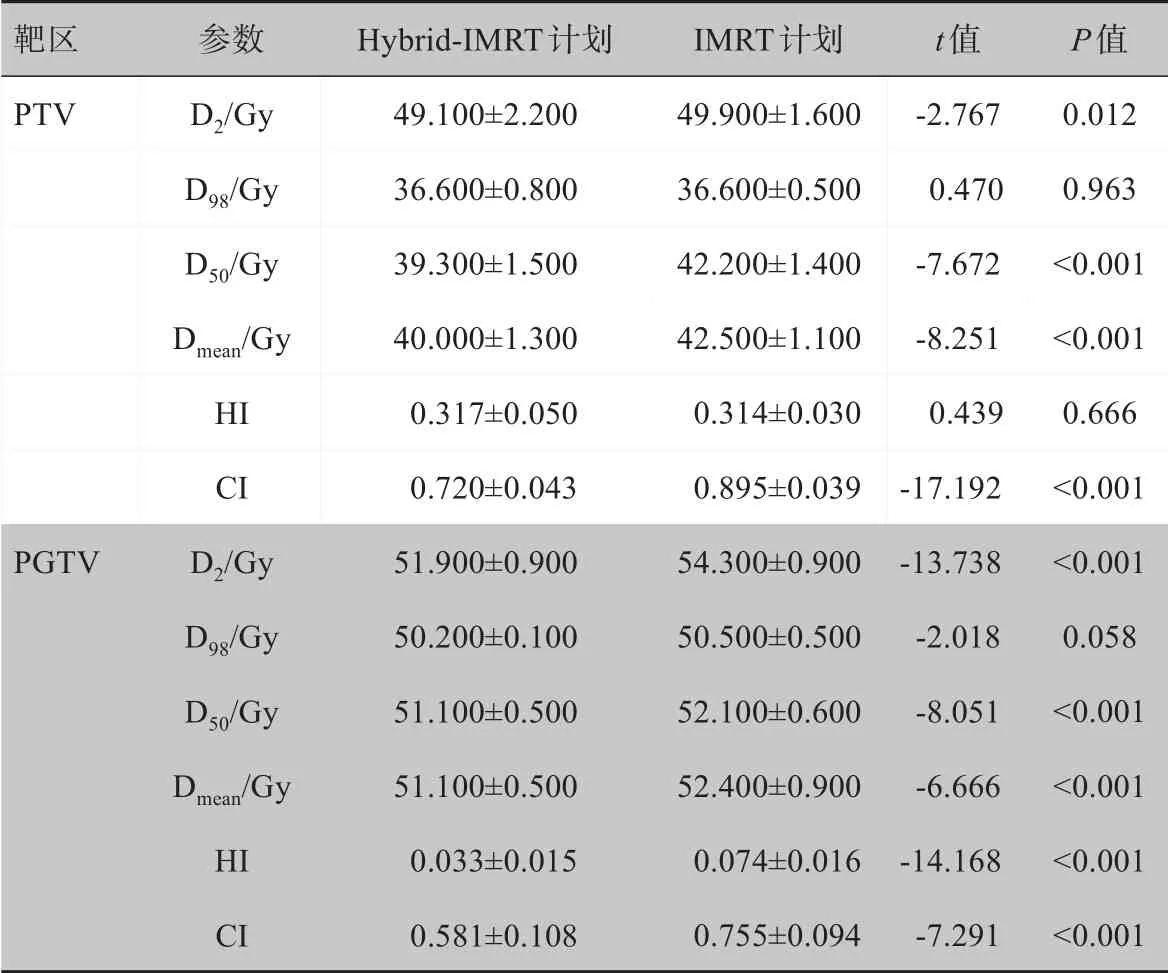
表1 靶区剂量学参数比较(± s)Tab.1 Comparison of dosimetric parameters of target areas(Mean±SD)
靶区PTV PGTV参数D2/Gy D98/Gy D50/Gy Dmean/Gy HI CI D2/Gy D98/Gy D50/Gy Dmean/Gy HI CI Hybrid-IMRT计划49.100±2.200 36.600±0.800 39.300±1.500 40.000±1.300 0.317±0.050 0.720±0.043 51.900±0.900 50.200±0.100 51.100±0.500 51.100±0.500 0.033±0.015 0.581±0.108 IMRT计划49.900±1.600 36.600±0.500 42.200±1.400 42.500±1.100 0.314±0.030 0.895±0.039 54.300±0.900 50.500±0.500 52.100±0.600 52.400±0.900 0.074±0.016 0.755±0.094 t值-2.767 0.470-7.672-8.251 0.439-17.192-13.738-2.018-8.051-6.666-14.168-7.291 P值0.012 0.963<0.001<0.001 0.666<0.001<0.001 0.058<0.001<0.001<0.001<0.001
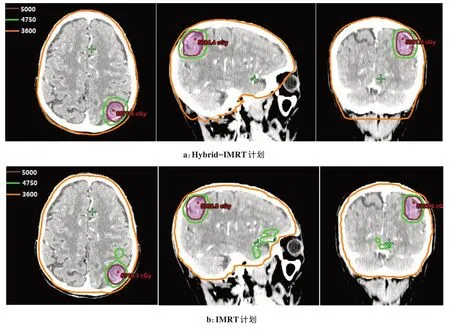
图1 同一例患者Hybrid-IMRT计划与IMRT计划剂量分布对比图Fig.1 Comparison of dose distribution between Hybrid-IMRT plan and IMRT plan for the same patient
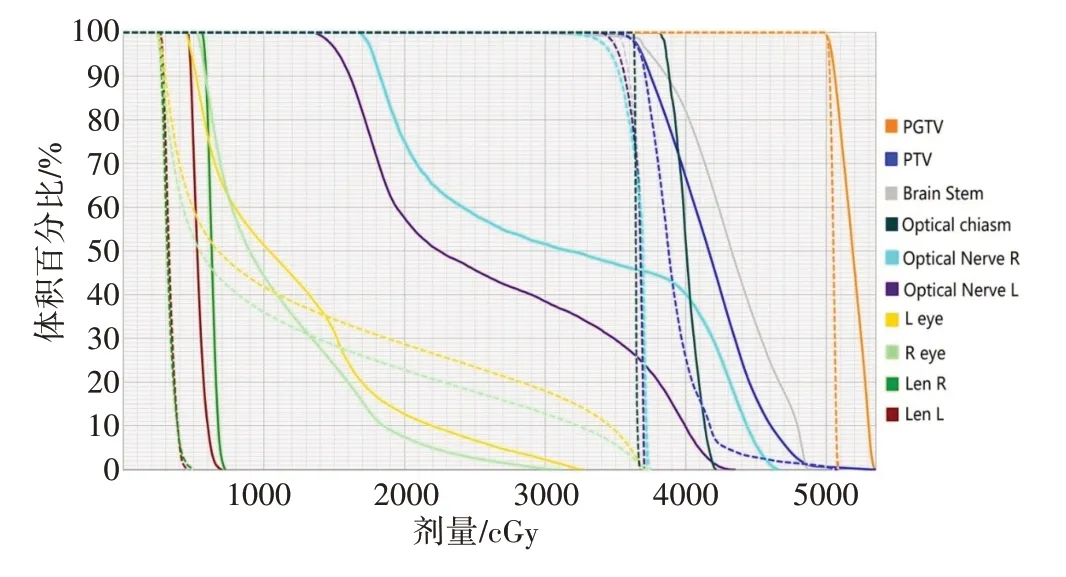
图2 同一例患者Hybrid-IMRT计划和IMRT计划的DVH图对比Fig.2 Comparison of dose-volume histogram between Hybrid-IMRT plan and IMRT plan for the same patient
2.2 危及器官剂量评估
Hybrid-IMRT 计划的脑干、视交叉、左右晶体的Dmax与Dmean,左右眼球的Dmean,左右视神经的Dmax均低于IMRT 计划。IMRT 计划的左右视神经Dmean、左右眼球Dmax低于Hybrid-IMRT计划。详见表2。
2.3 机器跳数评估
Hybrid-IMRT计划的机器跳数为(1 099±108)MU,IMRT 计划的机器跳数为(318±26)MU。Hybrid-IMRT 计划的机器跳数相比于IMRT 计划减少约70%(P<0.001),因此Hybrid-IMRT 计划的治疗时间更短,更有利于病人在治疗过程中保持相同体位,效率越高。
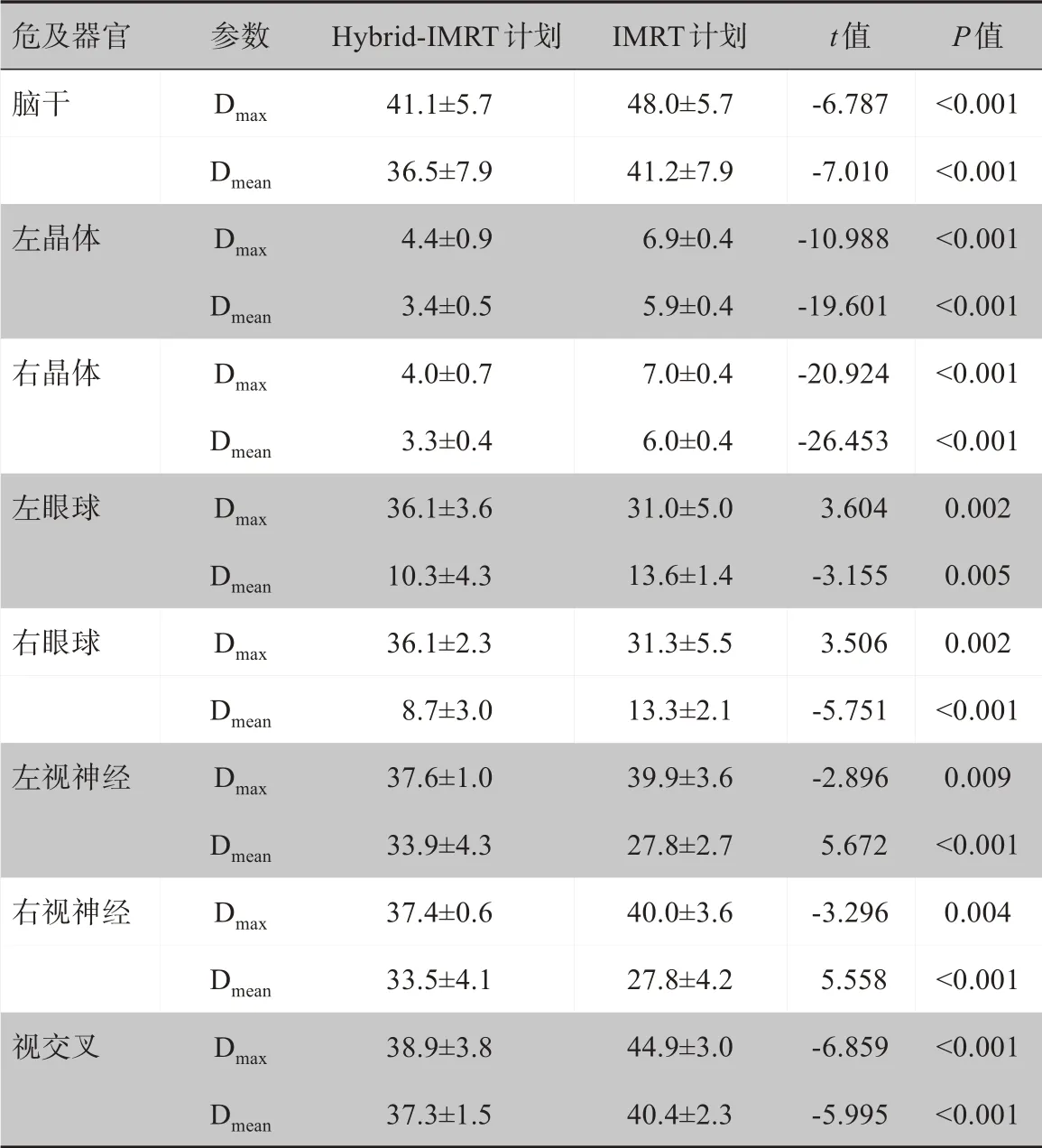
表2 危及器官剂量学参数比较(Gy, xˉ± s)Tab.2 Comparison of dosimetric parameters of organs-at-risk(Gy,Mean±SD)
3 讨论
WBRT在脑转移瘤的治疗中有重要地位。如今,随着技术的进步,WBRT+SIB 已成为3个以下脑转移瘤患者的常规治疗模式。针对IMRT和3D-CRT在脑部肿瘤的应用比较已有大量研究报道[16-19]。Hermanto 等[17]研究了IMRT 与3D-CRT 在脑胶质瘤剂量学方面的比较,得出IMRT 有更好的靶区适形度以及能够更好地保护正常脑组织。邹喜等[18]研究脑转移瘤同步加量使用3D-CRT 与IMRT 的剂量学比较,结果表明IMRT 有更好的适形度,危及器官受量并未有明显差异。倪玲琴等[19]研究认为,针对脑转移瘤同步加量在2~3 个转移瘤且无共层或3~4 个转移瘤且有共层时,剂量学比较上3D-CRT 较优。杨金磊等[14]对脑转移瘤同步加量使用混合适形调强与调强进行对比,认为混合适形调强在剂量投递方面有其特有的优势。
本研究的结果显示IMRT计划的适形度优于Hybrid-IMRT计划,因为Hybrid-IMRT计划是由3D-CRT计划与IMRT计划叠加而成,3D-CRT计划提供了主要的靶区剂量,导致其适形度低于IMRT计划。但是,Hybrid-IMRT计划靶区均匀性优于IMRT计划,同时,Hybrid-IMRT计划靶区Dmax、Dmean优于IMRT计划,尤其是PTV的D50和Dmean大大低于IMRT计划,这说明Hybrid-IMRT计划可减少PGTV以外的正常脑组织的受量。Hybrid-IMRT计划大部分危及器官的Dmax、Dmean均低于IMRT计划,尤其是左、右晶体的Dmax分别平均降低了36.2%、42.9%。但是IMRT计划左右视神经的Dmean以及左右眼球的Dmax更低,这是由于Hybrid-IMRT计划中PTV的剂量是由左右两野对穿使用3D-CRT技术完成,眼球与视神经位于脑组织的凹陷处,剂量无法贴合靶区,导致眼球与视神经的剂量变高。此外,Hybrid-IMRT计划的机器跳数相比IMRT计划减少了约70%,其治疗时间大大少于IMRT计划。
综上所述,尽管IMRT 较3D-CRT 技术手段更加先进,但是对于脑转移瘤放疗同步加量的计划来说,IMRT 计划除了靶区有更好的适形度以外,在危及器官受量、治疗时间以及靶区的均匀性上都略逊于Hybrid-IMRT 计划,尤其是Hybrid-IMRT 计划对于保护正常脑组织具有更大的优势。但是,本研究只分析了3个以下脑转移瘤的情况,当转移瘤数目进一步增加时,Hybrid-IMRT 计划是否还具备上述优势需进一步研究。此外,脑转移瘤位置也会影响剂量学参数,本次所选病例的脑转移瘤位置随机,后续工作将会分别对特定位置脑转移瘤进行更深入的讨论。
