连翘中双四氢呋喃木脂素类化学成分及其波谱特征
2020-07-07阎新佳江园园聂承冬李文兰
阎新佳,江园园,温 静,李 畅,梁 伟,郑 威,聂承冬,李文兰
1哈尔滨商业大学 药学院;2黑龙江省预防与治疗老年病药物研究重点实验室 哈尔滨商业大学药学院,哈尔滨 150076;3哈尔滨医科大学 药学院,哈尔滨 150081
连翘(Forsythiasuspensa(Thunb.)Vahl)是我国的传统中药,早在《本草图经》中就有记载,其味苦,性微寒,归肺、心、小肠经,具有清热解毒、消肿散结之功效,常用于风热感冒、温病初起、温热入营、高热烦渴、热淋尿闭、痈疽、瘰疬、乳痈、丹毒和肿毒等症,被誉为“疮家圣药”。主要分布于我国山西、陕西、山东、安徽西部、河南等地[1,2]。本课题组曾对连翘的化学成分进行过系统的研究,从中得到了一系列结构新颖且具有抗氧化、抗肿瘤和抗菌药理活性的化合物[3-6]。本文对连翘的50%乙醇提取物经多种柱色谱分离纯化,从中分离得到了7个双四氢呋喃木脂素类化合物,分别(+)-8-hydroxyepipinoresinol-4-O-β-D-glucopyranoside(1)、(+)-8-Hydroxyepipinoresin-ol-4′-O-β-D-glucopyranoside(2)、(+)-松脂素-4-O-β-D-葡萄糖苷(3)、(+)-表松脂素-4-O-β-D-葡萄糖苷(4)、(+)-表松脂素-4′-O-β-D-葡萄糖苷(5)、(+)-phyllrin(6)和(+)-pinoresinol(7)。
长久以来,对于双四氢呋喃木脂素类化学成分的相对构型和绝对构型的确认一直是一个难点[7-8],构型上的微小差别可导致其活性的巨大差异,有文献报道[4](+)-8-hydroxyepipinoresin-ol-4-O-β-D-glucopyranoside(1)对5种癌细胞(HL60、A549、Hep-3B、Colo-205和KB)具有显著的细胞毒活性,其活性明显好于阳性药5-氟尿嘧啶(5-Fu),且与紫杉醇活性相当,对人肝癌细胞Hep-3B的细胞毒活性甚至强于紫杉醇(taxol)。双四氢呋喃木脂素8位有羟基,7位处于e键,7′位处于a键,且糖处于4位可能是其具有抗肿瘤活性的条件,其余构型均无活性。所以,立体构型的确认是判断活性化合物的关键。13C NMR可以作为确定相对构型和绝对构型的有力工具[9],本文通过对NMR数据的总结对7个双四氢呋喃木脂素类化合物的13C NMR和CD特点进行了总结,为该类成分结构确认提供理论依据。
1 仪器和材料
核磁共振波谱仪(Bruker AV 600 NMR spectrometer,TMS 做内标);紫外光谱仪(SHIMADZU UV1700);CD光谱仪(Bio-LogicMOS 450)HR-ESI-TOF-MS(Bruker Co.,Karlsruhe,Germany)。高效液相色谱仪(HITACHI,检测器655 variable wavelenth UV Monitor;Waters,检测器2489 UV/Visible Detector);制备色谱柱(YMC ODS-A,5 μm,250×10 mm);分析色谱柱(YMC ODS-A,5 μm,150×4.6 mm)。柱色谱硅胶(100~200目,200~300目,青岛海洋化工厂);薄层色谱硅胶H(300~400目);GF254(青岛海洋化工厂);ODS柱色谱填料(60~80 μm,德国Merck);Sephadex LH-20(北京绿百草);AB-8大孔吸附树脂(中国沧州)。
连翘药材:2009年购于河北安国药材公司(产地:山西),经鉴定为Forsythiasuspensa(Thunb.)Vahl的干燥果实。
2 提取与分离
中药连翘(F.suspensa)的干燥果实8.3 kg,以50%乙醇回流提取3次,每次2 h,合并提取液,浓缩得到的浸膏(出膏率约等于6.51%)依次用氯仿、乙酸乙酯、正丁醇萃取3次,减压回收溶剂得氯仿层40 g、乙酸乙酯层100 g、正丁醇层350 g。
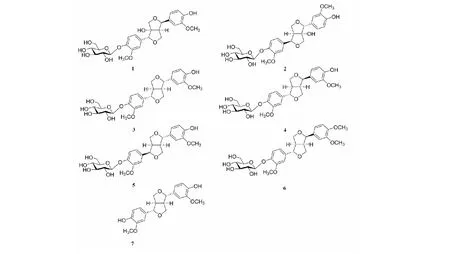
图1 化合物1~7的化学结构
正丁醇层(350 g)部分以适量水溶解后用大孔吸附树脂柱色谱分离,依次用纯水,体积分数10%、30%、50%和95%的乙醇-水梯度洗脱。其中体积分数20%乙醇部分(40 g)经硅胶柱色谱分离,依次用CH2Cl2-MeOH(体积分数100∶1、50∶1、30∶1、20∶1、10∶1、8∶1、5∶1)进行梯度洗脱,得到流分Fr.1~Fr.7。经过反复Sephadex LH-20柱色谱,硅胶柱色谱,聚酰胺柱色谱并结合半制备液相分离纯化得到化合物1~7(图1)。
3 结构鉴定
化合物1~7的13C NMR数据如表1。

表1 化合物1~7的13C NMR光谱数据(150 MHz,DMSO-d6)
4 讨论
连翘中含有大量木脂素类成分,2015版《国家药典》规定将双四氢呋喃木脂素成分连翘苷作为连翘质量控制的指标性成分[10]。双四氢呋喃木脂素类化合物苷元母核结构中共有4个手性碳,但8位和8′位均以cis骈合[11]。故苷元结构中包含3个手性,构型有8种同分异构体[12]。
H-7和H-7′为(R,R)构型时(虚线表示),该化合物旋光值通常为(+),在CD谱中,235和280 nm下为(+)的Cotton效应;反之,H-7和H-7′为(S,S)构型时(实线表示),该化合物旋光值通常为(-),在CD谱中,235和280 nm下为(-)的Cotton效应。连翘中的化合物的旋光值均为右旋(图2)。

图2 双四氢呋喃木脂素类的Cotton效应
在13C NMR(DMSO-d6)谱中,对于苯环取向(直立或平伏键)不同时,C-7/C-7′和C-8/C-8′的化学位移明显不同,可以作为判断苯环取向的特征,而且不受苯环上取代基的影响。4(4′)位为羟基时,当苯环处于平伏键(虚线)时,对应的C-1位上的δC为132.3左右;直立键(实线)对应的δC为129.0左右。当4位羟基被甲氧基取代,1位碳化学位移+1.6;羟基成苷1位碳化学位移+3.0左右[11]。当8或8′位被羟基取代,其对应的1位C的化学位移向高场方向移动(-4.0)(图3)。当1位和1′位苯环均处在直立键时,Cotton效应消失(图4)[12,13]。

图3 取代基的不同对C-1、C-1′化学位移值的影响

图4 当1/1′位为a键时无CE
连翘中含有大量四氢呋喃型木脂素,该类化合物遇到酸碱条件容易发生立体异构化(a键与e键互换):是由于呋喃环上的氧原子与苯甲基相连,容易开环,重复闭环时发生构型变化[14](图5)。
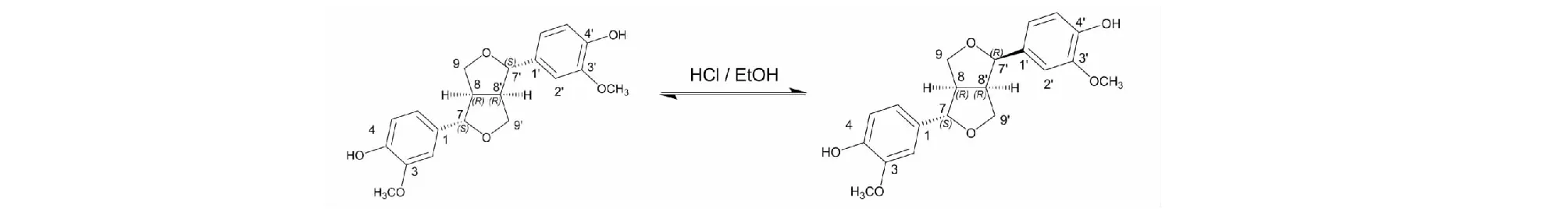
图5 四氢呋喃型木脂素遇到酸碱条件容易发生立体异构化
双四氢呋喃木脂素结构中手型碳较多,其构型的确定一直以来是个难点问题。本文总结了13C NMR谱和CD谱的相关数据,通过总结发现具有一定的规律,对今后确认连翘中的此类化合物以及其他植物中此类化合物的绝对构型具有借鉴意义。
