HPLC-PAD法测定西洋参类保健食品中10种皂苷的含量
2020-07-06吴晓云刁飞燕李秀慧刘春霖李启艳
吴晓云,刁飞燕,李秀慧,刘春霖,李启艳
(山东省食品药品检验研究院,山东 济南 250101)
西洋参为五加科人参属植物,是名贵的中药材,人参皂苷是其主要活性成分,主要有人参皂苷Rg1、Rb1、Rb2、Rc、Rd和Re等。以西洋参为原料的保健食品具有缓解体力疲劳,增强免疫力、抗氧化和抗肿瘤等作用[1]。目前,西洋参类保健食品的剂型有硬胶囊、软胶囊、片剂和口服溶液等,主要以总皂苷作为标志性成分,总皂苷的测定主要采用香草醛-高氯酸或硫酸显色后用紫外分光光度法测定[2],该方法存在专属性差,操作复杂和干扰因素多等缺点。
为此,徐灿辉等[3]改进了西洋参类保健食品中人参皂苷测定方法,建立了西洋参类保健食品中7种参皂苷含量高效液相色谱(HPLC)测定的方法。此外,人参皂苷测定方法还有超高效液相色谱(UPLC)[4]、高效液相色谱-质谱联用法(HPLC-MS)[5-6]等。在众多资料中,主要研究西洋参根茎叶提取物中人参皂苷含量,但对西洋参类保健食品中10种人参皂苷含量测定的报道较少。
本试验通过参考西洋参药材中皂苷测定的有关文献[7-9],建立高效液相色谱法同时测定多种剂型西洋参类保健食品中10种人参皂苷,为质量标准的提升提供依据。
1 试验部分
1.1 仪器 液相色谱仪(Agilent 1260 高效液相色谱仪,美国安捷伦公司), 配二极管阵列检测器(PAD);电子天平(Mettler Toledo MS,梅特勒-托利多);数控超声波清洗器(KQ-500DE型,昆山市超声仪器有限公司);恒温水浴锅(北京永光明)。
1.2 试药与供试品 乙腈(色谱纯,Honeywell);甲醇(色谱纯,Honeywell);超纯水;正丁醇(分析纯,国药集团);氨水(分析纯,国药集团)。
标准品:人参皂苷Rb1、Rb2、Rb3、Rg1、Rg3、Rd、Re由中国食品药品检定研究院提供,含量分别为95.9%、93.8%、97.0%、96.3%、100%、94.4%、97.4%,人参皂苷Rg2、Rc、Rf由上海甄准生物科技有限公司提供,含量分别为98.02%、99.11%、99.62%。
供试品均由市场购得,名称与剂型见表1。
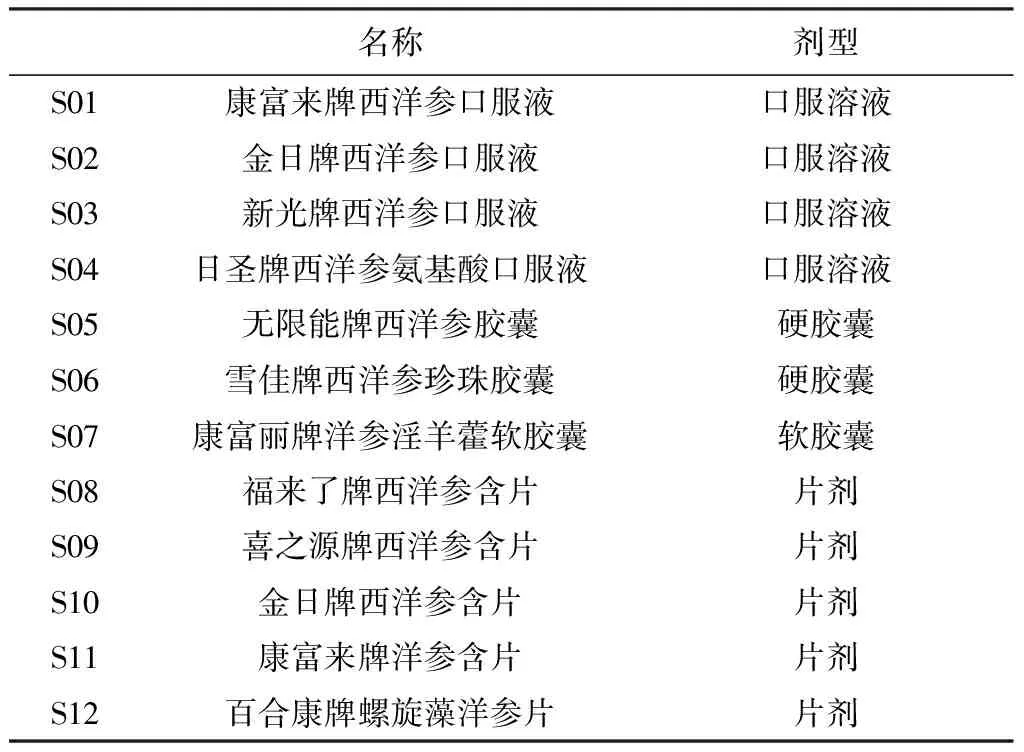
表1 12种供试品的名称和剂型
2 方法与结果
2.1 色谱条件 色谱柱:Kromasil C18(4.6 mm×250 mm,5 μm);流动相:乙腈(A)-水(B),梯度洗脱(0~40 min,17%A→19%A;40~60 min,19%A→29%A;60~75 min,29%A;75~100 min,29%A→40%A;100~105 min,40%A→17%A);流速1.0 mL·min-1;检测波长203 nm;柱温35 ℃;进样量:10 μL。
2.2 对照品储备液及对照品混合工作液配制 分别精密称定人参皂苷Rg1、Rg2、Rg3、Rb1、Rb2、Rb3、Rc、Rd、Re、Rf对照品适量,置于25 mL量瓶中,用甲醇溶解并定容,制成人参皂苷单体浓度分别为2.409、2.141、0.047 12、1.947、1.758、2.138、2.250、2.062、2.077、2.008 mg·mL-1的对照品储备液。分别取10种人参皂苷对照品储备液适量,加甲醇稀释制成6个浓度的混合对照品工作液。
2.3 供试品溶液的制备
2.3.1 片剂、胶囊剂供试品溶液的制备 片剂、胶囊剂,取内容物研磨混匀后,片剂2 g,胶囊剂1 g,精密称定,置于100 mL锥形瓶中,精密加水饱和正丁醇50 mL,密塞,放置过夜,超声处理(功率250 W,频率50 kHz)30 min,滤过,弃去初滤液,精密量取续滤液20 mL,用氨试液洗涤两次,每次20 mL,正丁醇提取液蒸干后,残渣加甲醇适量使溶解,作为供试品溶液。
2.3.2 口服溶液供试品溶液的制备 口服溶液,精密量取8.0 mL供试品至分液漏斗中,用水饱和正丁醇振摇提取3次,每次10 mL,合并正丁醇提取液,用氨试液洗涤2次,每次10 mL,正丁醇提取液蒸干后,残渣加甲醇适量使溶解,作为供试品溶液。
2.4 线性关系考察 分别取6个浓度的混合对照品工作液,进样10 μL,记录峰面积,以对照品浓度X(μg·mL-1)为横坐标,对照品的峰面积Y为纵坐标,绘制标准曲线,求得回归方程。得到10种人参皂苷在相应线性范围内均具有良好的线性,相关系数都在0.99以上,结果见表2。
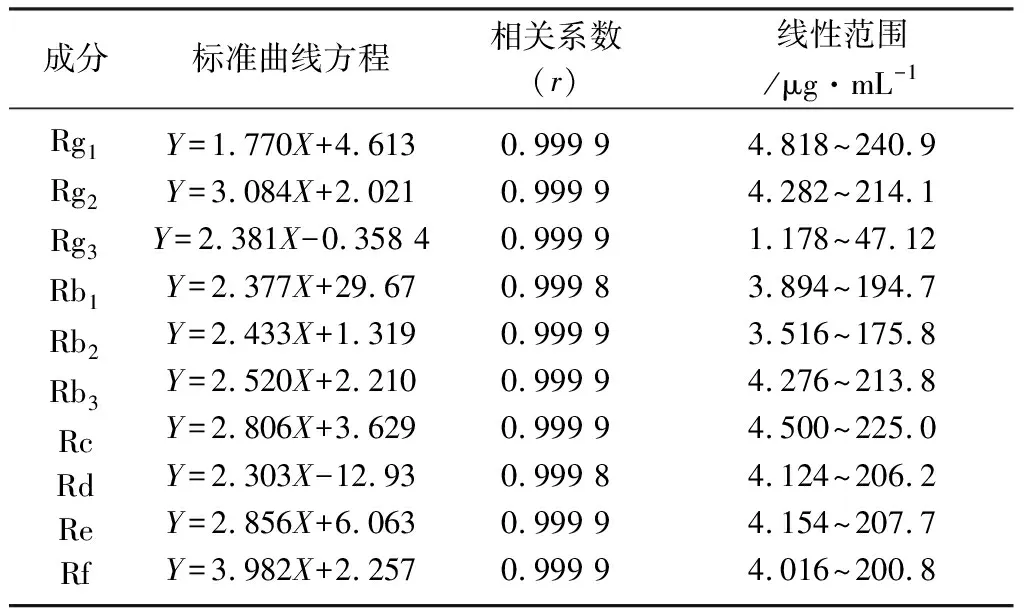
表2 标准曲线方程的结果
2.5 试样重复性试验 准确量取6份口服溶液供试品(S01)8.0 mL至分液漏斗中,以下按“2.3.2”项下方法操作,制备供试品溶液。
准确称取6份胶囊剂供试品(S05)1 g,6份片剂供试品(S08)2 g,置于100 mL锥形瓶中,以下按“2.3.1”项下方法操作,制备供试品溶液。
分别取3种剂型供试品溶液10 μL注入液相色谱仪,以保留时间定性,测定峰面积,计算供试品中10种人参皂苷的含量。3种剂型供试品中人参皂苷含量RSD(n=6)均小于3%,结果表明方法重复性良好,结果见表3。
2.6 系统适应性考察 取10种人参皂苷混合对照品工作液10 μL进样,计算10种人参皂苷的理论板数。得到人参皂苷Rg3、Rg1、Re、Rf、Rg2、Rb1、Rc、Rb2、Rb3、Rd的理论板数分别为103 427、50 732、104 490、157 284、120 457、82 876、253 440、260 991、410 628、239 554,分离度分别为5.4、1.6、32.6、15.1、2.2、4.0、4.8、1.6、8.0。对于供试品,虽然存在基质干扰影响分离度,但是3种剂型供试品中10种人参皂苷均能达到基线分离,分离度均能达到1.5以上。
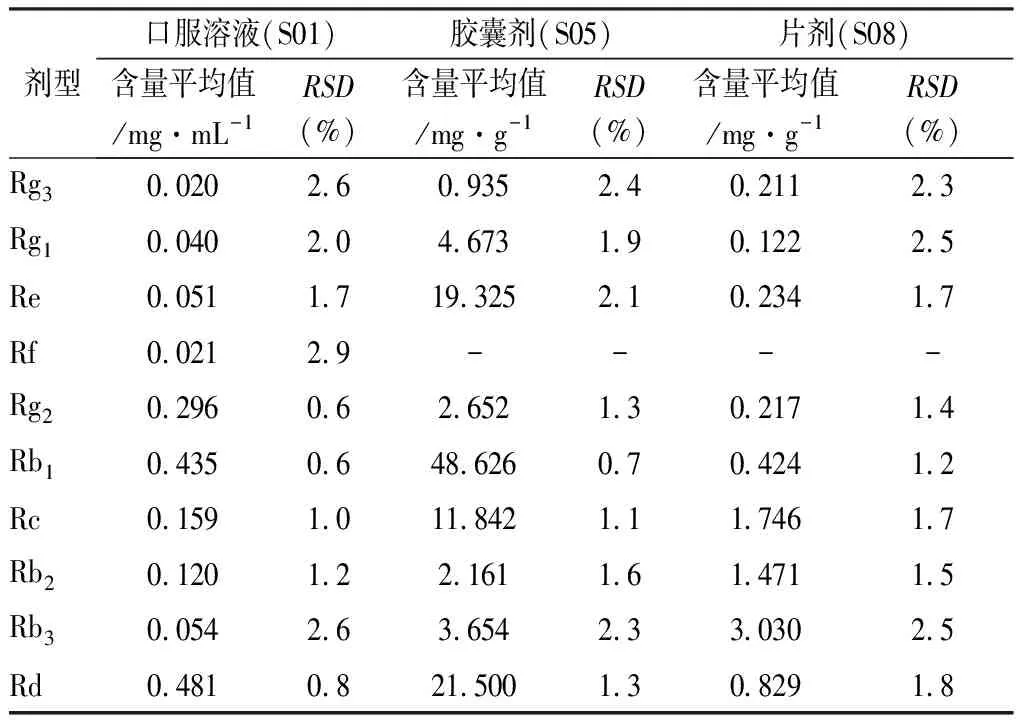
表3 重复性试验结果
注:“-”表示未检出或低于定量限
2.7 精密度试验 取10种人参皂苷混合对照品工作液10 μL连续进样5次,以测得的峰面积响应值作评价标准,得到10种人参皂苷的RSD(n=5)均小于3.0%,表明在本方法仪器条件下,仪器精密度良好。
2.8 稳定性试验 分别取供试品S01、S05、S08,按“2.3”项下方法操作,得到供试品溶液,室温下放置24 h,分别在0、2、4、8、12、24 h取10 μL进样,得到10种人参皂苷峰面积RSD(n=6)都在3.0%以内,表明供试品溶液在24 h内稳定。
2.9 回收率试验 准确量取6份已知含量的供试品(S01)4.0 mL至分液漏斗中,分别精密加入人参皂苷对照品储备液适量(对照品加入量与供试品中各人参皂苷含量之比为1∶1),以下按“2.3.2”项下方法操作,即可得到加标溶液。
准确称取已知含量的供试品(S05)0.5 g,供试品(S08)1 g,各6份,分别精密加入人参皂苷对照品储备液适量(对照品加入量与供试品中各人参皂苷含量之比为1∶1),置于100 mL锥形瓶中,以下按“2.3.1”项下方法操作,即可得到加标溶液。
取10 μL注入液相色谱仪,以保留时间定性,测定峰面积,得到10种人参皂苷的平均加样回收率(n=6),RSD均小于4.0%,结果见表4。

表4 回收率结果
注:“-”表示未检出或低于定量限
2.10 检出限与定量限 S/N=3时,得到检出限LOD,人参皂苷Rg1、Rg2、Rg3、Rb1、Rb2、Rb3、Rc、Rd、Re、Rf检出限分别为0.002 4、0.002 1、0.002 9、0.001 9、0.001 8、0.002 1、0.002 2、0.002 1、0.002 1、0.002 0 μg;S/N=10时,得到定量限LOQ,定量限分别为0.006 0、0.005 4、0.007 4、0.005 0、0.004 4、0.005 3、0.005 6、0.005 2、0.005 2、0.005 0 μg。
2.11 供试品的测定 取12批供试品,按照按“2.3” 制备供试品溶液,每批平行处理2份,按上述色谱条件进行测定,将峰面积代入“2.4”线性回归方程计算含量,结果见图1~2及表5。
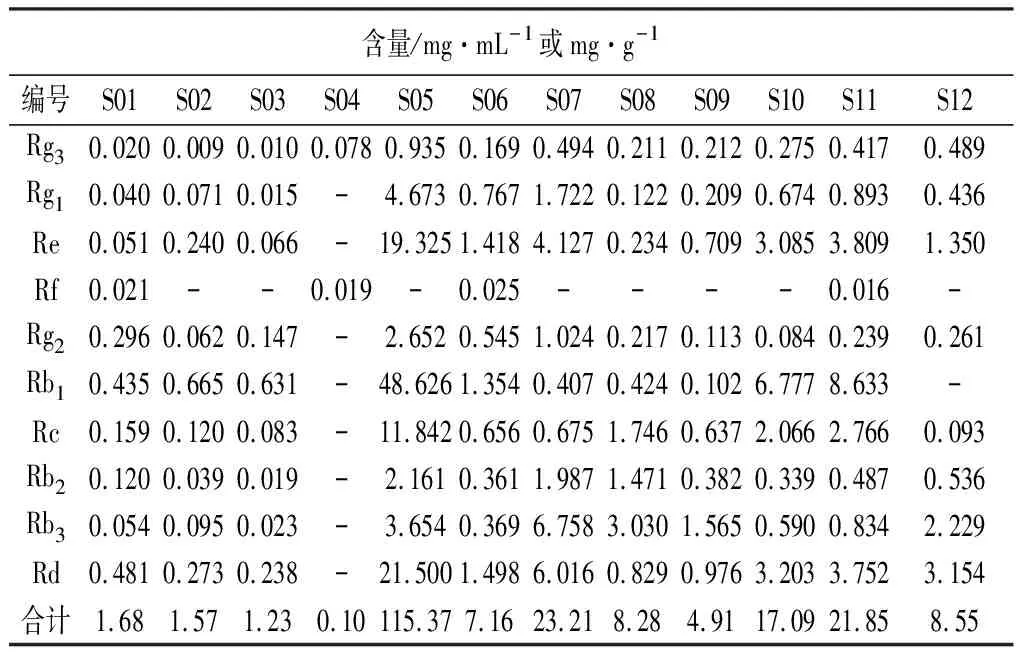
表5 供试品中10种成分含量测定结果
注:“-”表示未检出或低于定量限
3 讨论
3.1 前处理考察 由于保健食品剂型种类多,而每种剂型的基质比较复杂,导致10种人参皂苷更难同时分离。首先,通过比较3种不同的提取试剂,水饱和正丁醇、甲醇和乙醇,最终得到水饱和正丁醇提取效率最高。其次,选用水饱和正丁醇分别采用回流提取、液-液萃取、浸泡放置过夜超声提取和直接超声提取4种提取方式进行比较,结果表明:对于片剂和胶囊剂,浸泡过夜超声提取与回流提取得到皂苷含量最高,又因为前者操作简单,且提取的多糖等杂质较少,最终采用浸泡过夜超声提取;对于口服溶液,回流提取与液-液萃取都能得到较高总皂苷含量,优先选取重现性好且操作较简单的处理方法,因此采用水饱和正丁醇振摇多次萃取。
3.2 流动相及梯度的选择 本文对甲醇-水,乙腈-水和乙腈-0.1%磷酸溶液3种不同流动相进行比较,结果表明,人参皂苷在低波长范围内检测时,乙腈比甲醇背景噪音低,可获得较好的分离效果,并且乙腈与水混合黏度小,可以有效降低系统压力,而加入磷酸对整体分离情况没有明显改善且磷酸盐对色谱柱损耗大,最终选择乙腈-水作为最佳流动相。
10种人参皂苷中Rg1和Re,Rb2和Rb3较难分离。人参皂苷Rg1和Re极性非常相似,较难分离,且供试品在人参皂苷Rg1和Re附近有杂质干扰,最终选择合适梯度,在45 min 左右达到基线分离。Rb2和Rb3是同分异构体,并且两者含量很低,容易包裹在杂质峰中,本试验在保证峰形和柱效的前提下完成了两种皂苷的基线分离。故最终采用梯度洗脱使每种皂苷达到较好分离效果。
3.3 样品测定结果分析 由表5可见,12批供试品10种皂苷含量之和差异很大,含量最高的为硬胶囊,片剂和软胶囊次之,口服溶液最低。每批供试品中,单种人参皂苷占10种皂苷比例各不相同,经过分析发现,Rb1、Rc、Rd、Re 4种所占比例最大,7批供试品含这4种皂苷比例为67.0%~88.5%,4批供试品的比例为39.0%~53.8%,1种供试品(S04)比例为0。对于供试品(S04),根据《保健食品检验与评价技术规范》(2003年版)中规定的紫外分光光度法进行总皂苷检测,得到总皂苷含量为80 mg·100 mL-1。本文建立的HPLC-PAD法可对西洋参类保健食品中皂苷成分进行初步鉴定,最终用紫外分光光度法进行总皂苷检测。
4 结论
本文共收集口服溶液、片剂和胶囊剂12批西洋参类保健食品,通过测定其线性范围、系统适用性、重复性、精密度、稳定性、检出限、定量限和回收率试验,结果令人满意。试验表明,在本文供试品制备方法和色谱条件下,人参皂苷Rg3、Rg1、Re、Rf、Rg2、Rb1、Rc、Rb2、Rb3、Rd能够达到完全分离,所建立的方法操作简便,重复性好,可以用来对以西洋参为原料的保健食品进行质量控制。
