疏水性低共熔溶剂对水中5种非甾体抗炎药物的萃取研究
2020-07-06张华陈强刘永静
张华,陈强,刘永静
(福建中医药大学药学院,福建 福州 350122)
低共熔溶剂(deep eutectic solvents,DES)是近年来发展的一类新型绿色溶剂,是由一定摩尔比的氢键受体和氢键供体在一定的温度下通过氢键作用形成的混合物,所制得的DES 具备其熔点比其任何单一组分的熔点更低的特性[1]。DES 与传统溶剂相比,具有价格低廉、可生物降解、无毒无害、合成方法简单等优点[2-4],目前已经成为绿色化学研究领域中一个重要的分支,被认为是传统易挥发有机溶剂和离子液体的良好替代品,并广泛应用在有机合成、电化学、功能材料、分离与萃取领域等各个领域[5-8]。目前已经合成出来的并已经应用在各个化学研究领域的DES,大多数都是亲水性的,在 2015 年之前,疏水性DES 未见任何报道,这极大地阻碍了DES 在水相中的应用,将DES 的应用范围从有机相扩展至水相显得尤为重要,疏水性低DES 正是在这样的大背景下出现的。2015 年,巴西里约热内卢联邦大学Bernardo 和葡萄牙新里斯本大学Catarina 等人首次以 DL-薄荷醇为氢键受体,4种天然的有机酸为氢键供体合成了疏水性DES。在随后的 2016、2017 和 2018 年又有不少关于疏水性DES 的文章发表,这些新合成的疏水性DES 在物质的萃取与分离过程中获得了充分的应用,如应用在萃取并测定在水中污染物、食品的人工合成色素、农药残留等方面[9-12]。
非甾体抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs)是一类不含有甾体结构的抗炎药,是全球使用最多的药物种类之一。大量NSAIDs最终会进入到水环境当中,并成为水环境中新型的重要污染物之一。因此,对于环境水中的NSAIDs的检测成为研究热点[13]。而对于痕量分析,样品前处理技术至关重要,分散液液微萃取(dispersive liquid-liquid microextraction,DLLME)是2006 年由Assadi 等提出的一种新型少溶剂的样品前处理技术,是一种极具应用潜力的样品前处理方法,但是在传统的DLLME中,常用的萃取剂为三氯甲烷、乙酸乙酯等毒性大、易挥发的有机溶剂,存在着操作不便和对环境污染较大的缺陷,不能满足绿色化学的需求。本研究采用安全、无毒的疏水性DES溶剂为萃取溶剂,应用DLLME方法对水溶液中的酮洛芬、布洛芬、洛索洛芬钠、萘普生、双氯芬酸(结构式见图1)5种非甾体抗炎药进行萃取研究。
1 仪器与试药
1.1 试验仪器 L2030A高效液相色谱仪(日本岛津公司);KH-3200B 型超声波清洗器(昆山禾创超声仪器有限公司);TGL-16G 高速离心机(上海安亭科学仪器厂); AR2140万分之一分析天平(梅特勒-托利多仪器上海有限公司)。
1.2 试剂与药品 甲基三辛基氯化铵(TAC)(含量≥90%,上海源叶生物有限公司);辛酸、癸酸、月桂酸、硬脂酸(国药集团化学试剂有限公司);酮洛芬(ketoprofen)对照品、布洛芬(ibuprofen)对照品、洛索洛芬钠(loxoprofen sodium)对照品、双氯芬酸钠(diclofenac sodium)对照品、萘普生(naproxen)对照品均供含量测定用,由中国食品药品检定研究院提供。
2 试验方法
2.1 色谱条件 色谱柱:Phenomenex C18(4.6 mm×250 mm,5 μm);流动相:乙腈-0.05 mol·L-1NaH2PO4(47∶53);流速:1.0 mL·min-1;进样量:10 μL;检测波长:264 nm,洛索洛芬钠为223 nm;柱温:30 ℃。在该色谱条件下,5种化合物的色谱图见图2。
2.2 疏水性DES 的制备 采用加热搅拌法制备疏水性DES,将TAC分别与4种不同的氢供体按照表1所示的比例混合,置于磁力搅拌器中,在60 ℃的温度下进行搅拌,直至形成均匀澄清透明的溶剂,即得。冷却后,DES溶剂在室温下保存。

表1 4种DES溶剂的组成和比例
2.3 对照品溶液的配制 分别精密称取酮洛芬、布洛芬、洛索洛芬钠、萘普生、双氯芬酸钠对照品11.4、34.5、33.2、28.9和24.6 mg置100 mL量瓶中,加甲醇适量溶解并稀释至刻度,即得浓度分别为0.114、0.345、0.332、0.289和0.246 mg·mL-1的对照品储备液。密封保存,放置于4 ℃的冰箱中备用。使用前需先放置至室温。
2.4 分散液液微萃取方法 精密量取10 mL添加有5种化合物对照品的水溶液,加入13.5%(W/V)NaCl,振摇使其溶解。随后加入乙腈650 μL,DES 300 μL,涡旋60 s,充分振荡后形成乳白色混浊溶液。将此溶液离心7 min(5 000 rpm,通过试验考察,离心时间越久,两相分层越明显,通过试验考察,当离心7 min时,两相分层明显,且吸取上层DES时操作较容易,因此,选择离心7 min。),在离心管上层形成DES液滴聚集相,用微量进样器吸取收集上层DES溶液(约200 μL),加乙腈至300 μL,0.45 μm 有机滤膜过滤后,HPLC法分析。
3 结果与讨论
3.1 DES-DLLME条件筛选
3.1.1 DES种类的筛选 萃取剂的选择在液相微萃取过程中是至关重要的。好的萃取剂往往用少量就能够在大量基质中有效地将待测物萃取出来,同步达到分离与富集的目的。而DES的组成会影响DES溶剂的性质,进而影响对化合物的萃取率,本研究以长碳链的季铵盐,甲基三辛基氯化铵为HBA,以4种不同碳链长度的脂肪酸为HBD制备DES溶剂,如表1 所示。试验结果表明,当以硬脂酸为HBD时,制备DES所需要时间比较久,且在室温下放置时会析出,因此,选择D-1~D-3为萃取溶剂,按“2.4”项下萃取条件考察其对5种NSAID的萃取率。5种NSAID的萃取回收率见图3A。萃取回收率的公式如下:
其中CD表示在DES层中化合物的浓度,而C0表示化合物在水溶液中的最初浓度。VD和V0表示DES层的体积和水溶液的体积。
从图3A可见,当以DES-2为萃取剂溶时,5种NSAID的萃取回收率均为最高,因而,选择DES-2(甲基三辛基氯化铵/癸酸)为最佳萃取溶剂,进行下一步试验条件考察。
3.1.2 HBA/HBD比例的考察 制备不同HBA/HBD比例为1∶2、1∶3、1∶4、1∶5 4种DES-2溶剂,并以其作为萃取溶剂,按“2.4”项下方法考察不同HBA/HBD比例对5种NSAID化合物的萃取率。结果见图3B。从图中可见,5种化合物的萃取率均随着HBA/HBD比例的增加而增加,并在1∶5时达到最大,因此,HBA/HBD的最佳比例选择为1∶5。
3.1.3 分散剂的选择 在DLLME萃取过程,分散溶剂的选择对于萃取效率至关重要,分散剂作为一种媒介作用,使得有机相成为小液滴,更加容易与水相混匀,增加它们之间的接触面积,有利于萃取效率的提高。本研究中,比较了两种分散剂,甲醇和乙腈对5种化合物的萃取率的影响,结果见图3C。试验结果表明,当以甲醇和乙腈作为分散溶剂时,5种化合物的萃取率并无明显差异。以乙腈作为分散溶剂时,提取率略高,因此,选择乙腈为分散溶剂。
3.1.4 响应面分析
3.1.4.1 响应面分析因素水平的选取 除上述3个因素外,萃取剂DES的用量、分散剂的用量以及盐的浓度对萃取率也有一定的影响。萃取剂用量多少直接影响分散液液微萃取方法的富集倍数,萃取剂用量在选择时既要满足一定的萃取率和富集倍数,还要有足够的体积以满足与水相分层。而分散剂用量也是影响萃取率的一个重要因素。分散剂用量较少时,萃取剂不能均匀地分散在水中,即不能形成良好的乳浊液体系,导致萃取率降低;而分散剂用量较大时,会导致目标物在水中的溶解度增大不易被萃取,也会导致萃取率降低。
为了进一步对DLLME的条件进行优化,在单因素考察试验的基础上,采用Box-Benhnken试验设计方案,以DES体积,分散剂的体积,NaCl的浓度为考察变量,分别以ABC表示,以5个化合物的提取率的平均值为响应值,进行3因素3水平的试验设计,试验因素与水平设计见表2,RSM分析方案试验结果、方差分析见表3~4。
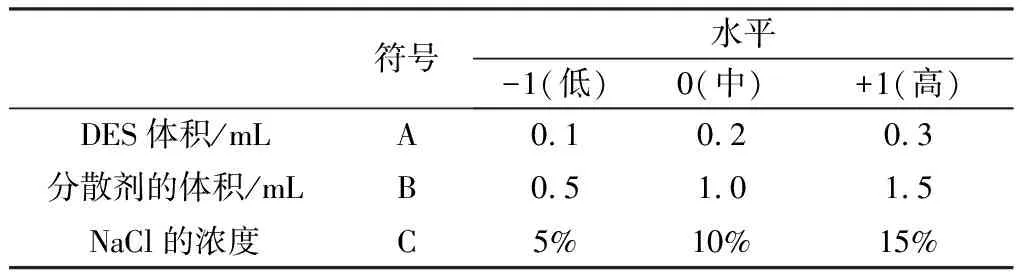
表2 响应面分析的试验因素与水平设计
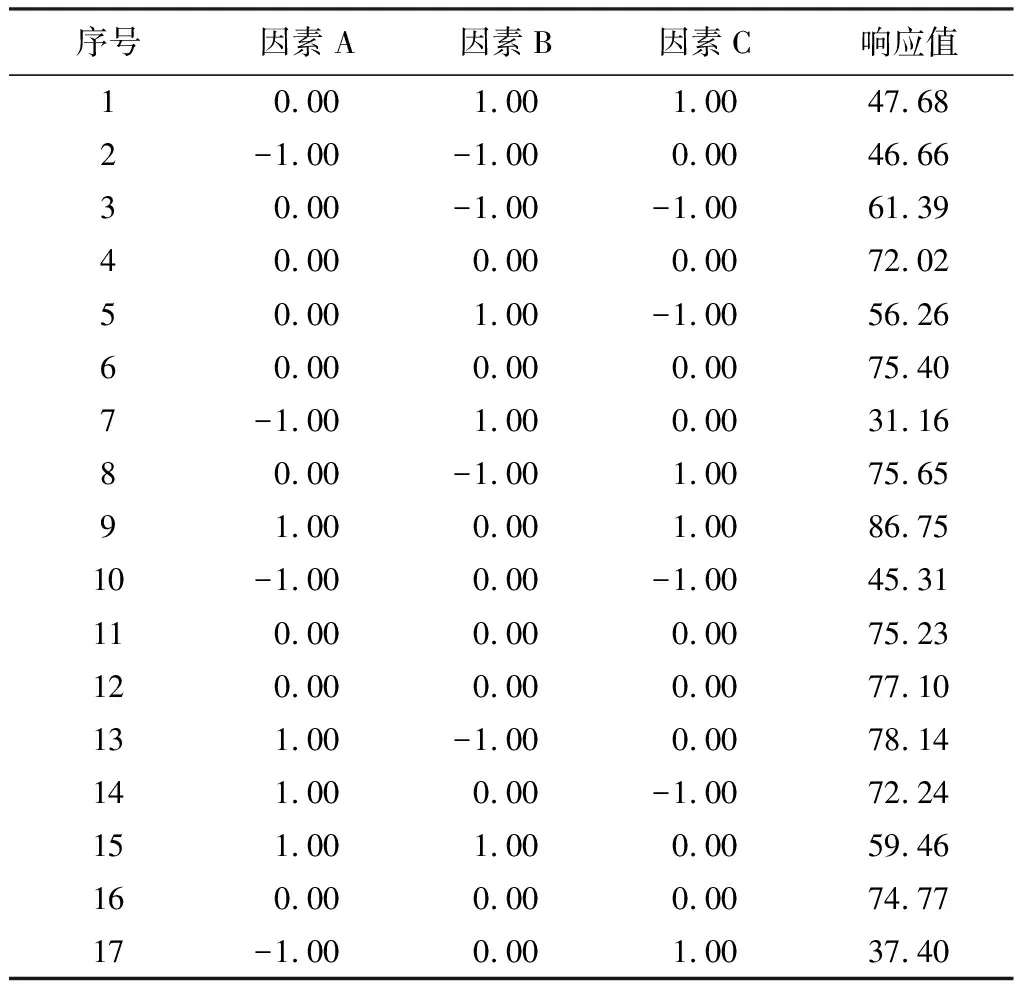
表3 响应面分析试验安排及试验结果
3.1.4.2 响应面分析方案及结果 从方差分析表中可见,模型F值为69.28,P<0.000 1表明总体上模型因素水平值显著,因此该试验设计是可靠的。回归模型中方差结果还表明,A、B、A2、B2均为显著项,即DES体积、分散剂体积对萃取率影响较为明显,而其他因素不明显。响应面图见图3。
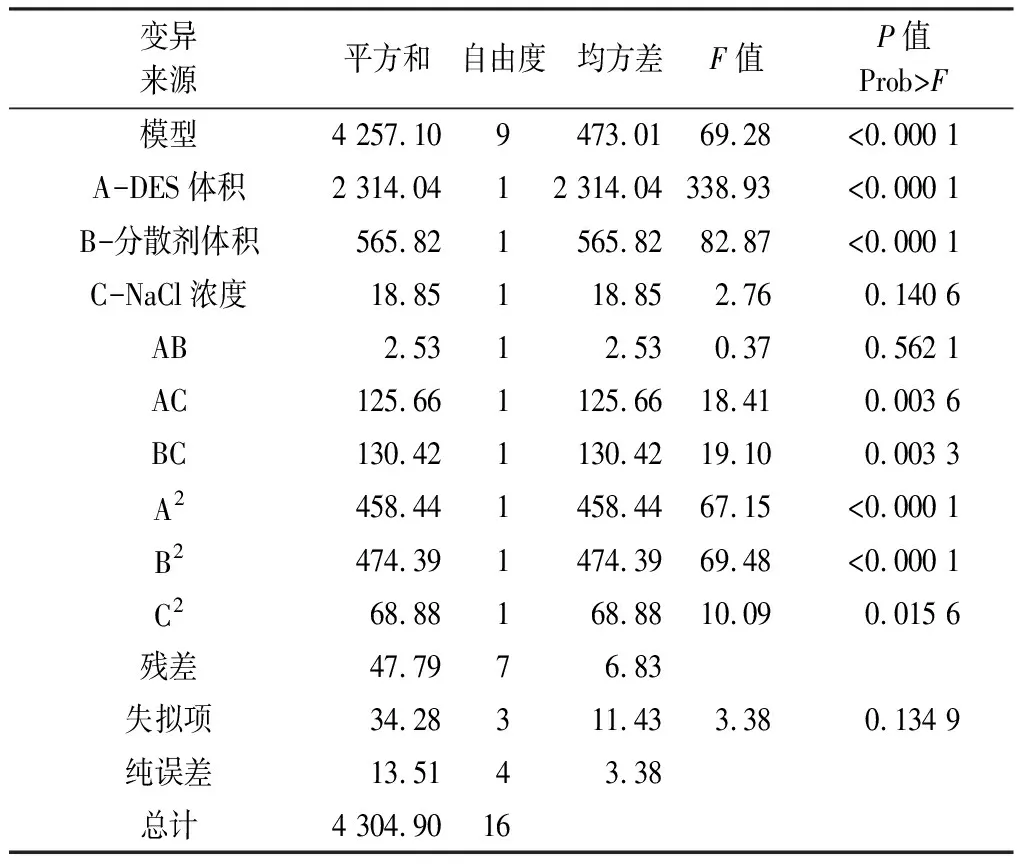
表4 方差分析结果
利用RSM软件各因素经回归拟合后,解得回归方程为:
Y=74.9+17.01X1-8.41X2+1.54X3-0.80X1X2+5.61X1X3-5.71X2X3-10.43X12-10.61X22-4.04X32
此外,经软件计算得到的R2为0.988 9,表明试验数据与每种模型的预测提取产率相当吻合。根据RSM的分析,得到提取优条件为:A:1.0; B:-0.70;C:0.73,即 DES的体积为300 μL,乙腈的体积为650 μL,氯化钠的浓度为13.5%,在此条件下,得到的理论最佳平均萃取率为87.45%。在此条件下,得到的理论最佳平均萃取率为87.45%。为检验RSM法的可靠性,采用上述最优提取条件进行DES-DLLME萃取试验,实际测得的酮洛芬、布洛芬、洛索洛芬钠、萘普生、双氯芬酸钠的萃取率为89.7%、80.3%、77.1%、92.6%和91.4%,5个化合物的平均萃取率为86.22%,与理论预测值比较接近。
综上所述,DLLME的最佳条件为以DES(甲基三辛基氯化铵/癸酸=1∶5)为萃取溶剂,以乙腈为分散剂,DES的体积为300 μL,乙腈的体积为650 μL,氯化钠的浓度为13.5%,在最佳条件下,酮洛芬、布洛芬、洛索洛芬钠、萘普生、双氯芬酸钠的萃取率为89.7%、80.3%、77.1%、92.6%和91.4%。
3.2 方法学验证
3.2.1 标准曲线 分别准确吸取5种对照品储备液0.01、0.02、0.05、0.2、0.5、1.0 mL置10 mL量瓶中,用流动相溶解并稀释至刻度,配制成一系列不同浓度的混合对照品溶液,0.45 μm 有机滤膜过滤,进入HPLC,进行分析。以色谱峰面积为纵坐标(Y),分析物浓度C(μg·mL-1)为横坐标(X),计算各对照品回归方程,结果见表5。如表所示,各个对照品在相对应的线性范围内线性关系良好。
3.2.2 仪器精密度试验 取同一对照品溶液,连续进样6次,计算各峰面积的RSD,结果表明RSD为0.92%,说明仪器精密度良好。
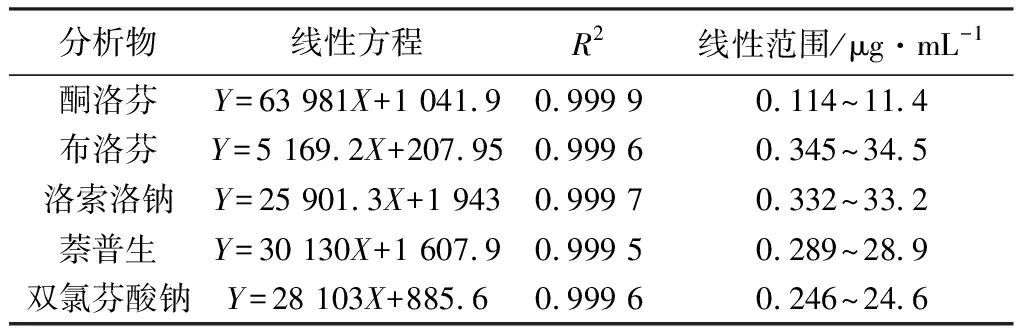
表5 5个化合物的线性关系考察结果
3.2.3 重复性试验 分别配置10、0.5 μg·mL-1两种浓度的加标样品,分别置于15 mL尖底离心管,按“分散液液微萃取方法”项下方法操作,进行日内精密度和日间精密度考察。日内精密度的测定是在一天之内对样品进行 6 次重复分析;日间精密度是连续6 d分析样品,每天分析 1 次。结果见表6,日内精密度和日间精密度的范围分别为0.9%~2.9%和 0.9%~3.2%,表明该方法具有较好的重现性。
3.2.4 回收率试验 按照“2.4”项下试验步骤,测定高、低两种不同浓度时分析物的回收率,各个分析物在高、低两个浓度下其平均回收率及RSD(n=3)如表6所示。结果表明本方法准确度度较好。
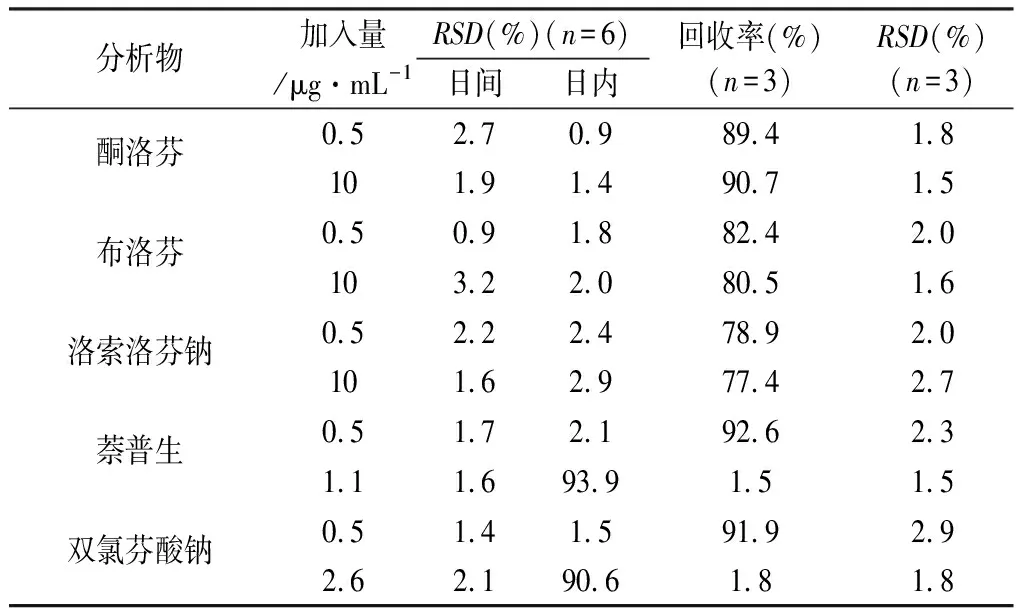
表6 重复性与回收率试验结果
4 结论
本研究建立了疏水性DES-DLLME萃取水溶液中5种非甾体抗炎药物的方法,该方法的最佳条件为以DES(甲基三辛基氯化铵/癸酸=1∶5)为萃取溶剂,以乙腈为分散剂,DES的体积为300 μL,乙腈的体积为650 μL,氯化钠的浓度为13.5%,在最佳条件下,酮洛芬、布洛芬、洛索洛芬钠、萘普生、双氯芬酸钠的萃取率为89.7%、80.3%、77.1%、92.6%和91.4%。
试验结果显示,所建立的方法具有简单、快速、准确、灵敏的优点,可选择性的对水溶液中的5种非甾体抗炎药物进行萃取纯化和富集。本方法首次采用合成简单、无毒、可生物降解的疏水性DES溶剂代替传统有机溶剂对水中的非甾体抗炎药物进行提取,克服了在传统有机溶剂由于毒性较大、挥发性强而带来的操作不便、对环境污染等缺点。
