溶液吸附法测定活性炭比表面积的实验改进
2020-07-01侯向阳侯秀芳柴红梅王智香高楼军
侯向阳,侯秀芳,柴红梅,王智香,高楼军
(延安大学 化学与化工学院,陕西 延安 716000)
物理化学实验教学,既可培养学生的实验技能、实验素养,又可促进学生对物理化学基本概念和原理的深入理解,对化学、化工相关专业的人才培养具有不可替代的作用。针对“物理化学实验教学与其相关理论内容教学相脱节”、“物理化学实验教学内容过于单薄,与学生的实践性教学、实验创新教育等环节衔接较少”及“物理化学实验教学内容滞后物理化学学科领域研究”等问题;结合溶液吸附法测定活性炭比表面积实验,对其教学内容、方法进行了探讨[1,2]。以达到实验教学目的,实现实验课程教学改革和课程建设的目标。溶液吸附法测定活性炭比表面积是化学、化工相关专业必开的一个经典实验,对学生深入理解界面与胶体相关概念、原理有很好的帮助作用[3]。
1 实验教学中有待探究的问题
溶液吸附法测定活性炭比表面积实验教学过程中,发现学生对以下问题认识模糊或错误:
(1)教材对亚甲基蓝是这样描述“亚甲基蓝是具有矩形结构的阳离子型表面活性剂,阳离子大小是(17.0×7.6×3.25)×10-30m3,被活性炭吸附时,亚甲基蓝有三种不同吸附取向和相应投影面积:(a)被平面吸附时,投影面积为135×10-20m2,(b)被侧面吸附时,投影面积为75×10-20m2,(c)被端基吸附时,投影面积为39×10-20m2,活性炭对亚甲基蓝采用端基取向吸附,δA=39×10-20m2”[4,5]。实验发现学生对亚甲基蓝的描述理解模糊,即不能正确回答“为什么会存在三种不同方向上的取向、三种吸附取向下亚甲基蓝的投影面积是如何计算的及为什么亚甲基蓝最终被活性炭采取端基取向吸附”的问题。
(2)实验要求采用非石墨型颗粒活性炭,但对“非石墨型活性炭有何本质特点及实验为什么选用非石墨型活性炭而不用其他类型活性炭”等问题未做说明[6,7]。
(3)教材要求当活性炭质量为0.1 g左右时,亚甲基蓝溶液的质量百分比浓度为0.2%[8,9]。学生对此产生的问题“(a)为什么活性炭质量为0.1 g左右时,亚甲基蓝溶液浓度必须为0.2%;(b)活性炭质量增大后,亚甲基蓝溶液浓度应怎样合理变化及亚甲基蓝溶液浓度改变对吸光值测定时有无影响”没有深入思考,甚至有部分学生就没有考虑到该问题的存在。若能帮助或引导学生彻底解决该实验内容中的这些难点问题,无疑对实验结果的保证、学生实验素养的形成、分析问题、解决问题能力的提升有很好的帮助。在该实验教学中,通过量化计算、学科前沿知识的引入,加强对实验内容中难点问题的深入探究以及增加实验操作、丰富实验内容两方面的实验改进,进行溶液吸附法测定活性炭比表面积实验教学,以提高该实验教学效果并对相关实验课程教学起到师范作用。
2 实验教学中亟需改进的内容
2.1 加强实验内容中难点问题的深入探究,进行教学改革
对实验涉及的难点理论问题,往往是学生实验过程中易忽略的问题。但若能彻底理解相关重难点问题,对激发学生实验、学习兴趣和培养学生的深度思维及探究能力非常重要。
(1)关于亚甲基蓝阳离子大小及被活性炭吸附时取向的问题,从理论计算角度进行了分析,结果如图1。采用Gaussian软件在b3lyp/6-311++g**水平优化亚甲基蓝阳离子的结构,使用Multiwfn软件计算分子的长、宽、高,用VMD软件显示图形,计算出平面、侧面、端基面三个不同方向吸附时投影面积的大小;亚甲基蓝阳离子的大小是(16.62×7.88×4.18)×10-30m3;其三个吸附面面积大小分别是:16.62×7.88=131.0×10-20m2;16.62×4.18=69.5×10-20m2;7.88×4.18=32.9×10-20m2。根据文献报道,无定型炭的结构是包括12~25个碳原子(3~7个苯环),按照“近程有序,远程无序”的原则随机连接而成[10]。实验以15个碳原子(4个苯环)为活性炭基本单元,组合成无定型多孔活性碳从三个不同方向对亚甲基蓝吸附进行模拟理论计算,吸附热结果如图1(b)所示。计算结果表明:端基吸附、侧面吸附(N端)、侧面吸附(S端)三个不同方向吸附热的大小分别是-16.4、-14.1、-12.1 kJ·mol-1。虽然不同方向的吸附热值大小差别较小,但这也是以15个碳原子(4个苯环)为无定型碳结构单元计算的吸附结果,无定型碳实际包含的碳原子或苯环数目非常多,随苯环数目增加三个方向吸附热及不同吸附热之间的差值会逐步增大。根据不同方向吸附热数值大小,足以说明无定型碳吸附亚甲基蓝采取端基吸附模式;同时计算结果也发现活性炭对亚甲基蓝的平面吸附模式不可能存在,图1(c)解释了原因。计算之前,将活性炭对亚甲基蓝的吸附模式假定为平面吸附,但理论计算过程、结果发现活性炭对亚甲基蓝的吸附模式在逐步变化,最终成为侧面吸附(N端或S端),且其吸附热数值也和直接假定为侧面吸附模式(N端和S端)的计算结果一致。N端侧面吸附热比S端侧面吸附热的数值大,说明在两种侧面吸附模式中N端侧面吸附几率较大一些。通过理论计算就很清楚的解释了这一问题,也使学生对理论计算化学有初步了解,意识到实验课程和其它学科之间的联系。

图1(a)亚甲基蓝分子大小示意图;(b)活性炭吸附吸附亚甲基蓝示意图及吸附热数值;(c)活性炭平面吸附亚甲基蓝变化过程示意图
(2)关于活性炭描述的问题,结合学科前沿知识,就炭材料概念及相关知识给予介绍,使学生对此有清晰了解。炭材料分为石墨、高比表面积石墨、活性炭等三类,很少见有非石墨型活性炭、石墨型活性炭的提法,但有石墨化提法。活性炭本质是SP2炭,是长程无序,多孔结构,习惯上称为无定型的炭,而石墨是晶体材料。所以有教材要求采用的非石墨型颗粒活性炭应该是长程无序、多孔结构的无定型炭,其堆积密度低,具有大的比表面积,吸附的容量大,可吸附多种类化合物,吸附作用力大,可发生化学吸附,发生反应的可能性高。这样,学生不仅对活性炭有正确的认识,也理解了为什么要选用这样的活性碳材料进行吸附亚甲基蓝的实验。最终意识到物理化学实验不单纯与物理化学方面有联系,也与材料化学等学科密切关联。
2.2 增加实验操作、丰富实验内容,进行教学改进
在实验中增加活性炭制取步骤,有关活性炭的制取方法已有大量的文献资料报告,且操作简单,学生在查阅文献资料,和老师、学生讨论的基础上可独立完成;该实验内容的增加,即丰富实验的内容,也平添学生实验兴趣,培养学生查阅文献、分析问题和解决实际问题的能力。并将亚甲基蓝溶液浓度涉及的问题,通过实验操作方法的改变、自身实验来解决。最终,学生形成活性炭制备方案,利用自制活性炭及优化亚甲基蓝浓度基础上平行进行6次实验,结果如表1、2、3和图2。
活性炭制备方法:将芦苇秸秆洗净,干燥、破碎(1~2 cm)后用配置好的ZnCl2溶液(45%)浸渍24 h,浸渍比为2∶1、温度为60 ℃,将浸渍好的芦苇秸秆置于干燥皿中,在90 ℃条件下干燥24 h后置于坩埚中,盖好盖子(保证碳化在缺氧或贫氧的前提下进行),将坩埚置于马弗炉中,关好炉门,控制器温度为600 ℃,1 h后将加热控制器关闭,待马弗炉内温度降至安全温度以下后,再将样品取出,置于烧杯中,加入一定量的1 mol·L-1的HCl,煮沸20 min后取下,待其冷却后,用蒸馏水洗涤,直至将多余的ZnCl2杂质完全除去后干燥、研磨、筛选得到100目成品活性炭。
表1是亚甲基蓝标准溶液及其原始溶液浓度的测定结果,根据测定数据得到亚甲基蓝溶液的标准工作曲线如图2(a)。按照表2配制不同浓度的亚甲基蓝溶液,分别准确加入活性炭约0.1 g左右,振荡平衡后,测定其吸光度。表3是实验中活性炭质量、活性炭吸附亚甲基蓝溶液平衡后吸光度数值,以及计算得到的亚甲基蓝被吸附前浓度、吸附后浓度、活性炭吸附量和比表面积的结果值。图2(b)是活性炭吸附亚甲基蓝的吸附量(Γ)与浓度(c)的关系曲线图,由图可知,随亚甲基蓝溶液浓度增大,Γ-c关系由曲线变成直线出现平台,充分说明活性炭对亚甲基蓝的吸附在亚甲基蓝溶液浓度较小时是不饱和吸附,随亚甲基蓝溶液浓度合理增大,吸附趋于饱和并最终刚形成饱和的单分子层吸附。图2(c)是c/Γ-c关系曲线,由该曲线的斜率值计算出活性炭吸附亚甲基蓝为饱和单分子层时的最大吸附量值。

表1 亚甲基蓝标准溶液及其原始溶液浓度测定结果

表2 活性炭吸附亚甲基蓝平衡溶液的配制

表3 平衡溶液吸光度测定及相关浓度和比表面积计算结果
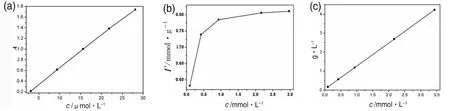
图2 (a)亚甲基蓝溶液浓度与吸光度标准工作曲线;(b)Г-c吸附等温线;(c)c/Γ-c关系曲线
3 结论
论文从引入量化计算、学科前沿知识加强对实验内容、方法设计难点问题的深入探究及增加实验操作、丰富实验内容,进行实验教学改进,以提高实验课程教学质量。通过对实验涉及重难点问题的详细探讨,使学生对物理化学学科前沿有一定了解,可开阔学生学习视野,增加实验兴趣;增加必要实验操作、实验内容更可培养学生分析问题、解决实际问题的能力。论文主要目的是提高溶液吸附法测定活性炭比表面积实验的教学质量,并对相关实验教学起到师范效应。
