肝多发上皮样血管内皮瘤1例并文献复习
2020-06-20程蒙蒙佘明金
程蒙蒙,荣 辉,佘明金*
(武警安徽省总队医院肿瘤科,安徽 合肥 230041)
肝脏上皮样血管内皮瘤(hepatic epithelioid hemangioendothehoma,HEHE)是罕见的肝脏血管源性肿瘤,由于其临床表现无特异性及医疗工作者对影像学表现认识尚不充分,组织学上易与其他肿瘤混淆,临床误诊率极高。本文报道1例反复影像学检查未能确诊,经穿刺活检及手术诊断HEHE,并结合相关文献,分析总结该病的临床表现、病理、影像学表现及目前的治疗,以提高对本病的认识。
1 病例介绍
患者男性,37岁,系“发现肝占位伴右上腹隐痛6年余”于2018年6月16日入院。查体:右上腹部压痛(+),余(-)。期间肝功能示谷草转氨酶反复轻度升高,保肝后降至正常。既往体健,无家族史。2011年9月腹部B超:肝囊肿。2014年6月B超:考虑血管瘤。2016.5 B超:肝囊肿,肝右叶偏低回声团。2016年6月2日上腹部CT:肝内多发强化密度影,考虑不典型血管瘤(图1)。2016年6月7日上腹部MRI:肝脏多发异常信号,多发血管瘤可能(图2)。2016年6月27日南京鼓楼医院肝脏肿瘤多学科团队会诊意见:考虑肝多发肿瘤(恶性转移性肿瘤可能性大)。CEA、AFP、CA199、CA125正常。2016年6月29日胃镜、肠镜:胃炎、直肠炎。2016年7月1日PET/CT:肝内多发低密度病变,肝左叶病灶FDG代谢增高,考虑恶性病变可能(图3)。2016年7月27日肝占位穿刺活检,免疫组化标记:CK+,Vim+,CD31+(血管),CD34+(血管),Ki67+3%,倾向上皮样血管内皮细胞瘤。2016年7月29日行“肝肿瘤切除术”,术中肝表面可触及多个大小不等的肿瘤,较大肿瘤位于左肝外叶、左肝内叶,质硬,符合上皮样血管内皮瘤(左肝内叶:2×2×1.5 cm;左肝外叶:2.8×2.5×1.3 cm)。2016年8月5日术后病理:病灶变性纤维组织内见短索状、小巢状瘤细胞,部分瘤细胞可见管腔或空泡形成,内含单个红细胞,周围肝细胞结节状增生,免疫组化(2016-3221):
CD34+,CD31+,CK+,Vim+,AFP-,GPC-3-,Herpar-1-,Ki-67+10%(图4)。该患者确诊HEHE,予“沙利度胺100mg QD”治疗,定期随访,目前病情稳定。
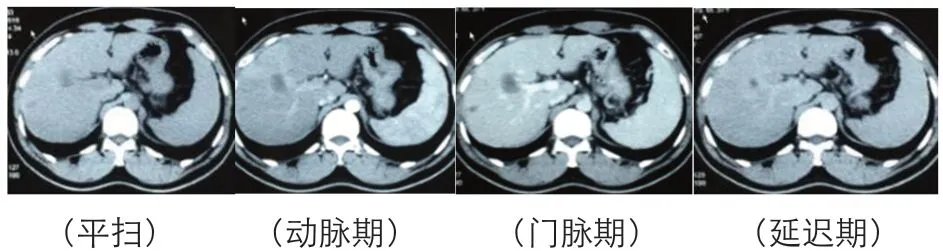
(图12016年6月2日上腹部CT平扫+增强)
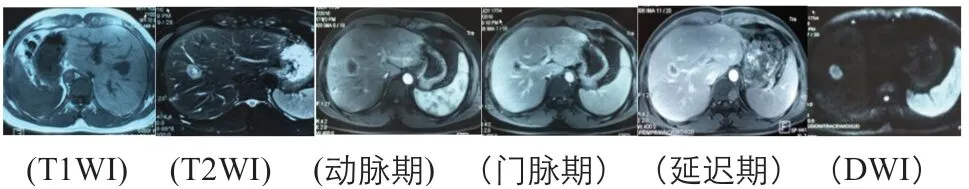
(图22016年6月7日上腹部MR平扫+增强)
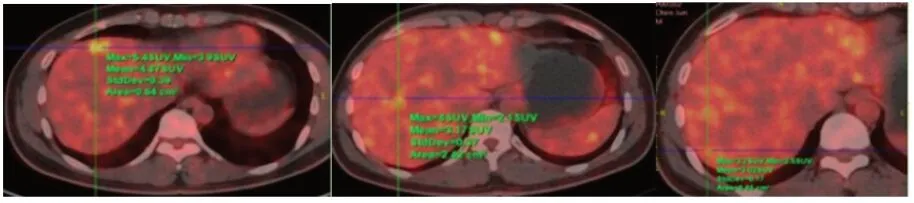
(图32016年7月1日PET/CT)
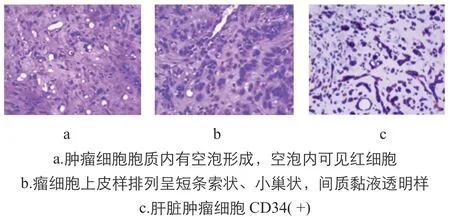
(图4 2016.8.5术后病理)
2 讨 论
HEHE发病率低于0.1/10万[1],女性易发病,30~40岁多见。根本病因尚不明确,可能与口服避孕药、氯乙烯、石棉、二氧化钍、造影剂、肝损伤、病毒性肝炎、原发性胆汁性肝硬化及饮酒有关,该病不受慢性肝病影响。
临床表现 无特异性,常见右上腹痛、肝肿大、体重减轻,可见体弱、厌食、上腹部肿块、腹水、恶心呕吐、黄疸、疲劳等。常为多中心病灶,具有侵袭性,部分患者存在肝外受累,最常侵犯肺、淋巴结、腹膜、骨、脾、横膈。
实验室检查:常出现肝功能异常,如碱性磷酸酶、谷草转氨酶、γ-谷氨酰转肽酶和胆红素指标升高等,肿瘤指标多正常,血小板分布宽度明显降低可能有助于诊断[2]。
影像学表现:目前分为三种类型:结节型、多灶型与弥漫型。多数医师对HEHE认识不足,易误诊。B超常规超声最常见为单发或多发边界清楚或模糊的低回声病变,少数为高回声,形态较规则,可见包膜回缩和钙化[3],造影常表现为动脉期不同程度增强,门脉期及延迟期呈低回声改变,部分病灶内缘呈短毛刺样增强及“血管征”[4]。CT“靶征”是其特征性表现[5],增强后病灶周边环状强化,门脉期及延迟期呈向心性强化,中心始终呈低密度,形似靶状而得名。“棒棒糖征”是另一特征性表现[6],起于肝静脉或门静脉,止于病灶,边缘强化而中心不强化的病灶中实体代表“糖果”,肝静脉或门静脉行向病灶逐渐变细并终止于病灶边缘代表 “棒子”,可能为HEHE在门静脉和肝静脉分支内浸润,静脉平稳终止在边缘或病灶边缘内[6]。肝包膜下病灶牵拉肝包膜形成“包膜回缩征",可能是由肿瘤中心供血不足出现缺血坏死致肿瘤牵拉周围组织[7],部分出现肿瘤内钙化。MRI T1WI图像常为低信号,中心为更低信号,部分可见中心低信号的同心环状表现,周围高信号,边缘低信号,即“黑靶征”。T2WI图像通常为高信号,部分为双层或三层靶征,中心高信号,周围低信号,边缘高信号,即“白靶征”。增强后多表现为外周强化,并呈向心性填充[8],也可出现“黑靶征” 或“白靶征”。DWI常显示病灶周围弥散限制边缘和中心的可变信号[9]。多数肿瘤中心信号从增强开始显示并缓慢增强,可能是HEHE的新诊断标志[10]。PET/CT FDG-PET/CT可用于HEHE诊断和分期、监测复发及转移[11]。恶性HEHE的FDG常较温和,约67%病灶FDG摄取增高,SUV(max)3.6±1.1[12]。能够评估血管生成的新型放射性示踪剂能及时准确评估病情[13]。
组织病理学及免疫组化:HEHE确诊有赖于组织病理学通过免疫组化证实内皮分化。HEHE具有独特的组织学特征,肿瘤细胞嵌入丰富的细胞外基质中,单个肿瘤细胞可出现上皮样或树突状细胞,且通常在单个细胞内显示小的内腔,呈印戒环外观。肿瘤边缘通常呈冲击性生长模式,肿瘤细胞常沿中央和门静脉生长。上皮样和树突状细胞的鉴定内皮细胞标记物(FVIIIRag、CD34和CD31),粘蛋白,胆汁,CEA或AFP的阴性染色和特征性超微结构特征较敏感,CAMTA1高度敏感[14],窦内扩散可能是一诊断特征[15]。
鉴别诊断:多数患者易误诊,最常误诊为胆管癌、脓肿、肝细胞癌、血管肉瘤和转移癌等,影像学关键的鉴别特征是结节的周围位置、包膜回缩以及多发性病灶合并的趋势[6],病理学上鉴别的重要特征包括浸润性生长模式、特征性的血管浸润以及上皮分化标志物的延迟染色。
治疗:由于该病的异质性及罕见性,HEHE的治疗时机及方案的选择目前无定论。手术切除或原位肝移植是主要治疗方法,由于肿瘤多中心性或解剖特征的复杂性,肿瘤切除多数情况下是不可能的。通常肝移植是最常见的治疗方式,但复发风险较高,不适合肝移植的患者可行TACE治疗。放疗[16]、化疗[17]重要性难以评估。靶向药物[17]如沙利度胺、来那度胺、贝伐珠单抗、索拉菲尼、舒尼替尼、阿帕替尼、mTOR抑制剂西罗莫司等报道有效,但仍需更大规模的研究来证明靶向药物的有效性。经手术、靶向、化疗后进展的患者,Ipilimumab+nivolumab治疗5个月达到部分缓解,8个月后持续缓解且无临床症状[13],免疫调节剂沙利度胺、来那度胺及干扰素α-2b也见成功报道[17]。目前免疫治疗报道很少,需临床进一步验证。尽管多种治疗手段在一定程度上有效,但无可靠证据表明综合治疗对生存或无复发有积极作用[18]。另外,HEHE多呈惰性病程,提示确诊后即刻治疗可能并非最佳策略。
临床预后:HEHE罕见,临床表现及病程高度可变,形态学分级及临床分期与预后的相关性未知。多为惰性病程,部分患者可以长期带瘤生存甚至病变自发消退,但仍具侵袭性。
该患者自2011年反复出现右上腹痛,临床症状无特异性,肝功能反复轻度异常,肿瘤指标正常,影像学资料无明确定论,CT平扫呈低密度,MRI T1WI呈低信号,T2WI呈“白靶征”,增强后均出现向心性强化及“棒棒糖征”,PET/CT FDG代谢轻度增高,SUV(max)为5.4,MDT意见为恶性肿瘤,自发病5年后经病理才证实为HEHE,术后给予免疫调节治疗,目前无复发或转移,该患者遵循惰性临床过程。
3 小 结
HEHE是一种罕见的血管源性肿瘤,具有高度异质性。单一手段易误诊,确诊需组织病理学结合免疫组化。治疗手段多样,但缺乏大规模的临床数据,无法系统评估治疗方案的有效性,亦无法准确筛选观察等待可临床获益的人群。作为临床医生,应综合评估患者疾病行为,制定合理的治疗方案,使患者临床获益最大化。
