自催化生长MnCr2O4纳米线及其对ORR/OER的抑制效应*
2020-06-19曹喻霖
曹喻霖
自催化生长MnCr2O4纳米线及其对ORR/OER的抑制效应*
曹喻霖
(深圳职业技术学院 工业训练中心物理教研室,广东 深圳 518055)
还原性气氛下在商品化导电不锈钢网筛的表面上合成了具有尖晶石单晶结构的MnCr2O4纳米线.在Ar/H2混合气体中,1100~1200 ℃条件下,对这些不锈钢网筛衬底进行热退火.电子显微镜研究表明,通过控制温度和生长时间,这些纳米线的直径在50~100 nm范围内,长度为1~10 μm.文章提出一种可能的自催化机制来解释这些MnCr2O4纳米线的生长,并研究了这些纳米线负载在不锈钢网筛上对非水锂空气电池的氧还原(ORR)和氧析出(OER)反应的影响,发现其对ORR/OER反应具有抑制作用.该抑制作用与不同热退火温度导致的不同表面积相关.研究结果有助于帮助了解作为锂空气电池的空气电极导电衬底上的表面纳米结构与其电化学性能之间的关系.
MnCr2O4纳米线;热退火;自催化成长;锂空气电池;氧还原/氧析出反应
锂空气电池(Li-air batteries,简称LABs)因其理论比能量高以及对环境友好的可再生能源的巨大需求引起人们的广泛关注[1-3].1996年,Abraham和他的同事展示了第一个锂空气电池(LABs)[4].这种非质子电池包括一个锂金属阳极,一个传导锂离子的有机电解质和乙炔黑碳阴极(也称为空气电极).通常认为,在放电时,锂离子通过氧还原反应(ORR)在空气电极表面上与O2反应生成Li2O2作为最终放电产物:2Li++ 2e-+ O2→ Li2O2,然后通过氧析出反应(OER):Li2O2→ 2Li++ 2e-+ O2,使过氧化锂分解,释放出锂离子和O2.与锂离子电池相比,锂空气电池的结构相对简单,关键部件是阴极,即空气电极.对于锂空气电池组件,通常将正极材料精细地粘贴到导电集电极上,例如不锈钢网筛,导电碳纸等.ORR和OER均发生在空气电极的表面,因此锂空气电池的电化学性能在很大程度上取决于空气电极的材料和结构[5].不同的材料,例如多孔碳颗粒[6],Mn3O4/介孔碳[7],碳纳米管/纳米纤维[8,9],石墨烯[10,11],MnO纳米结构[12-15],多孔Au[16],TiC纳米颗粒[17]等,已经被尝试用作锂空气电池的电极.
一维(1D)纳米结构材料由于其独特的物理和化学特性及其在场效应晶体管(FET)、光电探测器、锂电池等领域中的应用,近年来受到了广泛关注[18-21].不同的纳米线(NWs)直接生长在导电基材上,包括CoxOyNWs[22,23],Si纳米线[24],Ge纳米线[25]等,已显示出在锂离子电池中的潜在应用.尽管已经制备了一些纳米线将其涂覆在集电极上,但是在集电极上直接生长纳米线将简化锂空气电池的制造过程,易于研究其电化学性能.
作为尖晶石(AB2O4)家族的重要成员之一,MnCr2O4具有典型的空间群Fd3m尖晶石结构,而Mn2+和Cr3+分别占据晶格的四面体和八面体位置[26-28],已有报道不同的MnCr2O4纳米结构,例如纳米颗粒和纳米线等[29-31].然而,人们对一维MnCr2O4纳米结构和锂空气电池的电化学性能之间关系的研究较少.本研究在还原性气氛下,在不锈钢网筛上负载大规模单晶MnCr2O4纳米线的气相合成,并探讨了它们对锂空气电池ORR/OER电化学性能的影响.
1 实验部分
1.1 纳米结构制备
在置于三温区管式炉中的石英管中合成MnCr2O4纳米结构.圆形不锈钢(Stainless steel,SS)316L(Fe0.7Cr0.16Ni0.1)网筛同时充当MnCr2O4纳米线生长的前躯体和衬底.依次用乙醇、丙酮和去离子水清洗SS网筛衬底.将SS网筛装入放在陶瓷管中央的Al2O3瓷舟中.然后将陶瓷管插入到管式炉中,并将SS网筛放置在炉的中心.将石英管抽真空至约6×10-2mbar的压力后,与体积分数5%氢气(H2)预混合的高纯氩气(Ar)以50 sccm(标准立方厘米/分钟)的速率进气.反应条件见表1.将炉温以10 ℃/min的速率升高至1100~1200℃,并在该温度下保持约1~5 h,石英管内部的压力保持在100 mbar.使该系统在相同的气流和压力下自然冷却至室温.然后在管的中心将经过热退火的SS网筛收集.对比实验,在相同的实验条件,但不是在Ar/H2混合气氛下,而是在纯Ar气氛下进行SS网筛的热退火.
1.2 结构表征
用附有能量色散X射线光谱仪(EDS)的扫描电子显微镜(SEM,Philips XL 30 FEG)研究热退火后的样品.另外,用X射线衍射仪(XRD,Siemens D-500)和透射电子显微镜(TEM,CM200 FEG,在200 kV下操作)表征所制备的样品.拉曼测量在Renishaw 2000光谱仪中进行.使用单色AlKα源(1486.6 eV)进行X射线光发射光谱(XPS)测量,以确定纳米结构的组成.对于XPS测量,分析仪的能量分辨率为0.36 eV.使用Micromeritics ASAP2020仪器在-196 ℃下获得氮吸附-脱附等温线.在测量之前,将样品在200℃的真空下脱气2 h.使用Brunauer-Emmet-Teller(BET)公式,利用在0.05/0.15之间的P/P0区域中的数据,计算比表面积[32].
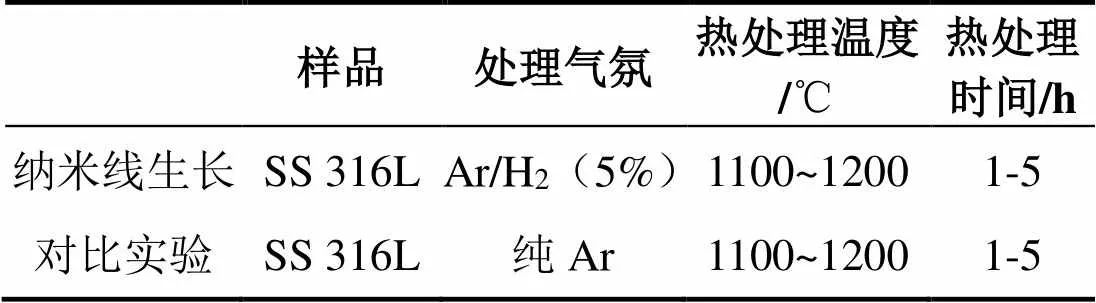
表1 MnCr2O4纳米线生长条件及对比实验
1.3 锂空气电池组装及电化学测试
使用前,将经过热退火处理的SS网筛在真空烘箱中于70 ℃干燥至少12h.将干燥后的SS网筛直接转移到充满Ar的手套箱中,SS网筛的处理完全在手套箱中进行.电池组装在充满Ar的手套箱中进行.锂空气电池的组装过程见文献[33].锂空气测试电池由锂金属阳极(直径:16 mm)、玻璃纤维膜隔板和SS网筛(直径:16 mm,质量:32 mg)组成.用300 μL电解质(溶解在DMSO中的0.1 M LiClO4)润湿隔板.在测试之前,将组装好的电池用纯O2吹扫30 s.使用VMP3(法国Bio-Logic)对锂空气电池进行恒电流测试.通过放电/充电容量的测量比较ORR/OER性能.
2 结果与讨论
2.1 纳米结构特性
当所有的316 L不锈钢(SS)网筛在Ar/H2气氛下进行热退火后,用肉眼观察时,其表面从原来的灰色变为深绿色.如图1所示,原始纯SS的表面非常光滑.而在热退后,这些SS衬底的表面上形成线状纳米结构.EDS表示存在Fe,Cr,Ni,Mn,O和C元素.Fe,Cr和Ni元素是316L不锈钢的主要成分.其他可能来自SS 316L中的次要元素.SS网孔的表面完全被密集的均匀纳米线阵列覆盖.所有纳米线主要垂直于该SS网的表面生长.这些纳米线的直径在50~100 nm范围内,长度可达5 μm.图1(e)所示的EDS光谱显示出Cr,Mn,Fe和O元素的存在.图1(f)中XRD图谱检查了纳米线的晶体结构.热退火后的XRD峰与MnCr2O4尖晶石的面心立方(fcc)结构的峰一致(JCPDS 75–1614).基于SEM,EDS和XRD,可以将这些纳米线归结为尖晶石MnCr2O4纳米线.
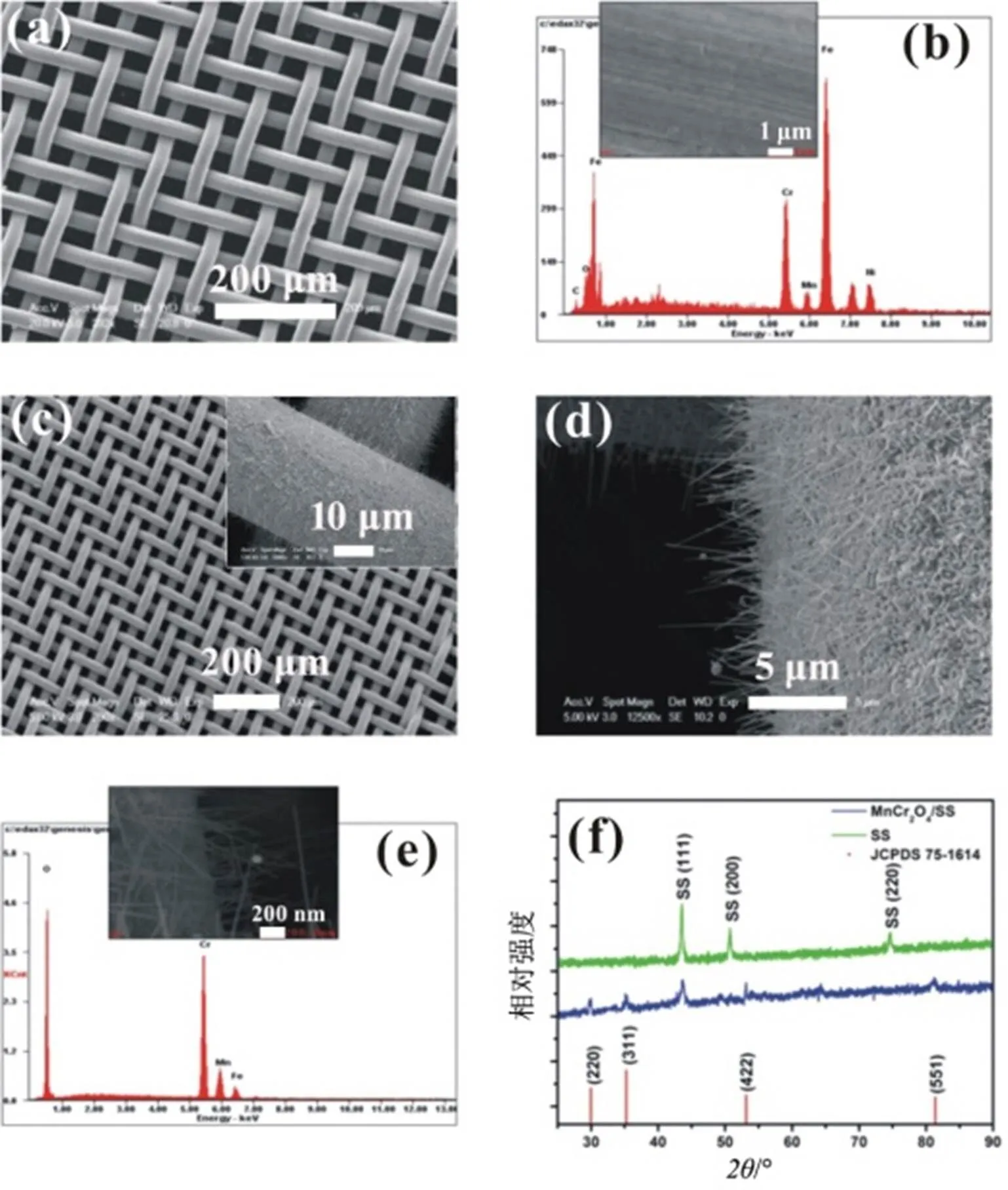
图1 (a)、(b)纯不锈钢(SS)的低倍SEM图像和EDS光谱;(c)、(d)在Ar/H2中的热退火不锈钢的低倍SEM和高倍SEM图像;(e)、(f)在Ar/H2中热退火不锈钢的EDS光谱和热退火前后纯不锈钢的XRD光谱.(b)、(d)、(e)中的插图都是相应的SEM图像
将SS网筛放在1150 ℃的Ar/H2中加热不同的时间,进一步研究退火时间和退火气氛对尖晶石MnCr2O4纳米线生长的影响.如图2所示,当退火40 min时,这些MnCr2O4纳米线的直径约为50~60 nm,长度约为3~5 μm.在这些MnCr2O4纳米线的尖端,可以清楚地观察到球形纳米结构,这是“气—液—固”(Vapor-Liquid-Solid,VLS)生长的纳米线的典型形态.当退火2.5 h时,观察到直径约为60 nm,长度约为5 μm的MnCr2O4纳米线,并且这些纳米线的生长方向在SS网筛的垂直方向上是一致的.当退火达到5 h时,形成了非常短的MnCr2O4纳米棒,尺寸约为80 nm,长度约为750 nm,并且SS网孔表面被低密度的MnCr2O4纳米棒覆盖.退火气氛在MnCr2O4纳米线的生长中也起着重要作用.在Ar中进行热退火后,SS的表面仍然光滑.没有观察到任何明显的纳米结构.因此,在相同的实验参数下,退火气氛从Ar变为Ar/H2,导致在SS网孔表面形成尖晶石MnCr2O4纳米线.
我们还研究了退火温度对MnCr2O4纳米线生长的影响.由图3可见,当退火温度为1100℃时,MnCr2O4纳米线的直径在90~100 nm的范围内,长度为1~3 μm.SS网的表面非常粗糙,生长了许多纳米线.在MnCr2O4纳米线的顶部可以清楚地看到小球形尖端,揭示它们可能的VLS生长机理.当退火温度升至1150℃时,MnCr2O4纳米线的尺寸约为80~90 nm,长度约为1~5 μm.而且SS表面相对光滑,表面没有大颗粒.在纳米线的顶部没有观察到明显的球形尖端.当退火温度达到1200℃时,MnCr2O4纳米线的尺寸约为60~70 nm,长度约为1~4 μm.
如图4所示,XPS谱图也证实了MnCr2O4纳米线的形成.以单色AlKα X射线作为激发源,确定了Mn2p,Cr2p和O1s的特征峰.图4(d)中的HRTEM显示了MnCr2O4纳米线是具有[110]取向的单晶.SAED也证实了MnCr2O4纳米线的良好结晶性.纳米线的层间间隔为~0.487nm,对应于尖晶石MnCr2O4的(111)面晶格参数.基于以上结果,制成的纳米线为单晶MnCr2O4纳米线.
如图5所示,MnCr2O4纳米线的拉曼光谱与NiCr2O4尖晶石的拉曼光谱非常相似[34].677 cm-1处的峰可以归因于A1g模式,这可能是由于由Cr3+O6八面体的键组成.在550 cm-1处最强的峰,在610和502 cm-1处相对较低的峰可以分配给F2g对称性.与NiCr2O4的拉曼光谱相比,在制备的纳米线的当前光谱中观察到一些峰位移:686 cm-1→677 cm-1,616 cm-1→610 cm-1,554 cm-1→550 cm-1和514 cm-1→502 cm-1.但是,NiCr2O4的拉曼光谱中的430和585 cm-1处的两个峰在MnCr2O4纳米线谱中消失了.以前曾提出,氧化物尖晶石有五种拉曼活性振动模式:A1g+ Eg+3F2g[35].有一些参数会导致峰移动和其他/消失的峰:成分变化(离子取代),结构变化,和尖晶石中离子的位置占有率.峰位移和消失的峰可能是由于尖晶石结构中的Mn取代了Ni离子[31].此外,峰位移也可能是由于合成MnCr2O4纳米线的纳米结构的尺寸效应引起的[36].

1150 ℃,Ar/H2中热退火:(a)、(b)40min;(c)、(d)2.5 h;(e)、(f)5 h.

在Ar/H2中热退火:(a)、(b)1100 ℃;(c)、(d)1150℃;(e)、(f)1200℃
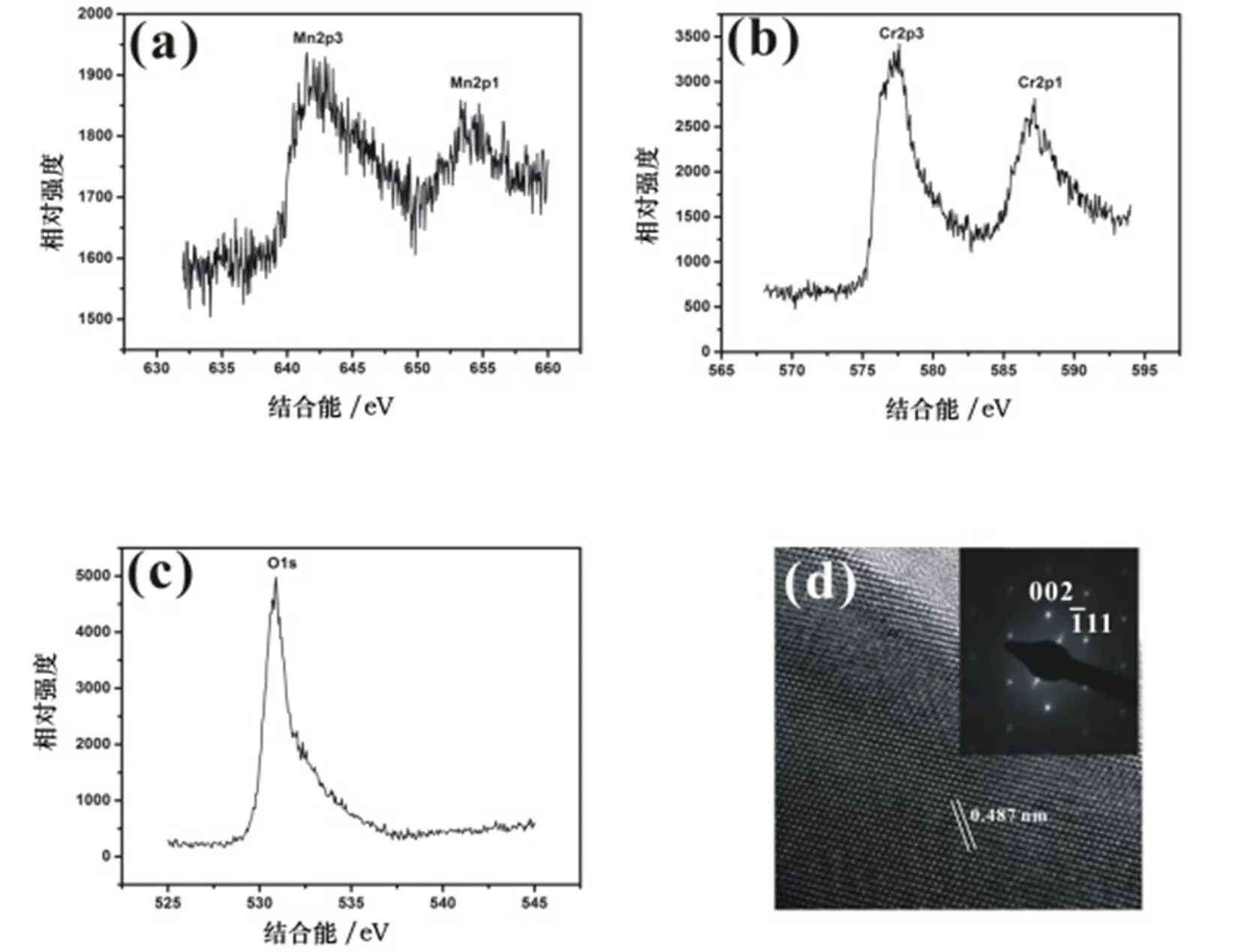
(a)Mn2p;(b)Cr2p;(c)O1s;(d)MnCr2O4纳米线的HRTEM图像,其中的插图是MnCr2O4纳米线的SAED图
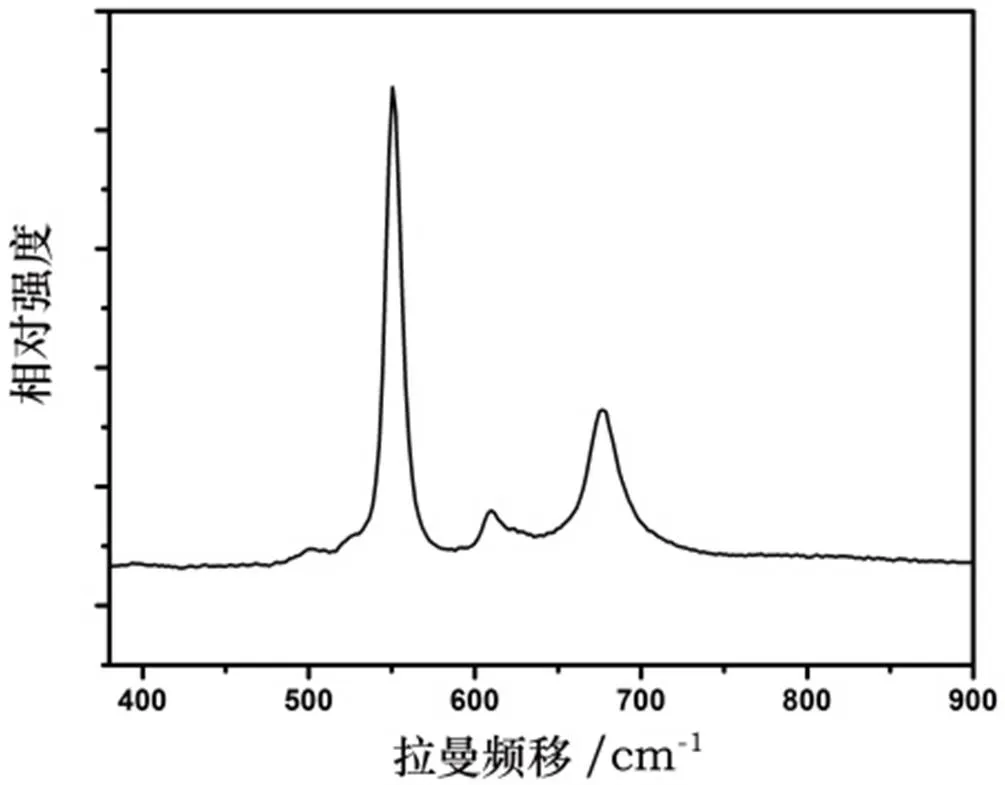
图5 MnCr2O4纳米线的拉曼光谱
2.2 纳米线合成机理
316L不锈钢的主要成分是Fe0.7Cr0.16Ni0.1,在Ar/H2中进行热退火后,合成的是MnCr2O4纳米线,而不是FeCr2O4,NiCr2O4或其他含Fe/Ni的化合物纳米线.有报道在还原性环境下对不锈钢进行热退火可以制备出MnCr2O4尖晶石[37,38].原因是不锈钢中的合金元素,包括Mn,Cr等,相比Fe和Ni更容易被氧化.基于SEM观察,由于MnCr2O4纳米线的头部被纳米颗粒终止,可以总结出属于VLS机理.首先,不锈钢中的Fe和Ni元素可以在高温下在不锈钢表面相互作用并通过以下反应:Fe(s)+ Ni(s)→Fe-Ni(l)形成低共熔合金液体(约1100~1200℃).Cr和Mn元素可通过氧化反应:4Cr(s)+ 3O2(g)→2Cr2O3(s)和2Mn(s)+ O2(g)→2MnO(s)与反应室中周围大气中的微量残留O2反应,生成Cr2O3和MnO化合物.然后Cr2O3和MnO扩散到合金液滴中并通过相互反应:MnO(s)+ Cr2O3(s)→MnCr2O4(s)生成MnCr2O4晶核.当MnCr2O4的浓度达到过饱和时,基于VLS机理,MnCr2O4晶体将沉淀并形成MnCr2O4纳米线.合金催化剂来自不锈钢本身,Mn和Cr的主要元素也来自钢.Ar/H2气氛导致较低的O2分压,并且MnCr2O4晶体的低过饱和度可能对一维MnCr2O4纳米线的生长有利.与先前在还原性气氛下对304不锈钢基板进行热退火的报道不同,在本研究案例中没有观察到MnCr2O4/SiOx纳米电缆[31].因此,这是MnCr2O4纳米线通过Mn和Cr元素的选择性氧化而自催化的VLS生长机理.
2.3 电化学性能
为了研究MnCr2O4纳米线在锂空气电池上的ORR/OER电化学性能,我们组装好标准的锂空气电池进行测试,如图6(a)所示,循环伏安(CV)曲线,没有观察到明显的还原峰.在CV曲线中观察到一个约3.6 V的清晰氧化峰和另一个约4.2 V的宽峰.在1100~1200℃,Ar/H2条件下生长的MnCr2O4纳米线,除了电流幅度稍不同外,都具有相似的CV曲线.
我们测试了这些锂空气电池的电化学阻抗谱(EIS),如图7所示,基于纯不锈钢的锂空气电池的EIS电阻约为11.2 Ω.而经过1200、1150、1100 ℃热退火处理样品的锂空气电池的EIS内阻分别约为15.2 、19.4 Ω、26.6 Ω,发现在不锈钢表面上生长MnCr2O4纳米线后,锂空气电池的EIS电阻增加,且在1100~1200 ℃,EIS内阻随热退火温度的增加而减少.这意味着MnCr2O4纳米线具有比原始纯不锈钢更高的电阻,这可能会抑制其相应的锂空气电池的ORR/OER性能.

图6 (a)锂空气电池组件和电化学测量的示意图;(b)在1150℃的Ar/H2中热退火处理不锈钢样品的锂空气电池的典型CV曲线
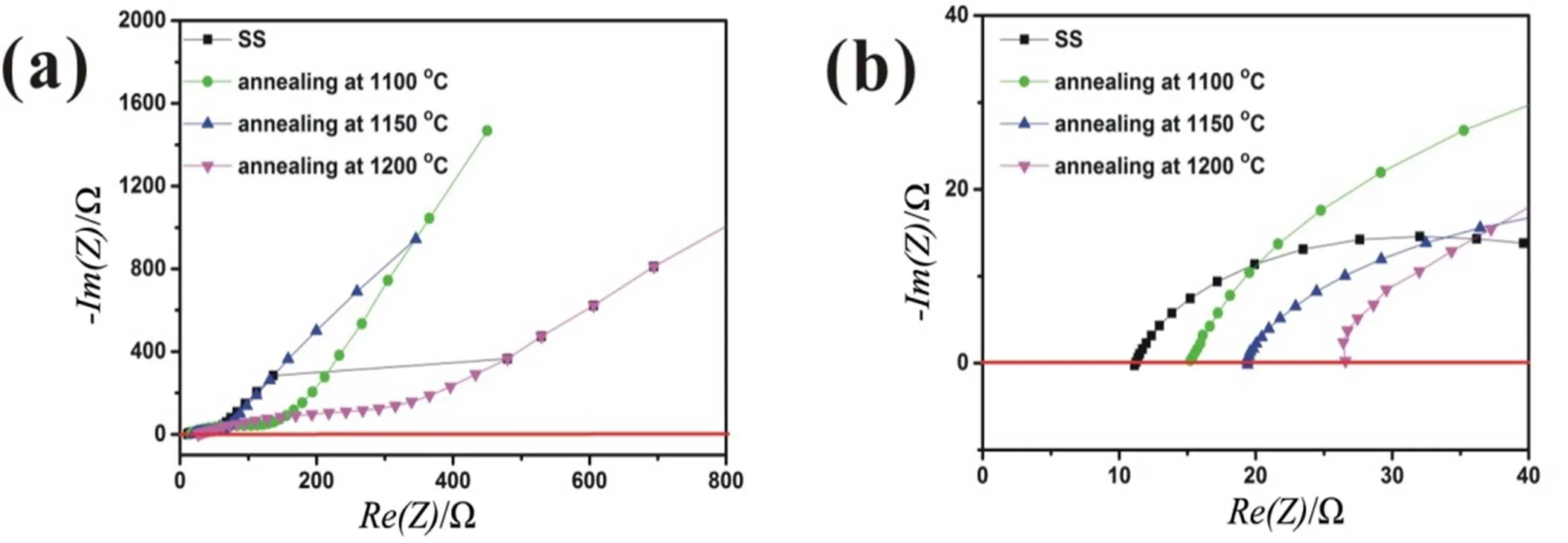
(a)1100,1150和1200℃热退火处理后样品的锂空气电池在0-800 Ω范围内的EIS谱图;(b)在0-40 Ω范围内放大部分的EIS谱图
我们进一步研究了基于纯不锈钢网筛和MnCr2O4纳米线修饰的不锈钢网筛的锂空气电池的ORR/OER循环特性.如图8所示,与用MnCr2O4纳米线修饰的不锈钢基锂空气电池相比,纯不锈钢基锂空气电池显示出更好的ORR/OER循环性能.还观察到,热退火温度也会影响锂空气电池的循环性能.根据EIS测量结果,用MnCr2O4纳米线修饰的不锈钢比纯不锈钢具有更大的电阻.因此,通过热退火在不锈钢上合成的MnCr2O4纳米线对锂空气电池的ORR/OER性能具有抑制作用.还测量到,在1100℃、1150℃和1200℃退火后,不锈钢的Brunauer-Emmet-Teller(BET)比表面积分别为88、10和5 m2/g.具有不同退火温度的不锈钢具有不同数量的MnCr2O4纳米线阵列,并且在不锈钢表面上具有不同的孔.在我们设定的情况下,退火温度越低(在1100~1200℃范围内),比表面积越大.同时,MnCr2O4的EIS内阻比纯不锈钢大,导致锂空气电池的循环性能较差.基于1100℃热退火不锈钢的锂空气电池表现出最差的ORR/OER循环性能.在提高热退火温度后,表面积减小,且EIS内阻减小,改善提高了ORR/OER性能.因此,由于固有的相对较高的EIS内阻特性且比表面积大,热退火后不锈钢上合成的MnCr2O4纳米线对ORR/OER性能具有抑制作用,而且在1100-1200℃范围内随热退火温度的逐渐升高,其对ORR/OER抑制作用逐渐减小.

图8 使用SS网筛和经1100-1200℃热退火后纳米线样品的锂空气电池的ORR/OER性能
根据以上实验结果,我们认为对于基于纳米结构修饰的集电极的锂空气电池,其中2个参数在决定ORR/OER性能方面起着重要作用:(1)合成后纳米结构的电阻(或电导率);(2)这些纳米结构的比表面积.当合成后纳米结构的电阻大于纯不锈钢的电阻时,这些纳米结构的表面积越大,内阻越高,可能导致相对较强的ORR/OER抑制作用.在锂空气电池中,放电时,Li+可以与氧气反应,通过ORR形成绝缘产物Li2O2.MnCr2O4纳米线在不锈钢上的大电阻进一步增加了整个系统的电阻,导致ORR/OER电化学性能较差.充电时,MnCr2O4纳米线的大电阻也阻碍了OER将Li2O2分解为Li+和氧气.然而,MnCr2O4纳米线在锂空气电池上的机理仍不十分清楚.关于MnCr2O4纳米线对锂空气电池ORR/OER电化学性能的影响目前正在进一步研究中.
导电衬底上的过渡金属氧化物纳米线可以成为研究锂空气电池ORR/OER电化学性能的理想模型系统,因为过渡金属氧化物具有作为锂空气电池应用阴极催化剂的巨大潜力[39].通过我们简单的热退火方法进行纳米线生长的合成策略,可以扩展到在相应的导电金属衬底上制备其他金属氧化物纳米线,例如NiO,CuO,Co3O4等.尽管金属衬底在锂空气电池中可能不稳定,但是金属表面上相应金属氧化物纳米线的完全覆盖可以保护金属,并且这些纳米线可以证明其对锂空气电池的电化学性能具有影响.
[1] Bruce P, Freunberger S, Hardwick L, et al. Li-O2and Li-S batteries with high energy storage[J]., 2012(11):19-29.
[2] Girishkumar G, McCloskey B, Luntz A, et al. Lithium -Air Battery: Promise and Challenges[J]., 2010(1):2193-2203.
[3] Liu L, Guo H, Fu L, et al.Critical Advances in Ambient Air Operation of Nonaqueous Rechargeable Li–Air Batteries [DB/OL]. [2019-03-18]. https://doi. org/10.1002/smll. 20190385418 September 2019.
[4] Abraham K and Jiang Z. A polymer electrolyte-based rechargeable lithium/oxygen battery[J]., 1996(143):1-5.
[5] Shao Y. Making Li-Air Batteries Rechargeable: Material Challenges[J]., 2013(23):987-1004.
[6] Yang X, He P and Xia Y. Preparation of mesocellular carbon foam and its application for lithium/oxygen battery[J]., 2009 (11):1127-1130.
[7] Wang Y, Cheng L, Li F, Xiong H, et al. High electrocatalytic performance of Mn3O4/mesoporous carbon composite for oxygen reduction in alkaline solutions[J]., 2007(19):2095-2101.
[8] Li Y, Zhang Z, Duan D, et al. An Integrated Structural Air Electrode Based on Parallel Porous Nitrogen-Doped Carbon Nanotube Arrays for Rechargeable Li-Air Batteries[J]., 2019(9):1412.
[9] Mitchell R, Gallant B, Thompson C, et al. All-carbon- nanofiber electrodes for high-energy rechargeable Li-O2batteries[J]., 2011(4):2952-2958.
[10] Chang Z, Yu F, Liu Z, et al. Co-Ni Alloy Encapsulated by N-doped Graphene as a Cathode Catalyst for Rechargeable Hybrid Li-Air Batteries[J]., 2020(12):4366-4372.
[11] Ryu W. Bifunctional composite catalysts using Co3O4nanofibers immobilized on nonoxidized graphene nanoflakes for high-capacity and long-cycle Li-O2batteries[J]., 2013(13):4190-4197.
[12] Debart A, Paterson A, Bao J, et al. α-MnO2nanowires: A catalyst for the O2electrode in rechargeable lithium batteries[J]., 2008(47):4521-4524.
[13] Zhang G. alpha-MnO2/Carbon Nanotube/Carbon Nanofiber Composite Catalytic Air Electrodes for Rechargeable Lithium-air Batteries[J]., 2011(158):A822-A827.
[14] Ida S. Manganese oxide with a card-house-like structure reassembled from nanosheets for rechargeable Li-air battery[J]., 2012(203):159-164.
[15] Oh D. Biologically enhanced cathode design for improved capacity and cycle life for lithium-oxygen batteries[J]., 2013(4):2756.
[16] Peng Z, Freunberger S, Chen Y, et al. A Reversible and Higher-Rate Li-O2Battery[J]., 2012(337):563-566.
[17] Thotiyl M. A stable cathode for the aprotic Li-O2battery[J]., 2013(12):1049-1055.
[18] Cao Y. Coaxial nanocables of p-type zinc telluride nanowires sheathed with silicon oxide: synthesis, characterization and properties[J]., 2009(20):455702.
[19] Cao Y. Single-crystalline ZnTe nanowires for application as high-performance Green/Ultraviolet photodetector[J]., 2011(19):6100-6108.
[20] Luo L. Silicon nanowire sensors for Hg2+and Cd2+ions[J]., 2009(94):193101.
[21] Shen L, Uchaker E, Zhang, X, et al. Hydrogenated Li4Ti5O12Nanowire Arrays for High Rate Lithium Ion Batteries[J]., 2012(24):6502-6506.
[22] Li Y, Tan B and Wu Y. Mesoporous Co3O4nanowire arrays for lithium ion batteries with high capacity and rate capability[J]., 2008(8):265-270.
[23] Jiang J. Direct Synthesis of CoO Porous Nanowire Arrays on Ti Substrate and Their Application as Lithium-Ion Battery Electrodes[J]., 2010(114):929-932.
[24] Chan C. High-performance lithium battery anodes using silicon nanowires[J]., 2008(3):31-35.
[25] Chan C, Zhang X and Cui Y. High capacity Li ion battery anodes using Ge nanowires[J]., 2008(8):307-309.
[26] Fava F, Baraille I, Lichanot A, et al. On the structural, electronic and magnetic properties of MnCr2O4spinel[J]., 1997(9):10715-10724.
[27] Song S, Yuan Z and Xiao P. Electrical properties of MnCr2O4spinel[J]., 2003(22):755-757.
[28] Winkler E. Magnetocrystalline interactions in MnCr2O4spinel[J]., 2009(80):104418.
[29] Bhowmik R, Ranganathan R and Nagarajan R. Lattice expansion and noncollinear to collinear ferrimagnetic order in a MnCr2O4nanoparticle[J]., 2006(73):144413.
[30] Masrour R, Hamedoun M and Benyoussef A. Magnetic properties of MnCr2O4nanoparticle[J]., 2010(322):301-304.
[31] Chen Y. Selective oxidation synthesis of MnCr2O4spinel nanowires from commercial stainless steel foil[J]., 2007(7):2279-2281.
[32] Cao Y, Cao J, Zheng M, et al. Synthesis, characterization, and electrochemical properties of ordered mesoporous carbons containing nickel oxide nanoparticles using sucrose and nickel acetate in a silica template[J]., 2007(180):792-798.
[33] Lu Y, Gasteiger H and Shao-Horn, Y. Catalytic Activity Trends of Oxygen Reduction Reaction for Nonaqueous Li-Air Batteries[J]., 2011(133):19048-19051.
[34] Maslar J, Hurst W, Bowers W, et al. In situ Raman spectroscopic investigation of stainless steel hydrothermal corrosion[J]., 2002(58):739-747.
[35] Chopelas A and Hofmeister A. Vibrational Spectroscopy of Aluminate Spinels at 1 Atm and of MgAl2O4to over 200-Kbar[J]., 1991(18):279-293.
[36] Chandramohan P, Srinivasan M, Velmurugan S, et al. Cation distribution and particle size effect on Raman spectrum of CoFe2O4[J]., 2011(184):89-96.
[37] Olefjord I, Elfstrom B. The Composition of the Surface during Passivation of Stainless-Steels[J]., 1982(38):46-52.
[38] Lou X, Archer L and Yang Z. Hollow Micro- /Nanostructures: Synthesis and Applications[J]., 2008(20):3987-4019.
[39] Debart A, Bao J, Armstrong G, et al. An O2cathode for rechargeable lithium batteries: The effect of a catalyst[J]., 2007(174):1177-1182.
Self-catalyzed Growth of MnCr2O4Nanowires and Their Inhibitory Effect on ORR/OER
CAO Yulin
(,,,,,)
This paper describes a vapor-phase approach to the facial synthesis of spinel single-crystalline MnCr2O4nanowires supported on the surfaces of commercial conducting stainless steel mesh substrates under a reducing atmosphere. A typical procedure simply included the thermal annealing of these substrates in Ar/H2mixed gas and within the temperature range from 1100 to 1200 °C. Electron microscopic studies indicated that these nanowires have a diameter within the range of 50-100 nm and lengths of 1-10 μm by varying the temperature and growth time. A possible self-catalyzed mechanism was proposed to account for the growth of these MnCr2O4nanowires. The effect of these nanowires supported on stainless steel mesh on non-aqueous Li-air batteries was also studied. The effect was found to be dependent on surface areas, which resulted from annealing temperatures. The results of this work help us understand the relationship between the surface nanostructures on conducting substrates as air electrode of Li-air batteries and their electrochemical performances.
MnCr2O4nanowires; thermal annealing; self-catalyzed growth; Li-air batteries; ORR/OER
2020-01-08
2017年深圳职业技术学院校级青年创新项目“单层二维介孔碳纳米复合材料的制备及其在高性能金属-氧电池中的应用”(编号:601722K35019);2017年深圳市科技创新委员会面上项目“基20170075新型高稳定锑基高效薄膜太阳能电池的研究”(编号:JCYJ20170413113645633);2018年广东省科技厅面上项目“锂离子电池锡铋纳米合金/介孔碳球负极材料的研究”(编号:2018A030313725)部分成果.
曹喻霖,男,江苏如东人,博士,讲师,主要研究方向为半导体纳米材料、能源物理与材料、透明导电物等.
O782.7
A
1672-0318(2020)03-0019-10
10.13899/j.cnki.szptxb.2020.03.004
