新试剂2-萘酚乙酰酪氨酸二氨基苯甲酰替胺的合成及铜(Ⅱ)的测定研究
2020-06-19汪大巍操燕明
汤 军,汪大巍,操燕明
(武汉华夏理工学院 生物与制药工程学院,湖北 武汉 430223)
铜是工业上广泛应用的金属,在环境中分布很广. 铜也是人体及动植物所必需的微量元素,对机体的新陈代谢有重要的调节作用,但过量摄入铜亦会产生危害[1]. 过量铜对水生生物的危害较大,其毒性与形态有关,游离铜离子的毒性比络合态的铜大得多,因此研究铜的分析方法一直受到人们关注[2]. 光度法测定铜的试剂很多[3],有荧光酮类、安替比林类、变色酸偶氮类、卟啉类、三氮烯类显色剂,但是偶氮类试剂较少.
联苯胺曾经是重要的染料中间体[4],其两个氨基均可重氮化,可与各种偶合组分进行对称和不对称偶合,制成各种色泽的多偶氮染料. 其合成简单,价格低廉,着色浓厚,遮盖力强,使用范围广. 但联苯胺类染料严重的致癌性已成为主要矛盾,其代用染料的研究非常活跃. 代用染料研究的方向首先是要考虑合成的产品是安全染料[5],不会分解和产生禁用中间体;其代用品在性能、效果上要予以保证[6].
本文以研究开发环境友好型染料代替致癌性试剂为目标,以二氨基苯甲酰替胺代替联苯胺,设计合成了新的显色试剂2-萘酚乙酰酪氨酸二氨基苯甲酰替胺(2-NATDAB),研究了其与铜(II)的显色反应,确立了2-NATDAB测定Cu(Ⅱ)含量的方法,测定了废水中Cu(Ⅱ)的含量.
1 实验部分
1.1 主要仪器
BRUKE AVANCE 500型核磁共振仪(瑞士BRUKE公司),UV-2550紫外-可见分光光度计(日本岛津公司),pHS-3B精密pH计(上海精密科学仪器有限公司).
1.2 2-萘酚乙酰酪氨酸二氨基苯甲酰替胺的合成
以4,4′-二氨基苯甲酰替苯胺、2-萘酚和N-乙酰-L-酪氨酸为原料,采用重氮化偶合反应,合成了一种新型的4,4′-二氨基苯甲酰替苯胺偶氮试剂2-萘酚乙酰酪氨酸二氨基苯甲酰替胺(2-NATDAB),合成路线见图1.

图1 2-萘酚乙酰酪氨酸二氨基苯甲酰替胺的合成路线Fig.1 Synthetic route of 2-NATDAB
称取4,4′-二氨基苯甲酰替苯胺2.3 g (0.01 mol)于三口烧瓶,加入20 mL水,6 mL浓HCl,搅拌加热使其溶解,外加冰水浴使三口烧瓶温度保持在0~5 ℃. 另取1.38 g NaNO2溶于4 mL水冷却,将其溶液慢慢滴入上述溶液,滴加的过程中确保三口烧瓶温度不得超过10 ℃,滴加完后,等待反应30 min,溶液变为棕红色,pH测试为1~2. 用淀粉KI试纸检测,显示为淡蓝色.
另取1.44 g 2-萘酚溶于10 mL 10% NaOH溶解,用NaOH控制pH为10左右. 立刻加入上述重氮盐溶液,控制pH为8~10左右,反应30 min,然后将乙酰酪氨酸2.22 g溶于20 mL乙醇中,再滴加到上述单偶氮体系中,控制pH为8~10左右,温度控制在10 ℃以内,室温再反应2 h,然后盐析,过滤,干燥.
将固体溶于二氯甲烷进行重结晶,冷却,抽干,烘干,最后得成品.
1H NMR (600 MHz, DMSO-d6)δ: 10.61(1H, -COOH),10.30 (1H, -OH), 8.77~6.86 (18H, Ar-H), 3.97(1H, -NH), 3.02 (1H, -CH), 1.76 (3H, -CH3).13C NMR (75 MHz, CDCl3)δ: 177.0 (-COOH), 170.9 (-NHCO), 165.2 (-COCH3), 150.6 (苯), 148.7(苯),139.6 (苯),136.0 (苯), 132.0 (苯,萘),129.2 (苯,萘),124.1 (苯,萘), 117.9 (苯),59.3 (CHCOOH), 36.7 (-CH2CH), 18.0 (1C, -CH3). EI-MS:m/z, 618(M+2)+,617(M+1)+,616(M)+. 元素分析,C18H18ClN3O4,实测值(计算值),%:C 66.12 (66.23),H 4.55 (4.58),N 13.10 (13.62),O 16.23 (15.57).
1.3 主要试剂
N-乙酰-L-酪氨酸按文献[7]方法合成,其余所用化学试剂均为分析纯或化学纯.
1.3.1 Cu(Ⅱ)标准溶液
称取0.25 g硝酸铜用蒸馏水定容到100 mL容量瓶中,然后取2.5 mL稀释到25 mL,配成1×10-5mol/L的工作液.
1.3.2 表面活性剂
十二烷基苯磺酸钠(SDBS)配成质量分数为0.5%的水溶液;聚乙二醇辛基苯基醚(OP),吐温-80(Tween-80)均配成体积分数为5%的水溶液.
1.3.3 缓冲溶液
按照标准配置方法配制成0.2 mol/L磷酸氢二钠溶液和0.1 mol/L柠檬酸溶液,然后用上述溶液配制成pH为2~8的一系列缓冲溶液;取氯化铵5.4 g,加水20 mL溶解后,加浓氯溶液35 mL,再加水稀释至100 mL,即得氨-氯化铵缓冲液(pH 10.0);取50 mL 0.05 mol/L磷酸氢二钠和4.1 mL 0.1 mol/L氢氧化钠溶液即得pH为11的缓冲溶液;取50 mL 0.05 mol/L磷酸氢二钠和26.9 mL 0.1 mol/L氢氧化钠溶液即得pH为12的缓冲溶液;
1.3.4 试剂溶液
称取0.6 g 2-NATDAB试剂,用N,N-二甲基甲酰胺定容到100 mL容量瓶中,再取2.5 mL稀释到25 mL,配成1×10-5mol/L显色剂溶液.
1.4 实验方法
在25 mL容量瓶中,准确加入一定量的金属离子标准溶液,然后依次加入一定量体积分数为5% OP溶液、一定pH的缓冲溶液和一定量质量分数的试剂溶液,用蒸馏水稀释至刻度,摇匀,放置一定时间后,用1 cm石英比色皿,在最大吸收波长处,以试剂空白为参比测量吸光度.
2 结果与讨论
2.1 紫外可见吸收光谱

图2 试剂络合物的吸收光谱Fig.2 UV spectrum of 2-NATDAB and Cu(Ⅱ) complex
2.2 表面活性剂的选择
分别用阴离子表面活性剂十二烷基苯磺酸钠(SDBS)、非离子表面活性剂Tween、OP作增溶增敏剂,测试试剂与Cu(Ⅱ)的配合物吸光度,见图3,实验结果表明非离子表面活性剂OP的增溶增敏效果最好. 故本实验采用OP作为表面活性剂.

图3 表面活性剂的选择Fig.3 UV spectrum of 2-NATDAB and Cu(Ⅱ) complex with various surfactants
2.3 表面活性剂的用量
取不同用量OP溶液,测试不同用量下的Cu(Ⅱ)的配合物吸光度,实验结果如图4所示.

图4 OP用量对显色体系吸光度的影响Fig.4 Influence of OP dosage on absorbance of system
OP的较佳用量范围在2.5~4.5 mL,故本实验时选择体积分数为5%的OP 4.0 mL.
2.4 pH的影响
在配合物最大吸收波长处测定了不同pH下各金属离子配合物的吸光度,见图5.

图5 pH值对显色体系吸光度的影响Fig.5 Influence of pH on absorbance of system
由图可知,较佳的pH范围是5~9,本实验选择pH=6的缓冲溶液.
2.5 缓冲溶液用量
在配合物最大吸收波长处测定了不同缓冲溶液用量下试剂与Cu(Ⅱ)显色配合物的吸光度,见图6.

图6 不同缓冲溶液用量下吸光度的影响Fig.6 Influence of buffer solution dosage on absorbance of system
缓冲溶液的用量大于2.5 mL后,配合物的吸光度达到最大且恒定,故本实验选用2.5 mL的缓冲溶液.
2.6 金属离子配合物的显色稳定时间
在室温下,使显色剂与Cu(Ⅱ)显色,在不同时间测定配合物的吸光度. 结果见表1.
“卧游”是从眼睛到心灵的转换,贯穿了从观看行为到内心体悟的整个过程。最后指向的是人的身心自由及天地大道,体现出一定的宗教语境与终极价值。但如果放眼于山水画这个普遍的概念,“卧游”的意义也就不仅仅在于其宗教层面,而在于对画面空间建构图像本身功能和意义的理解。“卧游”的技术与理念,很可能与“悟对通神”、“澄怀观道”等观念存在着某些特殊的联系。

表1 配合物的显色稳定时间
结果表明,显色剂与Cu(Ⅱ)显色时,15 min后显色完全,12 h后配合物就开始分解. 说明形成的金属离子配合物在15 min至12 h内是稳定的.
2.7 各组分加入顺序的影响
由于这类偶氮类试剂不溶于水,因此能起到增溶作用的表面活性剂必须在加入试剂之前加进溶液中,以免试剂在水中产生浑浊.
比较试剂和金属离子加入顺序的影响,采用的加入顺序是先加表面活性剂,再加入缓冲溶液,再加试剂溶液,最后加入金属离子溶液.
2.8 配合物的组成
用平衡移动法[8],可以确定显色剂与金属离子的配合比.
利用平衡移动法确定配合物的表观稳定常数和配位比,设溶液中存在金属离子M与配位体L形成的配合物MLn的平衡:
M+nL=MLnβ=[MLn]/[M][L]n
取对数,得:
lgβ=lg[MLn]-lg[M]-nlg[L](1)
整理式(1)可得:
lg[MLn]/[M]=lgβ+nlg[L](2)
以lg[MLn]/[M]为纵坐标,lg[L]为横坐标作图,则可得一直线,其斜率n即为配合物MLn的配位数,直线在纵坐标上的截距即为lgβ,从而得到配合物的表观稳定常数β=1.56×104,金属离子配合物在此条件下有较好的稳定性.
测定了490 nm波长的lgA-lg[L]图,见图7,可以通过曲线斜率0.896 5近似得出显色剂与Cu(Ⅱ)的配合比为1∶1.
2.9 工作曲线
分别取不同质量的金属离子标准工作溶液,测定溶液的吸光度见图8.

图7 平衡移动法lgA-lg[L]图Fig.7 lgA-lg[L] of Balanced moving method
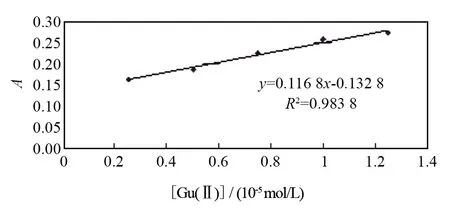
图8 显色剂与Cu(Ⅱ)的工作曲线Fig.8 Working curve of 2-NATDAB and Cu(Ⅱ) complex
显色剂与Cu(Ⅱ)的工作曲线的相关结果如图8所示,吸光度与金属离子浓度在(0.25~1.25)×10-5mol/L范围内呈线性相关,y=0.116 8x+0.132 8,R2=0.983 8.
2.10 样品测定
按以上选定最佳参数,从某工厂取处理前后的废水水样进行测试. 结果如表2所示. 相对标准偏差为0.91%和0.72%,表明该方法具有良好的准确性和重复性.

表2 废水中铜离子含量的测定
本实验所测得某工厂处理过的废水中的铜离子的含量0.474 mg/L,符合现实中大部分工厂0.5 mg/L污水综合排放标准(GB8978-1996)[9]. 结果显示本方法可用于企业污水铜离子含量测定.
3 结论
以4,4′-二氨基苯甲酰替苯胺与2-萘酚、乙酰酪氨酸,发生重氮化偶合反应得到新型试剂2-萘酚乙酰酪氨酸二氨基苯甲酰替胺(2-NATDAB),确证了所合成化合物的结构.
研究了试剂2-NATDAB与铜(II)的显色反应. 在紫外吸收光谱、表面活性剂的选择与用量、酸度、缓冲液用量、显色时间及体系稳定性、配合物组成、工作曲线、工厂废水样品中铜的测定等方面做了深入研究和优化,建立了微量铜的检测方法. 本方法有望在工业废水质量检测系统中得到使用.
