富马酸替诺福韦艾拉酚胺片人体生物等效性及饮食对其药动学的影响*
2020-06-18励璇玮唐玲王燕陈绍春陈柠李乐丁黎
励璇玮,唐玲,王燕,陈绍春,陈柠,李乐,丁黎
(1.中国药科大学药物分析系,南京 210009;2.南京科利泰医药科技有限公司,南京 211100;3.大理大学药学与化学学院,大理 671000)
替诺福韦艾拉酚胺(tenofovir alafenamide,TAF)是替诺福韦(tenofovir,TFV)的前体药物,是一种治疗慢性乙型肝炎(乙肝)的新型核苷酸逆转录酶抑制剂。该药物由美国吉利德公司研发,商品名为Vemlidy®,于2016年10月被美国食品药品管理局(FDA)批准用于治疗成人慢性乙肝,这也是近10年来美国 FDA 批准唯一治疗慢性乙肝的新药[1]。替诺福韦艾拉酚胺作为亲脂性化合物,通过口服给药,经转运体进入原代肝细胞,在细胞内因羧酸酯酶1(carboxylesterase 1,CES1)作用被水解为替诺福韦。原代肝细胞内细胞激酶将替诺福韦磷酸化,使其转化为具有药理活性的替诺福韦二磷酸酯。替诺福韦二磷酸酯会嵌入到乙肝病毒的DNA逆转录酶中,以此抑制DNA的复制,进而阻止乙肝病毒的复制,治疗慢性乙肝[2]。到目前为止,替诺福韦艾拉酚胺片在中国人体内药动学特征并无系统性研究报道。笔者在本文旨在建立一种高效液相色谱-串联质谱(high performance liquid chromatography-mass spectrometry/mass spectrometry,HPLC-MS/MS)法同时测定人血浆中替诺福韦艾拉酚胺及其活性代谢物替诺福韦的方法,评价富马酸替诺福韦艾拉酚胺片国内仿制药与国外原研药的生物等效性,并考察饮食对替诺福韦艾拉酚胺及其代谢物替诺福韦在健康中国人体内药动学特征的影响,报道如下。
1 材料与方法
1.1药品与试剂 受试制剂:富马酸替诺福韦艾拉酚胺片(石家庄龙泽制药股份有限公司,批号:1800026151,规格:每片25 mg);参比制剂:富马酸替诺福韦艾拉酚胺片(商品名:Vemlidy®,Gilead Sciences,Inc,规格:每片25 mg,批号:ZFTMA);富马酸替诺福韦艾拉酚胺对照品(石家庄龙泽制药股份有限公司,批号:1800036091,含量:99.8%);替诺福韦对照品(Toronto Research Chemicals 公司,批号:1-JMO-90-1,含量:96%);内标富马酸替诺福韦艾拉酚胺-d5(Toronto Research Chemicals公司,批号:12-XAL-35-3,纯度:92.37%);内标替诺福韦-d7(TLC Pharmaceutical Standards Ltd.,批号:2776-020A4,纯度:96.1%);甲醇、乙腈(色谱纯,Merck KGaA);甲酸(ACS-Reagent,Sigma-Aldrich公司);试验用水为超纯水(Milli-Q制备)。
1.2仪器 高效液相色谱仪(液相泵:LC-30AD,柱温箱:CTO-20AC,控制器:CBM-20A Lite,脱气机:DGU-20A5R,自动进样器:SIL-30ACMP,Shimadzu);质谱仪(Triple QuadTM5500,Applied Biosystems/ Sciex);质谱工作站(Analyst 1.6.3,Applied Biosystems/ Sciex);电子天平(型号:MSA6.6S-OCE-DM,Sartorius公司,感量:0.001 mg);离心机(型号:Heraeus Muitifuge X1R,Thermo Fisher公司);氮吹仪[型号:NG150-1A,科学仪器(北京)有限公司];纯水仪(型号:Milli-Q,Merck Millipore公司)。
1.3HPLC-MS/MS法的色谱条件与质谱条件
1.3.1色谱条件 色谱柱:Venusil ASB C18(2.1 mm×50 mm,3 μm);流动相:0.1%甲酸水溶液(A)-乙腈(B),采用梯度洗脱:0~1.5 min,2%B;>1.5~1.6 min,2%→36%B;>1.6~4.0 min,36%B;>4.0~4.1 min,36%→100%B;>4.1~5.1 min,100%B;>5.1~5.2 min,100%→2%B;>5.2~6.5 min,2%B。进样体积:8 μL;流速:0.3 mL·min-1;柱温:40 ℃。
1.3.2质谱条件 采用电喷雾离子化源(ESI),在多反应监测(multiple reaction monitoring,MRM)模式下同时对替诺福韦艾拉酚胺(478.1→270.0,去簇电压为82 V,碰撞电压为23 V)、替诺福韦(288.1→176.1,去簇电压为71 V,碰撞电压为35 V)、内标替诺福韦艾拉酚胺-d5(482.2→270.0,去簇电压为80 V,碰撞电压为44 V)和内标替诺福韦-d7(295.1→183.1,去簇电压为71 V,碰撞电压为37 V)进行正离子检测。
1.4血浆样品前处理 在冰浴条件下,取含酸血浆样品血浆(50%甲酸水溶液=1000:10)120 μL,加入内标工作溶液(替诺福韦艾拉酚胺-d5: 5.00 ng·mL-1,替诺福韦-d7:500 ng·mL-1)30 μL和沉淀剂甲醇-乙腈(1:1)480 μL,涡旋10 min,在4 ℃条件下以1789×g离心10 min,取上清液360 μL,氮气吹干后用0.1%甲酸水溶液250 μL复溶,取复溶液8 μL,进行HPLC-MS/MS定量分析。
1.5生物等效性研究 本试验服从《赫尔辛基宣言》中规定伦理原则,经过武汉市传染病医院药物临床试验伦理委员会审批同意后实施,临床批件号为GCP-ICT-2019-29.01。所有受试者均自愿签署知情同意书,并经过严格体检证明心、肝、肾等功能正常,无既往病史、药物过敏史及药物滥用史,首次给药前14 d内未使用过任何药物,符合入选标准。
1.6空腹给药试验方案 空腹试验入组健康受试者42例,男27例,女15例,年龄(29.4±6.3)岁,体质量(59.7±6.7)kg,身高(162.6±6.7)cm,平均体质量指数(BMI)为(22.5±1.8)kg·(m2)-1。试验采用随机、开放、单剂量、两制剂、三序列、三周期、部分重复交叉等效性试验设计,每周期间清洗期为10 d,所有受试者于每周期给药前1 d入住Ⅰ期病房,并统一晚餐,不禁水,隔夜空腹至少10 h。给药当天,受试者于试验给药前静脉埋留置针,给药前1 h内测量生命体征,然后根据随机表空腹服用受试制剂或参比制剂1片,给药时研究者监督受试者将药物放置于舌上方,水240 mL送服(需吞服切勿弄碎或咀嚼),给药后研究者对受试者口腔进行检查,以确保药已被吞咽。给药前1 h至给药后1 h不得饮水,其他时间正常饮水,给药后保持上身直立状态2 h。受试者给药后4 h内禁食,给药4,10 h后分别进食统一标准午餐和晚餐。空腹试验于每周期给药前0 h及给药后5,10,15,20,30,45 min及1,1.25,1.5,2,3,4,5,8,12,24,48,72,96,120 h(共21个采血点),从受试者上肢静脉采集血样。每个采血点采集静脉血4 mL,将之加入到预冷的含EDTA-K2抗凝剂的真空采血管中,在2~8 ℃条件下以2000×g离心10 min。在冰浴条件下,分取2份血浆,每份0.70 mL,置于含有50%甲酸水溶液7.0 μL的冻存管中,混匀,于-70 ℃冰箱中保存待测。
1.7餐后给药试验方案 餐后试验入组健康受试者42例,男24例,女18例,年龄(24.0±5.2)岁,体质量(61.3±6.5)kg,身高(165.2±8.1)cm,平均BMI为(22.5±1.7) kg·(m2)-1。与空腹试验相同,所有受试者于每周期给药前1 d入住Ⅰ期病房,并统一晚餐,不禁水,隔夜空腹至少10 h。给药当天,受试者于给药前30 min时开始进食标准高脂餐(吐司60 g、培根80 g、黄油13 g、煮鸡蛋110 g、薯条55 g、牛奶250 mL),并在30 min内用餐完毕,在开始进餐后30 min(±30 s)准时服用受试制剂或参比制剂1片。餐后试验于每周期给药前0 h及给药后10,20,30,45 min及1,1.25,1.5,2,2.5,3,3.5,4,5,8,12,24,48,72,96,120 h(共21个采血点),从受试者上肢静脉采集血样。
1.8统计学方法 使用Phoenix WinNonlin 6.4版药动学统计软件以非房室法计算替诺福韦艾拉酚胺及替诺福韦的药动学参数,并根据《高变异药物生物等效性研究技术指导原则》[3]对替诺福韦艾拉酚胺主要药代学参数峰浓度(Cmax)、血药浓度-时间曲线下面积(AUC0-120)和AUC0-∞进行生物等效性分析。
2 结果
2.1HPLC-MS/MS同时测定人血浆中替诺福韦艾拉酚胺及替诺福韦的检测方法评价 血浆中内源性物质不干扰替诺福韦艾拉酚胺及替诺福韦的测定。替诺福韦艾拉酚胺的标准曲线线性范围为1.00~300 ng·mL-1,替诺福韦的标准曲线线性范围为0.350~20.0 ng·mL-1,线性关系好;准确度及精密度结果见表1。血浆样品中替诺福韦艾拉酚胺的提取回收率为95.2%~100.0%,替诺福韦提取回收率为75.1%~76.8%,内标替诺福韦艾拉酚胺-d5的回收率为98.5%,内标替诺福韦-d7回收率为75.8%。替诺福韦艾拉酚胺在225~1000 ng·mL-1浓度范围内,替诺福韦在18.0~50.0 ng·mL-1浓度范围内,稀释因子为1:5时具有良好的稀释可靠性。含甲酸的血浆样品(血浆:50%甲酸水溶液=1000:10)在室温条件下放置4.9 h稳定性良好,在冰浴条件下放置20.3 h稳定性良好,在-70 ℃条件下5次冻融循环稳定性良好,长期冰冻56 d稳定性良好;血浆样品处理后上清液在8 ℃自动进样器中放置6 d稳定性良好;基质效应(包括溶血基质效应与高脂基质效应)、残留均不影响血浆中替诺福韦艾拉酚胺及替诺福韦的准确定量。方法学验证结果表明本方法可用于临床试验血浆样品的分析。
2.2药动学和生物等效性评价结果
2.2.1空腹试验 42名健康受试者空腹口服富马酸替诺福韦艾拉酚胺受试制剂或参比制剂后,替诺福韦艾拉酚胺平均血药浓度-时间曲线见图1,主要药动学参数见表2,替诺福韦平均血药浓度-时间曲线见图2,主要药动学参数见表3。采用Phoenix WinNonlin 6.4软件评价受试制剂和参比制剂的生物等效性,结果表明,在空腹试验中,参比制剂的替诺福韦艾拉酚胺Cmax、AUC0-120和AUC0-∞的个体内标准差(SWR)均小于0.294,故采用平均生物等效性(Average bioequiva-lence,ABE)评价标准来评价两种制剂的生物等效性。参比制剂与受试制剂的替诺福韦艾拉酚胺的Cmax、AUC0-120和AUC0-∞的几何均值比值(T/R)的90%置信区间(CI)均落在80.00%~125.00%范围内,符合生物等效性标准,具体结果见表4。作为临床参考,活性代谢物替诺福韦的主要药动学参数Cmax、AUC0-120和AUC0-∞的几何均值及几何均值比值(T/R)见表3。
表1 日内及日间的准确度、精密度

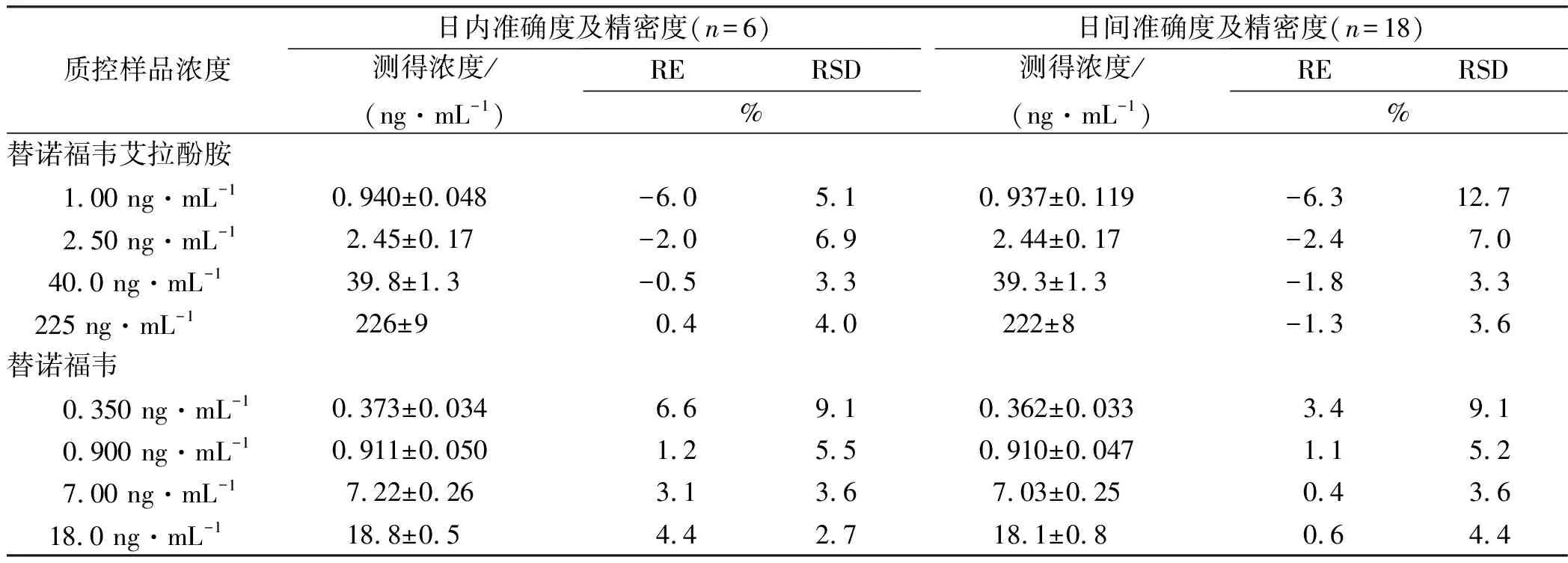
质控样品浓度日内准确度及精密度(n=6)测得浓度/(ng·mL-1)RERSD%日间准确度及精密度(n=18)测得浓度/(ng·mL-1)RERSD%替诺福韦艾拉酚胺 1.00 ng·mL-1 0.940±0.048-6.05.1 0.937±0.119-6.312.7 2.50 ng·mL-1 2.45±0.17-2.06.9 2.44±0.17-2.47.0 40.0 ng·mL-1 39.8±1.3-0.53.3 39.3±1.3-1.83.3 225 ng·mL-1 226±90.44.0 222±8-1.33.6替诺福韦 0.350 ng·mL-1 0.373±0.0346.69.1 0.362±0.0333.49.1 0.900 ng·mL-1 0.911±0.0501.25.5 0.910±0.0471.15.2 7.00 ng·mL-1 7.22±0.263.13.6 7.03±0.250.43.6 18.0 ng·mL-1 18.8±0.54.42.7 18.1±0.80.64.4

3 讨论
3.1检测方法比较 笔者在本试验采用HPLC-MS/MS法同时测定人血浆中替诺福韦艾拉酚胺及替诺福韦的含量,由于两化合物极性差异较大,试验过程中尝试多种不同型号的色谱柱,最终选择Venusil ASB C18色谱柱,此色谱柱可使用100%水作为流动相,适用于极性化合物替诺福韦的分析,有效缩短分析时间。试验中也对不同沉淀剂进行筛选,甲醇-乙腈(1:1)相较纯甲醇、纯乙腈或含酸乙腈明显提高替诺福韦的回收率,最终建立的方法灵敏度高,替诺福韦艾拉酚胺和替诺福韦的定量下限可达1.00和0.350 ng·mL-1且专属性良好。
3.2血浆样品稳定性 在方法开发阶段,发现替诺福韦艾拉酚胺在血浆中会逐渐转化为其代谢物替诺福韦,这可能是由于替诺福韦艾拉酚胺作为一种磷酰胺酯在弱碱性的血浆中易水解[4]。因此,本试验尝试在血浆中加入不同比例的甲酸或乙酸来抑制其水解,最终选择50%甲酸水溶液作为稳定剂,加入比例为血浆-50%甲酸水溶液=1 000:10。稳定性考察结果证明在含酸血浆中替诺福韦艾拉酚胺稳定性良好,满足临床试验的需求,保证本试验药动学数据的准确性。
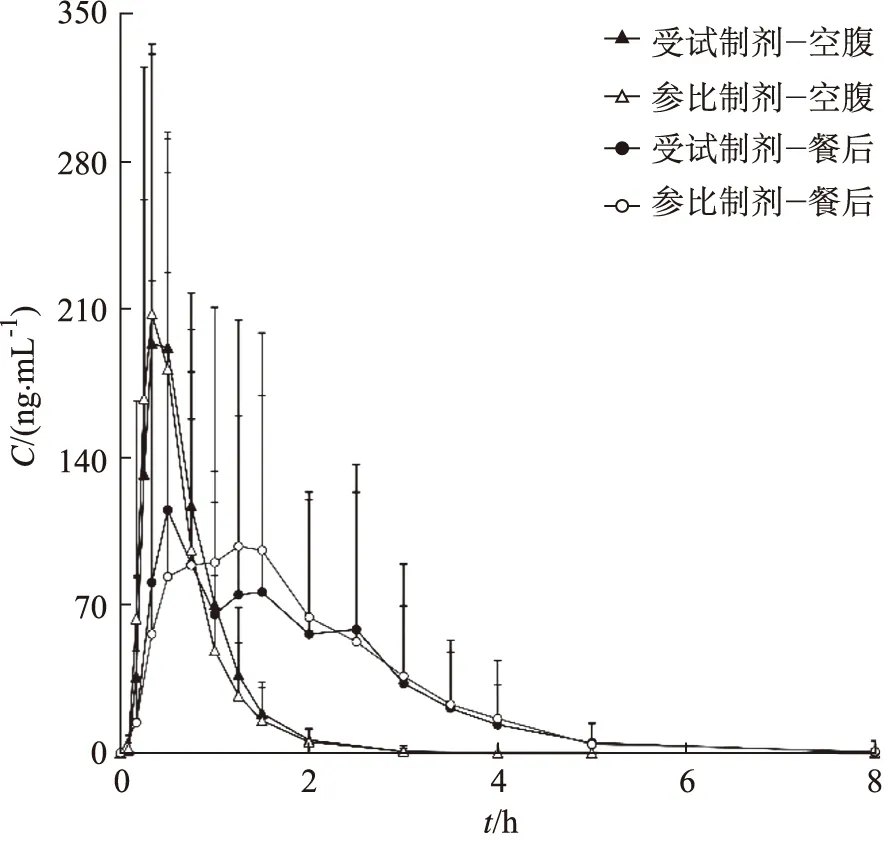
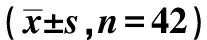
Fig.1 Mean plasma concentration-time profiles of tenofovir alafenamide after oral administration of test and reference preparation under fasting and fed conditions in 42 healthy volunteers
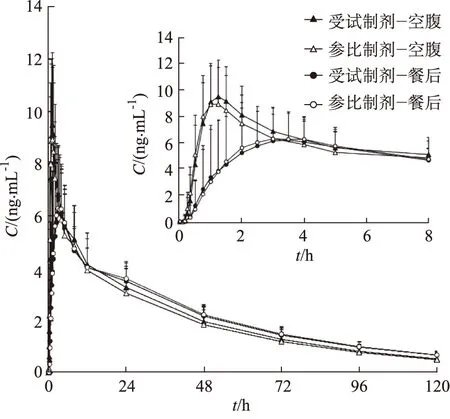
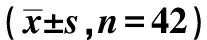
Fig.2 Mean plasma concentration-time profiles of tenofovir after oral administration of test and reference preparation under fasting and fed conditions in 42 healthy volunteers
3.3试验方案设计 本研究在正式试验前开展空腹与餐后各12例健康受试者的两周期交叉生物等效性预试验,获得替诺福韦艾拉酚胺的最大个体内变异为63.71%,为高变异药物,参考《高变异药物生物等效性研究技术指导原则》[3],考虑采用重复交叉生物等效性试验设计。同时根据预试验结果,活性代谢物替诺福韦的t1/2约为40 h,设计清洗期为10 d,若采用四周期完全重复设计,试验持续时间长,受试者脱落率高,故最终采用三周期部分重复交叉等效性试验设计。根据替诺福韦艾拉酚胺的最大个体内变异63.71%,受试制剂与参比制剂几何均值比87.04%,把握度80%,估算有效样本量为36例,考虑脱落率,设计样本量为42例,即空腹和餐后试验各42例。正式试验结果表明,两制剂在空腹及餐后状态下均具有生物等效性,且正式试验中受试制剂与参比制剂几何均值比均约为100%,明显优于预试验结果,其可能原因有:①正式试验采用三周期部分重复交叉等效性试验,减少由个体内变异带来的误差,试验结果更加准确;②正式试验受试者例数是预实验的3倍以上,其结果更具代表性;③正式试验可能在受试者招募及临床管理阶段要求更严格,其结果更具科学性。
3.4高变异药物生物等效性试验 当某药物的一个或多个药动学参数的个体内变异系数≥30%时,此药物称为高变异药物,而高变异药物的生物等效性研究一直是药学研究中的难题之一。若使用常规的数据分析方法与ABE评价标准,由于较大的个体内差异,极可能发生统计学错误,导致评价结果的假阴性。为解决这一难题,研究者们提出例如增加样本量、重复交叉设计和多剂量稳态评价、放宽等效性判断限值等解决办法[5]。国家药品监督管理局于2018年6月颁布《高变异药物生物等效性研究技术指导原则》,对高变异药物的生物等效性研究方法和评价方式提出明确要求[3],近年来,包括本试验在内的多个高变异药物生物等效性试验[6-8]均采用其推荐的重复交叉设计及RSABE评价标准,采用科学的方法最大程度地降低了生物等效性评价的偏倚。
表2 42例健康受试者空腹和餐后口服受试制剂与参比制剂后替诺福韦艾拉酚胺的药动学参数
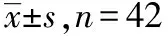
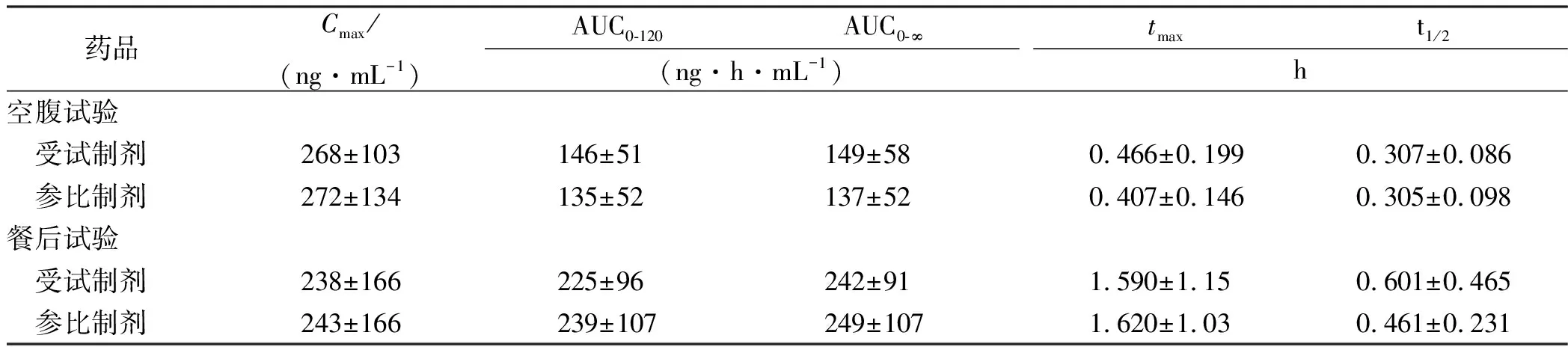
药品Cmax/(ng·mL-1)AUC0-120AUC0-∞(ng·h·mL-1)tmaxt1/2h空腹试验 受试制剂268±103 146±51 149±580.466±0.1990.307±0.086 参比制剂272±134 135±52 137±520.407±0.1460.305±0.098餐后试验 受试制剂238±166 225±96 242±911.590±1.150.601±0.465 参比制剂243±166 239±107 249±1071.620±1.030.461±0.231
表3 42例健康受试者空腹和餐后口服受试制剂与参比制剂后替诺福韦的药动学参数
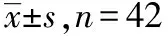
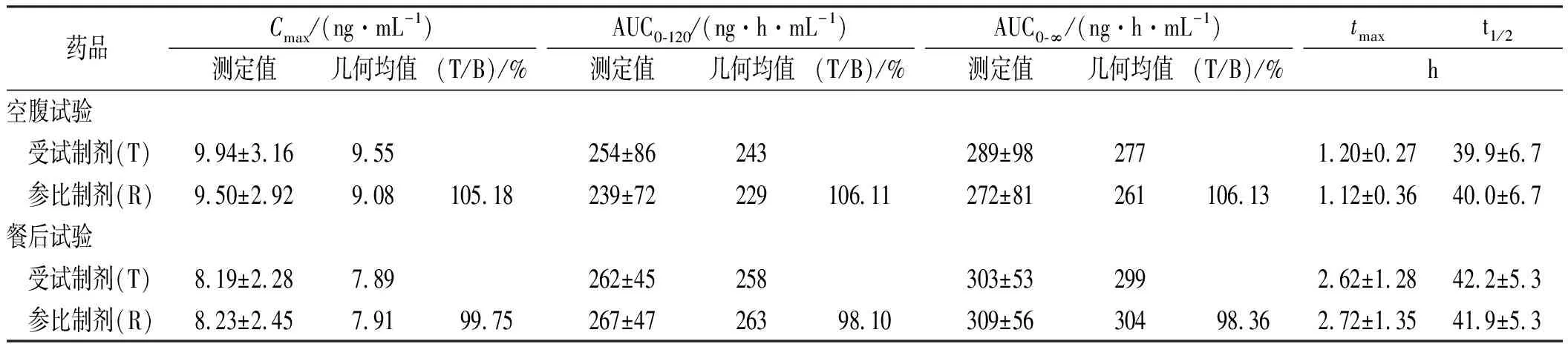
药品Cmax/(ng·mL-1)测定值几何均值(T/B)/%AUC0-120/(ng·h·mL-1)测定值几何均值(T/B)/%AUC0-∞/(ng·h·mL-1)测定值几何均值(T/B)/%tmaxt1/2h空腹试验 受试制剂(T)9.94±3.169.55254±86243289±982771.20±0.2739.9±6.7 参比制剂(R)9.50±2.929.08105.18239±72229106.11272±81261106.131.12±0.3640.0±6.7餐后试验 受试制剂(T)8.19±2.287.89262±45258303±532992.62±1.2842.2±5.3 参比制剂(R)8.23±2.457.9199.75267±4726398.10309±5630498.362.72±1.3541.9±5.3
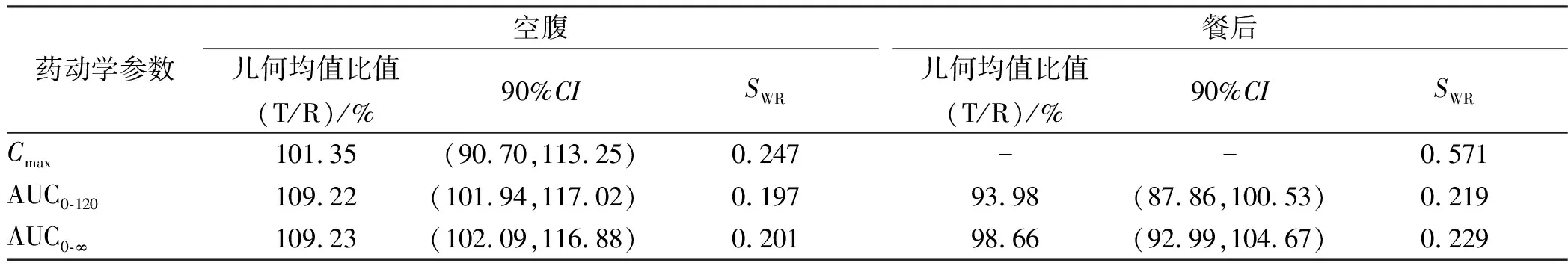
表4 替诺福韦艾拉酚胺的生物等效性结果
3.5饮食影响 本试验首次考察饮食对替诺福韦艾拉酚胺及其代谢物替诺福韦在健康中国人体内药动学特征的影响。与空腹给药比较,餐后给药替诺福韦艾拉酚胺药物暴露量AUC0-120增加77%,Cmax降低11.2%,且tmax推迟约1.2 h,说明饮食对替诺福韦艾拉酚胺的药动学存在明显影响,与国外文献[9-10]报道结果一致。同时,其活性代谢物替诺福韦在餐后状态下tmax推迟1.6 h,但其他药动学特征变化不明显。导致替诺福韦艾拉酚胺Cmax降低而AUC0-120增加的原因可能有以下几点:①进食后胃排空速度减慢[11],药物到达小肠被吸收需要更多时间,tmax推迟,Cmax降低;②进食高脂餐后,可促进胆汁分泌[11],胆汁中胆酸盐可增加亲脂性化合物的溶解度,使替诺福韦艾拉酚胺生物利用度提高。③食物的存在可能抑制替诺福韦艾拉酚胺的代谢,使得餐后AUC0-120增加。本试验的研究结果为富马酸替诺福韦艾拉酚胺片在中国人体内临床安全合理用药提供重要的参考依据。
