薏苡仁油致突变性实验研究
2020-06-17黄样增陈言枧吴长辉姚渭溪陈冠敏
黄样增,张 昆,陈言枧,吴长辉,姚渭溪,陈冠敏,李 晔
(1.福建仙芝楼生物科技有限公司 药用菌栽培与深加工国家地方联合工程研究中心,福州 350002;2.福建省疾病预防控制中心,福州 350001)
薏苡仁油是从禾本科植物薏苡(Coixlacryma-jobiL. var.ma-yuan(Roman.)Stapf)的干燥成熟种仁[1]中提取的,薏苡仁含有2%~8%的薏苡仁油。张栋霞[2]、谢春英[3]等发现薏苡仁油中的主要成分有薏苡内酯(又称薏苡素)、脂肪酸甘油酯、甾醇、角鲨烯及维生素E等,具有增强免疫力[4]和抗肿瘤[5]等作用,其应用前景十分广阔。但是,目前对于薏苡仁油的遗传毒性报道较少,缺乏相关研究数据。遗传毒性研究是非临床安全性评价的重要内容,包括致突变性、致癌性、致畸性。本试验按照《保健食品检验与评价技术规范》,通过对鼠伤寒沙门氏菌回复突变试验(Ames试验)、小鼠骨髓细胞微核试验和小鼠精子畸形试验对薏苡仁油的致突变性进行评价,以期为薏苡仁油的开发利用以及安全食用提供科学依据。
1 材料与方法
1.1 试验材料
1.1.1 试验样品
薏苡仁油软胶囊,薏苡仁按照《中国药典》检测合格后,采用图1生产工艺流程制备薏苡仁油(密度为0.87 g/L),直接经压丸后制得。药理取薏苡仁油软胶囊内容物,即薏苡仁油。
1.1.2 试验动物及饲养环境
选用上海斯莱克实验动物有限责任公司提供的清洁级健康ICR小鼠200只,体重25~30 g;清洁级SD大鼠80只,体重67~85 g,雌雄各半。许可证号为SCXK(沪)2012-0002。小鼠、大鼠饲养于福建省疾病预防控制中心SPF级动物实验室,许可证号为SYXK(闽)2012-0008。
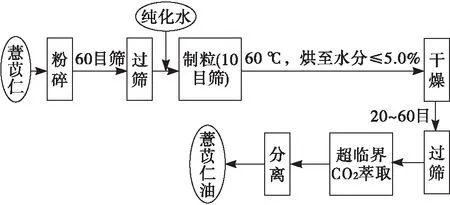
注:超临界CO2萃取条件为萃取压力25 MPa、萃取温度60℃、分离压力6.5 MPa、分离温度45℃、CO2流量100 L/h、萃取时间4 h。
图1 薏苡仁油生产工艺流程
1.1.3 菌株
鼠伤寒沙门氏组氨酸缺陷型菌株TA98、TA97、TA102和TA100,由福建省疾病预防控制中心赠送(购于复旦大学公共卫生学院),经鉴定符合要求后再进行试验。
1.1.4 仪器与试剂
电子天平,BSC-1360ⅡA2生物安全柜,SHP-250生化培养箱,DK-S28电热恒温水温箱,SS-325型自动高压灭菌器,自动菌落计数仪,Olympus CH显微镜。
丝裂霉素C(MMC),2,4,7-三硝基芴酮(2,4,7-TNFone),2-氨基芴(2-AF),1,8-二羟基蒽醌,三氮化钠(NaN3),二甲基亚砜(0.055 MPa,20 min灭菌),环磷酰胺(40 mg/kg),大豆油。
1.2 试验方法
1.2.1 鼠伤寒沙门氏菌回复突变试验(Ames试验)
釆用多氯联苯诱导的大鼠肝匀浆作为体外代谢活化系统。称取样品5.0 g加二甲基亚砜至100 mL作为高剂量受试物,量取高剂量受试物20 mL加二甲基亚砜至100 mL搅拌均匀作为次高剂量受试物,以下3个剂量如此类推配制,由高到低配成5 000、1 000、200、40、8 μg/皿5个剂量,经0.103 MPa、20 min灭菌,同时设自发回变组、阳性对照组和溶剂(二甲基亚砜)对照组,每个剂量设3个平皿。在顶层琼脂中加入0.1 mL受试物溶液、0.1 mL测试菌株增菌液和0.5 mL S-9混合液(当需要代谢活化时),混匀后倒入底层培养基平板上,于37℃培养48 h,计数每皿回变菌落数,试验重复1次。如果样品的回变菌落数是溶剂对照组回变菌落数2倍以上,并具有剂量反应关系则定为试验结果阳性。
1.2.2 小鼠骨髓细胞微核试验
选取50只体重25~30 g健康小鼠,雌雄各半,各性别小鼠随机按体重分成5组,每组5只。鉴于动物、人的种属和个体之间的生物学差异,安全系数通常为100,因此试验设3个剂量组为4.35、8.70、17.40 g/kg,相当于成人推荐量的130、261、522倍,另设阳性(环磷酰胺)对照组、溶剂(大豆油)对照组。分别称取样品2.5、5.0、10.0 mL各加大豆油至20 mL配成3个浓度,各组动物分别按体重0.02 mL/g间隔24 h灌胃给予不同浓度的受试物及对照物2次,末次灌胃6 h后脱颈椎处死动物,取胸骨骨髓用小牛血清稀释涂片,经甲醇固定,Giemsa染色。在光学显微镜下观察,每只动物计数1 000个嗜多染红细胞(PCE),微核发生率以含微核PCE率计,按χ2检验进行统计分析。同时计数200个PCE,求出 PCE(嗜多染红细胞)/NCE(正染红细胞)值。
1.2.3 小鼠精子畸形试验
选用体重25~30 g雄性性成熟小鼠25只,随机按体重分成5组,每组5只,试验设3个剂量组为4.35、8.70、17.40 g/kg,相当于成人推荐量的130、261、522倍,另设溶剂对照组和阳性对照组。分别称取样品2.5、50、10.0 mL各加大豆油至20 mL配成3个浓度,各组动物分别按0.02 mL/g灌胃给予不同浓度的受试物及对照物,连续5 d。于首次灌胃后35 d,处死动物,取双侧附睾尾按标准程序制片、染色,显微镜下每只动物观察1 000个完整精子,记录各类畸形精子数,计算精子畸形率,按χ2检验进行统计分析。
2 结果与分析
2.1 鼠伤寒沙门氏菌回复突变试验(Ames试验)(见表1、表2)
由表1、表2可见,阳性对照组菌株的回变菌落数均超过自发回变组和溶剂(二甲基亚砜)对照组2倍以上,而该样品受试物各剂量组的回变菌落数均未超过溶剂对照组回变菌落数的2倍。说明Ames试验结果为阴性。
2.2 小鼠骨髓细胞微核试验(见表3)
由表3可见,该样品各剂量组PCE(嗜多染红细胞)/NCE(正染红细胞)未少于溶剂对照组的20%,提示骨髓红细胞系统的增殖并无明显抑制,对嗜多染红细胞微核的观察无明显影响。阳性(环磷酰胺)对照组微核发生率明显高于溶剂对照组,差异有统计学意义(P<0.01),而样品各剂量组与溶剂对照组比较差异无统计学意义(P>0.05),说明该样品未表现出使小鼠骨髓PCE微核率上升的致突变效应。

表1 样品Ames试验结果(第一次)
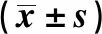
表2 样品Ames试验结果(第二次)
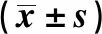
表3 样品小鼠骨髓细胞微核试验结果
注:*表示与溶剂对照组相比P<0.01。下同。
3.3 小鼠精子畸形试验(见表4)
由表4可见,阳性(环磷酰胺)对照组与溶剂(大豆油)对照组比较,差异有统计学意义(P<0.01),而样品各剂量组与溶剂对照组比较,差异无统计学意义(P>0.05),可见样品对小鼠精子畸形率未产生明显改变,提示该样品对小鼠精子不产生畸变作用。

表4 样品小鼠精子畸形试验结果
3 结 论
采用反映基因突变的Ames试验、反映染色体损害的小鼠骨髓细胞微核试验和反映生殖细胞突变的小鼠精子畸形试验研究薏苡仁油的致突变性。结果发现,薏苡仁油对小鼠骨髓细胞微核无明显增多作用,对雄性小鼠生殖细胞无遗传损伤作用,也不具有基因致突变作用。因此,在本试验条件下,薏苡仁油未显示有致突变性。试验表明薏苡仁油对人体无致突变作用。
