巨细胞病毒IgM抗体及巨细胞病毒DNA联合检测诊断婴幼儿巨细胞病毒肝炎的价值分析
2020-06-12毋乐乐
毋乐乐
焦作市妇幼保健院检验科,河南 焦作 454000
巨细胞病毒(CMV)又称人类疱疹病毒5型,可通过唾液、宫内、围生期与性接触传播,当机体发生原发性感染时后,CMV不能完全被宿主清除,而潜伏在宿主体内,可由多种情况引发感染而在活化[1]。婴幼儿因为免疫系统发育不完善与抵抗力较弱,容易感染CMV发展为巨细胞病毒肝炎(HCMV)。患儿感染HCMV无临床症状,且感染严重的情况下会损害多种脏器[2]。感染CMV的诊断主要依据实验室检查,包括血清特异性抗体检测、DNA的PCR技术检测、抗原血症、基因转录产物与病毒培养等,其中最常见的实验室检查是血清特异性抗体检测与PCR技术检测CMV-DNA。但抗原血症检测是巨细胞病毒感染早期的诊断指标。多形核白细胞中低基质的磷酸化蛋白抗原(pp65)是活动性感染的标志,CMV-pp65是CMV的被膜蛋白,其表达与病毒复制有关,但国内很少开展[3]。基于此,本研究旨在探讨CMV-IgM及CMV-DNA联合检测诊断婴幼儿巨细胞病毒肝炎的价值分析。现报告如下。
1 资料与方法
1.1 一般资料
回顾性研究2018年3月—2019年4月间焦作市妇幼保健院收治的200例婴幼儿巨细胞病毒肝炎患儿的临床资料作为观察组,同期选择100例无感染症状健康婴幼儿作为对照组。观察组中男120例,女80例;年龄1~3岁,平均年龄(1.66±0.22)岁。对照组中男55例,女45例;年龄1~3岁,平均年龄(1.68±0.13)岁。比较两组一般资料,差异无统计学意义(P>0.05),具有可比性。此次研究已正式通过医院医学伦理委员会的审核,所有患儿及其家属均知情且签署了知情同意书。
1.2 入选标准
纳入标准:(1)观察组经单克隆抗体检查病毒抗原检查确诊为巨细胞病毒肝炎者;(2)临床资料、影像学资料均完整者;(3)凝血功能正常者。排除标准:(1)严重器官功能衰竭者;(2)感染单纯疱疹病毒者;(3)合并其他原因引起的肝炎者。
1.3 方法
标本采集处理:静脉采集患儿的清晨空腹血3 ml,置于促凝管中,然后静置离心,取上层血清分别检测CMV-IgM、CMV-DNA。CMV-IgM检测:用化学发光仪及其配套试剂(美国雅培公司)检测CMV-IgM;CMV-DNA检测:用ABI stepone Plus仪(中山大学达安基股份有限公司),荧光定量PCR技术检测CMV-DNA。
1.4 评价指标
CMV-IgM>22 U/ml为阳性,≤22 U/ml为阴性;CMV-DNA≥2000 IU/ml为阳性,CMV-DNA<2000 IU/ml为阴性。
1.5 统计学方法
数据采用SPSS 24.0软件进行统计分析,全部计量资料均经正态检验,均符合正态分布,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料用例数和百分比(%)表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 不同检测方法检测结果比较
观察组患儿CMV-IgM、CMV-DNA的检测结果均显著高于对照组,差异有统计学意义(P<0.05),见表1。
表1 不同检测方法检测结果比较(±s)
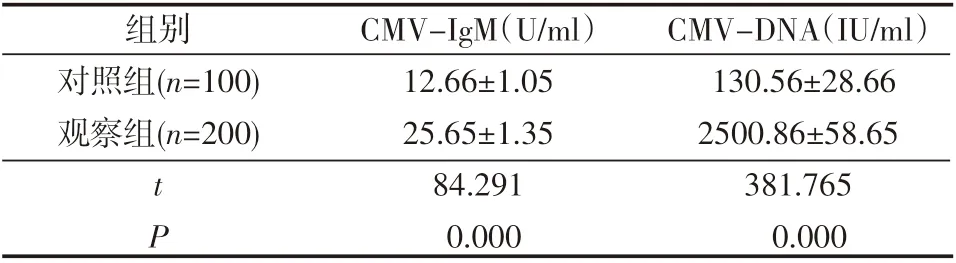
表1 不同检测方法检测结果比较(±s)
组别对照组(n=100)观察组(n=200)tP CMV-IgM(U/ml)12.66±1.05 25.65±1.35 84.291 0.000 CMV-DNA(IU/ml)130.56±28.66 2500.86±58.65 381.765 0.000
2.2 不同检测方法阳性率比较
观察组患儿CMV-IgM阳性率、CMV-DNA阳性率、联合检测阳性率均显著高于对照组,且联合检测阳性率均高于CMV-IgM阳性率、CMV-DNA阳性率,差异有统计学意义(P<0.05),见表2。
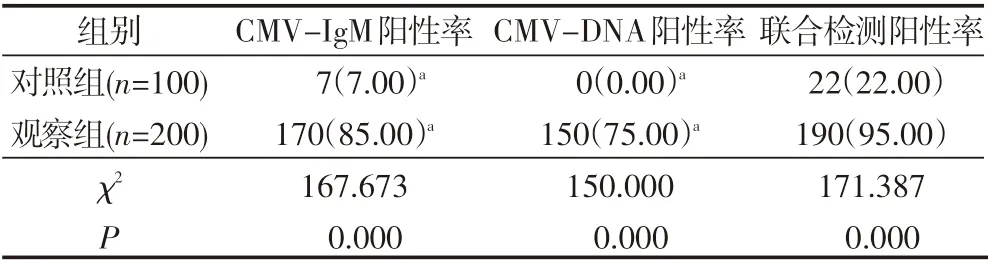
表2 不同检测方法检测阳性率比较 例(%)
3 讨论
婴幼儿感染病毒性肝炎的病原体有很多,包括:CMV、单纯疱疹病毒、乙型肝炎病毒与柯萨奇病毒等,因此准确诊断感染何种病原体与有效的治疗是关键。婴幼儿感染CMV和传播的途径有母乳、胎盘、产道等,且可分为:先天性感染、获得性感染与围生期感染[4-5]。CMV-pp65抗原是CMV活动性感染的主要蛋白,具有敏感度好与特异度高的优点,是早期快速的诊断指标,是国际公认的检测CMV活性感染的方法,因此可以作为诊断CMV感染的金标准[6]。但是,目前对于HCMV的诊断主要依据CMV-IgM检测与CMV-DNA检测。
血清特异性抗体检测是用于诊断HCMV最常用的方法。当患儿感染CMV后,机体产生一些特异性抗体如CMV-IgM、CMV-IgE、CMV-IgG,因此检测患儿血清中的抗体可证实患儿机体感染了CMV。患儿检测出IgM抗体阳性,表示感染CMV,但是其阳性率较低,因为IgM抗体在感染CMV后的2~4周才能被检测发现,又受患儿免疫力低下的影响,会出现假阴性的结果。人CMV-IgM与CMV-DNA无关,表示CMV-IgM与病毒的复制无关[7]。实验室检测CMV是最主要的方法,其中用化学发光法检测CMV-IgM具有一定的优势,与传统酶联免疫吸附法比较,化学发光法速度快、自动化好、敏感度与特异度高,且检测结果更可靠。荧光定量PCR技术通过在反应体系中加入荧光基团,用荧光信号检测PCR的进程,可以定量分析未知模板。荧光定量PCR技术检测CMV-DNA对诊断CMV具有很好的诊断价值,但也存在一定的问题,主要是DNA抽提、PCR反应条件与检测位点的选择等方面存在差异,影响检测结果,且定性PCR会出现假阳性结果,不能准确的判断是否感染CMV[8]。本研究结果显示,观察组患儿CMV-IgM、CMV-DNA的检测结果均显著高于对照组;观察组患儿CMV-IgM阳性率、CMV-DNA阳性率、联合检测阳性率均显著高于对照组,且联合检测阳性率均高于CMV-IgM阳性率、CMV-DNA阳性率。提示联合检测CMV-IgM及CMV-DNA,对诊断婴幼儿巨细胞病毒肝炎具有重要意义,可提高检测阳性率。
综上所述,CMV-IgM及CMV-DNA联合检测对婴幼儿巨细胞病毒肝炎具有诊断意义,可提高检测阳性率,对婴幼儿巨细胞病毒肝炎的早期诊断、治疗、预防并发症的发生具有重要意义,值得在临床广泛推广应用。
