非小细胞肺癌分子基因方面研究
2020-06-10张银马维郭婵娟
张银,马维,郭婵娟
云南省红河州第三人民医院病理科,云南红河 661000
肺癌是一种十分常见的临床恶性肿瘤疾病之一,通过查阅相关的临床资料可知, 非小细胞肺癌的患者数量约占整个肺癌患者的80%~85%[1]。伴随着手术与放化疗技术的不断改进,虽然患者获得了良好的治疗,但患者的5年生存率仍然较低[2]。 随着病程的发展,诸多患者将发生EGFR 基因突变的情况,对自身的健康造成造成极为负面的损伤, 有效地给予准确检测是进行针对性治疗的根本和基础[3],伴随着研究的深入,临床中目前以EGFR 为靶点的分子靶向治疗成为新型的治疗目标, 通过相关的临床研究可知[4],EGFR-TKI 靶向治疗EGFR 体细胞突变患者具有良好的效果。 该研究选取该院收治的92 例非小细胞肺癌患者, 研究时间段为2017年3 月—2018年4 月,将探讨非小细胞肺癌分子基因方面研究的临床意义, 为日后的深入研究提供一定的借鉴,现报道如下。
1 资料与方法
1.1 一般资料
选取该院收治的92 例非小细胞肺癌患者, 男58 例,女34 例,年龄为42~83 岁,平均年龄为(62.5±4.9)岁。
1.2 纳入标准
①均符合非小细胞肺癌的临床诊断标准; ②患者均自愿参加且获得家属的同意; ③患者及其家属知晓了该次实验研究的全部内容并签署了知情同意书; ④该次实验研究经过了医学伦理委员会的批准认可。
1.3 排除标准
①无法积极配合完成检测;②患有其他恶性肿瘤疾病。
1.4 方法
EGFR 基因检测。ADx-ARMSTMEGFR 基因突变检测试剂盒对患者组织中EGFR 基因外显子18、19、20 与21 突变情况进行检测。具体方式如下:①选用ADx-ARMS EGFR基因突变检测试剂盒进行检测。 ②检测方式。 依据患者的肿瘤细胞含量及组织大小,使用石蜡切片进行剔除,然后使用二甲苯进行脱蜡处理,刮取玻片组织后将其放置Eppendorl 管中,震荡混匀,在室温下静置10 min,之后进行约5 min 的离心处理,去除上清液后予以乙醇洗脱,之后再次进行离心与洗脱处理, 依据基因组DNA 提取试剂盒的相关标准提取基因组DNA。 选用ABI7500Real Time PCR System 扩增仪, 将ADx-ARMS EGFR 基因突变检测试剂盒通过荧光PCR 法进行EGFR 基因的突变检测。
对患者进行EGFR-TKI 靶向治疗。 依据基因突变情况将其分为突变组与非突变组, 均对其予以EGFR-TKI靶向治疗, 使患者服用盐酸厄洛替尼片 (注册证号H20090225,F.Hoffmann-La Roche Ltd.150 mg)与吉非替尼片(国药准字H20163465,0.25 g),盐酸厄洛替尼片的剂量为1 次/d,150 mg/次;吉非替尼片的剂量为1 次/d,250 mg/次,两种药物连续使用2 个月。
1.5 观察指标
①患者的EGFR 基因检测情况。
②两组患者的临床治疗效果情况,评价标准:患者的肺部肿瘤体积明显缩小, 患者的大部分指标均恢复到正常范围内为显效; 肺部肿瘤体积的缩小幅度在20%~40%, 指标均有所改善但未恢复到正常范围值内为有效;肺部肿瘤体积无改变甚至继续增大,指标未有改善为无效。
1.6 统计方法
使用SPSS 20.0 统计学软件对数据进行分析, 计数资料以频数和百分比(%)表示,采用χ2检验,P<0.05 差异有统计学意义。
2 结果
2.1 患者的EGFR 基因检测情况
经临床检测可知,在92 例患者中,共有45 例患者的EGFR 基因发生突变,突变率为48.91%;47 例患者未发生基因突变,占比51.09%。 在EGFR 基因发生突变患者中,19 号外显子缺失突变率占首位。
2.2 患者的临床治疗效果情况
突变组的治疗总有效率明显较高, 与非突变组相比差异有统计学意义(P<0.05),见表1。
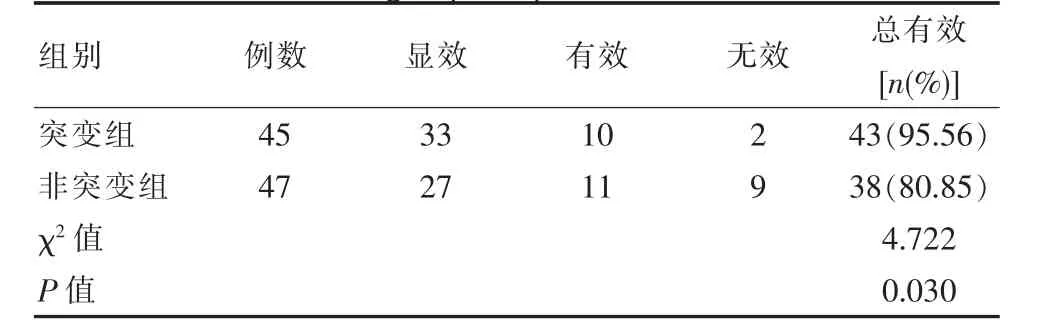
表2 两组患者的临床治疗效果情况比较Table 2 Comparison of clinical treatment effect between two groups of patients
3 讨论
随着生活方式的不断变化与环境的不断变化, 近年来肺癌的发病率不断增加,并且多呈年轻化趋势,通过查阅相关的临床研究显示[5],肺癌是广大人民群众生命的重要威胁。 非小细胞肺癌是一种常见肺癌疾病,通过相关的临床报道可知,非小细胞肺癌约占整个肺癌患者的80%,同时随着病程的不断发展, 诸多患者将会出现基因突变现象。 作为跨膜受体型酪氨酸激酶,EGFR 在NSCLC 中存在过表达或发生突变的现象, 将会对患者造成更加严重的不良影响。 随着我们国家医学技术的不断发展,以及检测技术的不断完善, 突变扩增组织系统已经成为了临床检验当中的重要检验方法, 这种检验方法可以有效地对患者的肿瘤个体化分子进行检测。 这种检测方法目前已经得到了国内外医学界的普遍认可[6]。 这种检测方法的原理为利用特异引物对患者的突变靶序列进行扩增放大,然后进行检测, 这种检测方法的检测灵敏度明显高于其他方式。 NSCLC 中最为常见的组织类型为腺癌,在该研究中, 共有45 例患者的EGFR 基因发生突变, 突变率为48.91%,这是由于ARMS 检测技术具有跟高的灵敏性,从而增加检出率[7]。
在临床研究中[8],EGFR 基因共包括28 个外显子,其中编码酪氨酸激酶区的是第18~21 外显子, 依据相关的临床研究显示,19 号外显子缺失突变、20 号外显子T790M 插入突变、21 外显子的L858R 突变是最常见的突变类型是临床中较为常见的基因突变类型, 该研究的研究结果与其相似,其主要原因在于19 外显子与21 外显子交易受到环境致癌物的攻击的不良影响, 当其发生突变之后将会对EGFR 的信号转导通路进行激活, 对于NSCLC 的发生与发展具有重要的参与作用。
所谓的EGFR-TKI 即为表皮生长因子受体酪氨酸激酶抑制剂, 是目前临床中一种新型的对于肺癌的靶向治疗技术, 与其他的治疗技术相比,EGFR-TKI 具有服用方法简单、耐受性高、安全性高、有效性高等特点,因而被广泛应用于临床治疗中。 但近年来通过相关专家的研究显示[8],非小细胞肺癌患者在应用TKI 类药物进行治疗时,其敏感性相对偏低。 因此,在进行治疗前对患者的进行是否存在EGFR 基因突变现象已成为非小细胞肺癌患者治疗方案选择的重要依据。 依据该项研究结果显示,相对于非存在基因突变的患者,EGFR-TKI 对于基因突变患者的治疗效果更佳, 总有效率高达95.56%, 主要原因在于EGFR-TKI 对于突变的EGFR 基因具有更高的敏感性,因而能够使患者获得更佳的治疗效果。
综上所述,该研究认为非小细胞肺癌患者的EGFR 基因突变率较高, 经治疗后能够获得良好的效果, 可将EGFR 基因作为靶向治疗的靶点。但临床检测人员仍然需要加强研究,以便能够获得更加准确的检测结果。
