氯胺酮单次注射对创伤后应激障碍模型动物场景恐惧行为的影响及机制
2020-06-09魏肇余李光香张雯雯王洛萱李云峰张有志王恒林
魏肇余,薛 瑞,李光香,张雯雯,王洛萱,李云峰,张有志,王恒林
(1.河北北方学院研究生院,河北 张家口 075000;2.解放军总医院第八医学中心麻醉科,北京 100091;3.军事科学院军事医学研究院毒物药物研究所,抗毒药物与毒理学国家重点实验室,北京 100850)
创伤后应激障碍(post-traumatic stress disorder,PTSD)是指个体在经历重大创伤事件,如战争、重大灾害(地震、交通事故等)或性侵害之后所表现出的迟发性慢性精神疾病,主要特征包括持续生动的创伤事件重现、创伤相关线索逃避、反应过度和认知与情感的负性改变[1-2]。PTSD与抑郁症和焦虑症具有高达50%的共患病比率。PTSD病因虽较明确,但病理生理机制复杂,尚未完全阐明,可能与神经递质失衡、以下丘脑-垂体-肾上腺(hypothalamicpituitary-adrenal,HPA)轴为主体的神经内分泌系统紊乱、神经免疫炎症、脑解剖结构和神经可塑性改变等多种因素密切相关[3-6]。心理疗法和药物干预是PTSD治疗最常规的2种方式,目前获美国FDA批准用于临床PTSD患者治疗的药物只有舍曲林(sertraline)和帕罗西汀(paroxetine),它们都是选择性5-羟色胺重摄取抑制剂,是治疗PTSD的首选药物[7-8]。遗憾的是,选择性5-羟色胺重摄取抑制剂治疗效果并不尽如人意,且存在起效延迟以及导致性功能障碍、认知功能损伤、自杀倾向等多种不良反应[9-11]。因此,深入研究PTSD的发病机制,研发具有强效速效抗PTSD作用的药物具有重要意义。
氯胺酮是一种非竞争性N-甲基-D-天冬氨酸(N-methyl-D-aspartic acid,NMDA)受体拮抗剂,临床上作为分离性麻醉剂使用。自2000年BERMAN等首次报道氯胺酮具有抗抑郁作用以来,越来越多临床证据表明,氯胺酮可发挥快速而持久的抗抑郁作用,且对难治性抑郁亦有效,引起了人们对氯胺酮在精神疾病中应用价值的高度兴趣和广泛关注[12-13]。2008年,MCGHEE等[14]研究表明,手术期间使用氯胺酮作为镇痛药的烧伤患者术后PTSD发生率显著低于未使用氯胺酮干预组;然而2014年,该作者对大样本临床数据进行分析,发现术中氯胺酮干预对术后烧伤患者的PTSD发展并无显著影响,即并未降低PTSD的发生率[15]。同年,FEDER等[16]报道,亚麻醉剂量的氯胺酮单次给药对慢性PTSD患者具有快速治疗作用。由此可见,氯胺酮对PTSD是否具有治疗作用并未取得一致性结论,需要进一步进行深入研究,明确氯胺酮对PTSD的影响可能为PTSD的治疗提供有效且快速的干预手段。
本研究采用小鼠条件性恐惧模型[17-18]和大鼠时间依赖敏化模型(time-dependent sensitization,TDS)模型[19]评价氯胺酮不同时间点单次预防给药对PTSD模型动物场景恐惧行为的影响,并采用Western印迹法评价调节脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)表达是否是氯胺酮防治PTSD的作用机制。
1 材料与方法
1.1 试剂和主要仪器
氯胺酮(军事医学研究院毒物药物研究所合成,纯度>99.00%)。氯化钠注射液(石家庄四药有限公司);兔抗小鼠BDNF单克隆抗体(ab108319)(美国Abcam公司);小鼠抗人β肌动蛋白单克隆抗体(sc-47778)(美国Santa Cruz Biotechnology公司)。自制麻醉用玻璃缸(20 cm×22 cm);自制游泳用玻璃缸(20 cm×41 cm);Video Freeze SOF-843条件性恐惧系统(美国Med Associates公司);Milli-Q纯水仪(美国Millipore公司);TDL-40B台式离心机(上海安亭科学仪器厂);蛋白电泳仪和蛋白电子转膜仪(美国Bio-Rad公司);EnVision多标记微孔板检测仪(美国PE公司)。
1.2 动物
100只SPF级C57小鼠,雄性,体质量18~20 g,购自斯贝福(北京)实验动物科技有限公司,合格证号:SCXK(京)2016-0002。32只SPF级SD大鼠,雄性,体质量260~270 g,购自斯贝福(北京)实验动物科技有限公司,合格证号:SCXK(京)2016-0002。饲养环境温度21~24℃,湿度40%~70%,12 h昼夜明暗交替(8∶00 Am-8∶00 Pm),自由进食饮水,适应性饲养7 d,每天抓取3 min,然后开始行为学测试,实验前1 h将小鼠或大鼠放进实验间内适应环境。
1.3 小鼠条件性恐惧实验
1.3.1 小鼠条件性恐惧模型的制备和场景恐惧行为测试
将小鼠放入电击箱中适应2 min后,给予声音刺激30 s(85 dB),最后2 s伴随给予0.6 mA足底电击,间隔2 min开始下一轮声音和电击,共进行5轮。
分别于造模后24 h进行5 min的场景恐惧测试,Video Freeze SOF-843软件自动记录5 min内的僵住时间,计算僵住时间百分率,僵住时间百分率(%)=僵住时间(s)/总时间(s)×100%。僵住行为定义为除呼吸运动外全身其余的肌肉运动均消失的一种刻板行为,是啮齿动物表达恐惧的方式。
1.3.2 不同时间点单次预防性给予氯胺酮对场景恐惧表达的影响
小鼠分为模型组和模型+不同时间氯胺酮组,分别于条件性恐惧造模前第7天、24 h和0.5 h单次ip给予生理盐水或氯胺酮10 mg∙kg-1,各组小鼠按1.3.1方法制备条件性恐惧模型,并于造模后24 h场景恐惧测试。实验流程见图1A。
1.3.3 氯胺酮对小鼠场景恐惧量效和起效时间行为测试
小鼠分为模型组和模型+不同剂量氯胺酮组,分别在造模前0.5 h单次ip给予生理盐水、氯胺酮3和10 mg∙kg-1。各组小鼠按1.3.1方法制备条件性恐惧模型,并于造模后24 h、第7天和第14天进行场景恐惧测试。实验流程见图1B。
1.3.4 Western印迹法检测条件性恐惧模型小鼠大脑皮质区BDNF蛋白表达水平
小鼠分为模型组和模型+氯胺酮组,分别在造模前0.5 h单次ip给予生理盐水或氯胺酮10 mg∙kg-1。各组小鼠按1.3.1方法制备条件性恐惧模型。同时取正常小鼠10只,放入电击箱中同样时间但不进行电击(正常对照组)。分别在造模训练后24 h、第14天场景恐惧表达测试后将小鼠处死,冰上取脑,分离皮质组织,-80℃冰箱中备用。
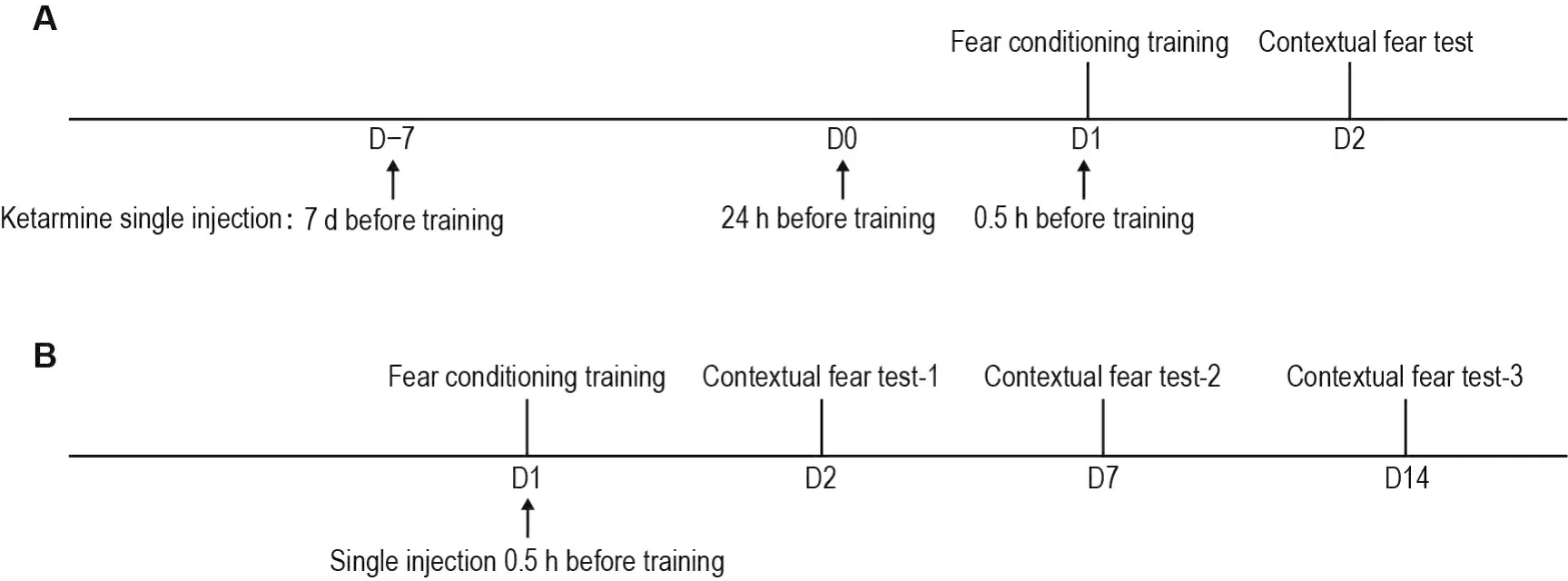
Fig.1 Fear conditioning regime in mice.A was the study on time point of drug treatment:ketamine 10 mg∙kg-1was ip injected 7 d,24 h or 0.5 h before fear conditioning training(D-7,D0,D1),and contextual fear expression test was performed 24 h later(D2).The percentage of freezing time in mice was calculated in 5 min test period.B was the study on dose-response and onset time of drug treatment:ketamine at 3 or 10 mg∙kg-1was ip given 0.5 h before fear conditioning training,and contextual fear expression test was performed in D2(24 h later),D7 and D14 after fear conditioning training.The percentage of freezing time in mice was calculated in 5 min test period.
皮质组织称重,并按10 mg/100 μL比例加入含蛋白酶抑制剂和蛋白磷酸酶抑制剂的预冷RIPA裂解缓冲液,并以BCA法蛋白定量。常规配置12%SDS-PAGE凝胶和5%基层胶,每孔上样30 μg,蛋白经电泳分离后恒压转印至PDVF膜。10%脱脂牛奶封闭2 h,之后加BDNF(1∶1000)和β肌动蛋白(1∶5000)一抗,4℃冰箱摇床孵育过夜,室温下二抗(1∶10 000)孵育2 h。在凝胶成像系统(Fluor Chem TMFC2)清晰显影记录图像。实验结果以目的蛋白与内参蛋白条带积分吸光度的比值表示目的蛋白的相对表达水平。
1.4 大鼠TDS实验
1.4.1 大鼠分组和TDS模型制备
大鼠分为模型组和模型+氯胺酮组,分别在条件性恐惧训练前第14天、24 h和0.5 h分别单次ip给予生理盐水或氯胺酮10 mg∙kg-1。TDS模型制备包括4步:①束缚:将动物固定于干净的聚丙烯啮齿动物限制锥里2 h。②游泳:动物束缚结束后立即放入游泳缸内游泳20 min,水温22~24℃,水深15 cm。③麻醉:游泳恢复15 min后,将大鼠放入充满乙醚的麻醉缸内,直至其翻正反射消失后取出,待大鼠恢复清醒后放回饲养间。④游泳(再次应激):造模后第7天,将动物重新放入游泳缸中进行20 min强迫游泳,结束后将动物放回饲养间饲养(图2)。
1.4.2 大鼠条件性恐惧训练和场景恐惧检测
TDS模型制备结束后第7天,进行条件性恐惧训练。将大鼠置电击箱中适应2 min,给予声音刺激20 s(85 dB),并在声音刺激的最后2 s伴随给予不可逃避的足底电击(0.7 mA,持续2 s),声音-电击配对共5次,间隔2 min。24 h后将大鼠再次置于接受过电击的装置中进行环境重现,但不给于任何刺激。场景恐惧检测持续5 min,每隔6 s观察一次,记录大鼠出现僵住行为的次数,计算僵住次数百分率(即僵住次数/观察次数×100%),评价氯胺酮对TDS大鼠场景条件恐惧表达的影响。
1.5 统计学分析
采用GraphPad Prism 8.0软件统计分析,实验结果以±s表示。除小鼠不同时间点单次预防给药对恐惧记忆表达影响的数据进行重复测量的单因素方差分析,其他数据采用单因素方差分析进行分析,post-hoc test采用Dunnettttest。P<0.05为差异具有统计学意义。

Fig.2 Establishment of time-dependent sensitization(TDS)model and contextual fear test in rats.Ketamine 10 mg∙kg-1 was ip injected to TDS rats 0.5 h,24 h and 14 d before fear conditioning training,and contextual fear expression test was performed 24 h after training.The percentage of freezing time in rats was calculated in 5 min test period.
2 结果
2.1 不同时间单次预防性给予氯胺酮对场景恐惧表达的影响
分别于条件性恐惧训练前第7天、24 h和0.5 h,单次ip氯胺酮10 mg∙kg-1,24 h后进行5 min场景恐惧测试,结果见图3。与模型对照组相比,氯胺酮第7天、24 h和0.5 h组僵住时间百分率均无显著差异,提示氯胺酮10 mg∙kg-1在这3个时间点单次预防给药对24 h场景恐惧表达无影响。

Fig.3 Effect of single prophylactic administration of ketamine on contextual fear behavior in mice.See Fig.1A for the mouse treatment.±s,n=9-11.
2.2 氯胺酮单次预防性给药对小鼠场景恐惧的量效和起效时程的影响
于条件性恐惧训练前0.5 h单次ip氯胺酮3或10 mg∙kg-1,分别于训练后24 h、第7天和第14天进行5 min场景恐惧测试(图4)。与模型对照组相比,仅训练后第14天氯胺酮10 mg·kg-1组显著降低小鼠僵住时间百分率(P<0.05),提示氯胺酮对小鼠场景恐惧表达有抑制作用,且该抑制作用具有延迟出现的特点。
2.3 氯胺酮单次预防性给药对TDS增敏的大鼠场景恐惧的影响
分别于TDS大鼠场景恐惧训练前第14天、24 h和0.5 h单次ip氯胺酮10 mg∙kg-1,训练24 h后进行5 min场景恐惧检测(图5)。与模型对照组相比,仅训练前0.5 h氯胺酮组可显著降低大鼠僵住次数百分率(P<0.05),提示其对TDS大鼠场景恐惧表达有抑制作用。
2.4 氯胺酮单次预防性给药对条件性恐惧模型小鼠大脑皮质区BDNF水平的影响
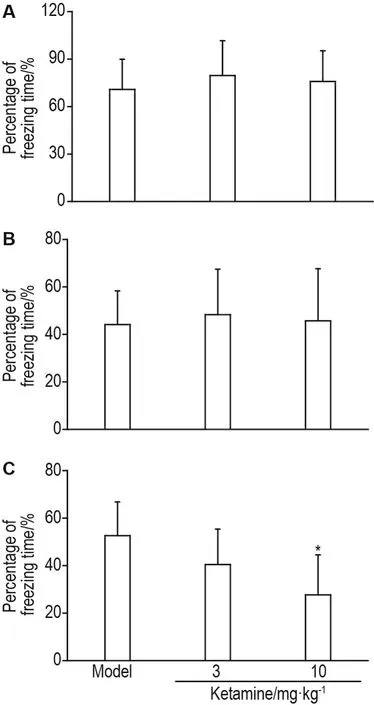
Fig.4 Effect of single prophylactic administration of ketamine on contextual fear behavior in mice.See Fig.1B for the mouse treatment.A-C was the result of contextual fear test at 24 h,the 7thand 14thday after training,respectively.±s,n=10-11. *P<0.05,compared with model group.
训练后24 h和第14天,与正常对照组比较,条件性恐惧模型组小鼠皮质BDNF含量均显著降低(P<0.01,P<0.05);氯胺酮10 mg∙kg-1组在上述时间点均逆转条件性恐惧造模所致的皮质BDNF降低,与模型组相比具有显著性差异(P<0.05,P<0.01)(图6)。

Fig.5 Effect of single prophylactic administration of ketamine on contextual fear behavior in time-dependent sensitized stress(TDS)rats.See Fig.2 for the rat treatment.±s,n=8-9.*P<0.05,compared with model group.

Fig.6 Effect of single prophylactic administration of ketamine on cortex brain-derived neurotrophic factor(BDNF)expression in mouse contextual fear model by Western blotting.Ketamine 10 mg∙kg-1was ip given 0.5 h before fear conditioning training,and BDNF protein expression was detected following contextual fear expression test in D2(A and C)and D14(B and D),respectively.C and D was the semiquantitative result of A and B,respectively.±s,n=9-12.*P<0.05,**P<0.01,compared with controlgroup; #P<0.05,##P<0.01,compared with model group.
3 讨论
条件性恐惧模型利用巴甫洛夫条件反射原理,将厌恶性刺激(如电击)与中性刺激(如训练场景)多次配对训练后建立,模型动物在重新暴露于原训练环境时会对该环境产生条件性恐惧反应,即场景恐惧[20-22]。条件性恐惧模型被认为是研究PTSD机制和评价药物作用的重要模型,特别是对于恐惧记忆的获得、提取和消退等阶段的研究具有重要价值[23-24]。本研究采用小鼠条件性恐惧模型对氯胺酮单次预防给药的作用进行研究。本研究结果表明,氯胺酮10 mg∙kg-1单次预防给药,在训练后第14天(而非训练后第2天)显著减轻模型小鼠的场景恐惧,且3 mg∙kg-1预防性给药无此作用,提示氯胺酮抑制小鼠场景恐惧表达的作用与剂量有关,且具有延迟出现的特点。MCGOWAN等[17]研究亦表明,在训练前1周单次预防性给予氯胺酮30 mg∙kg-1可降低场景恐惧的表达,但训练前在1个月或1 h单次给予氯胺酮30 mg∙kg-1,并不会影响恐惧的表达。由此进一步验证了氯胺酮对恐惧的表达是具有抑制作用,该作用依赖于给药时间点、药物剂量以及起效时程。
此外,本研究建立了大鼠TDS模型,并在该模型上评价了氯胺酮对PTSD增敏的恐惧行为的影响。单一连续刺激(single prolonged stress,SPS)模型依次经过2 h的束缚、20 min的游泳和乙醚麻醉3种刺激模拟动物心理、生理和内分泌方面的应激,模型动物对条件性恐惧的僵住反应增强,呈现恐惧增敏,与文献[25-26]报道的PTSD患者症状一致。大鼠TDS模型是在SPS模型的基础上进行进一步强化刺激,在SPS模型建立7 d后进行短暂的再次刺激(20 min强迫游泳),再经过7 d后进行相关行为学测试[18]。TDS模型可模拟PTSD患者在经历与创伤无关刺激时导致的焦虑和恐惧增加的现象,不同实验室已证明TDS模型具有很好的表观效度、结构效度和预测效度,且TDS模型动物行为学缺陷的出现需要1~2周的潜伏期,与临床PTSD症状的延迟出现具有良好的一致性[27-30]。本研究结果发现,TDS模型大鼠在条件性恐惧训练前不同时间点单次预防性给予氯胺酮10 mg∙kg-1,只有在恐惧训练前0.5 h给药时可显著抑制场景恐惧的表达,提示氯胺酮对于TDS增敏的场景恐惧表达具有快速干预作用,此作用同样依赖于给药时间点。然而值得注意的是,氯胺酮单次给药在大鼠TDS模型中呈现速效抑制恐惧表达的作用,而其在小鼠条件性恐惧模型中却具有延迟起效特点,二者的不一致性可能与动物种属和造模方式的不同有关。TAKAHASHI等[18]研究亦发现,在大鼠条件性恐惧模型中,场景恐惧训练后SPS模型大鼠与正常大鼠相比呈现恐惧增敏反应,表现为僵住时间的进一步延长;而5-羟色胺重摄取抑制剂帕罗西汀长期给药仅对SPS增敏的场景恐惧表达有抑制作用,对正常大鼠条件性恐惧表达无影响,这与本研究结果一致。
近年来,人们对氯胺酮的作用机制研究具有突破性的进展。传统观念认为,氯胺酮发挥速效抗抑郁作用主要与其拮抗NMDA受体有关,而新近观点认为,氯胺酮是通过抑制中间神经元NMDA受体,进而激活α-氨基-3-羟基-5-甲基-4-异噁哑唑丙酸受体,引起BDNF表达升高或快速释放,进而激活哺乳动物雷帕霉素靶蛋白受体有关。此外,氯胺酮与单胺再摄取转运蛋白、5-羟色胺受体、多巴胺能受体和阿片类受体等多种蛋白和受体系统具有相互作用,其抗抑郁作用机制仍在深入研究中[31-32]。目前,氯胺酮抗PTSD的作用机制并未达成共识,但也有零星报道,如张黎明等[19]发现,小剂量慢性给予氯胺酮的抗PTSD作用与升高BDNF含量有关。另有研究表明,氯胺酮可通过激活内侧前额叶皮质中哺乳动物雷帕霉素靶蛋白信号通路增强恐惧记忆的消退作用等[33-34]。本研究发现,氯胺酮在小鼠条件性恐惧模型中单次预防给药对恐惧记忆表达具有抑制作用,但该作用在训练后第14天才显现,提示其具有延迟起效的特点。随后采用Western印迹法分别检测了训练后24 h和第14天小鼠皮质内BDNF表达。结果发现,在上述2个时间点,与对照组相比,模型组BDNF水平均显著降低,提示恐惧发生可能与BDNF表达降低有关;然而,与模型组相比,在上述2个时间点氯胺酮组BDNF表达均显著升高,与其抑制恐惧表达作用的起效时间(训练后第14天)不一致,提示BDNF表达增加可能与氯胺酮抑制恐惧表达作用无关。
本研究发现,氯胺酮单次给药对恐惧记忆表达可能有预防作用,该作用与剂量和时间(给药时间点和时间窗)密切相关。此外,单次给予氯胺酮抗PTSD延迟起效的特点与恐惧记忆形成后BDNF含量的改变在时间上不具有一致性,提示单次给予氯胺酮的抗PTSD作用可能与调节BDNF表达无关。本研究为氯胺酮预防PTSD恐惧记忆的表达提供了实验依据,但其具体机制有待进一步研究。
