R 氯胺酮国内外药品研究资料文献综述
2020-06-22相晓伟
相晓伟
(江苏恒瑞医药股份有限公司,江苏 连云港222047)
氯胺酮是苯环利定类药物,于1962 年由Stevens 合成,1965年由Corssen 和Domino 首次在人体应用,1970 年投入临床,至今仍在临床中广泛应用[1]。
氯胺酮是由S 和R 异构体组成的消旋混合物,2000 年科学家意外发现氯胺酮可在2 小时内发挥抗抑郁尤其是重度抑郁和遏制自杀意念的作用,成为近60 年来抗抑郁领域最为突破性的发现,在此之前所有抗抑郁药都需要治疗数周之后方能起效。科学界对于氯胺酮作用机制的探究一直如火如荼地在进行,不断有新的机理被发现,包括代谢产物在内的一系列结构或机制相似的化合物陆续进入药物筛选序列;2019 年3 月5 日S 氯胺酮鼻喷剂作为全球唯一可以快速起效的抗抑郁药在美国获批上市。R 氯胺酮在动物试验中证实起效速度不亚于S 氯胺酮,并且其特定代谢产物(2S,6S;2R,6R)-HNK 还可持续发挥抗抑郁作用,动物和人体试验中R 异构体表现出比S 异构体更轻的精神症状和成瘾潜力,有望克服氯胺酮使用的最大顾虑——拟精神病症状,因此极具开发潜力。目前恒瑞在国内申报的R 氯胺酮鼻喷剂(受理号CXHL1900090)用于难治性抑郁症的治疗。
R 氯胺酮在抗抑郁领域具有不同于S 氯胺酮的作用机制和优势,可以与S 氯胺酮一道填补快速起效抗抑郁治疗领域的巨大空白。下文以R 氯胺酮为核心从药学、有效性、安全性等各方面展开综述。
1 原料药制备
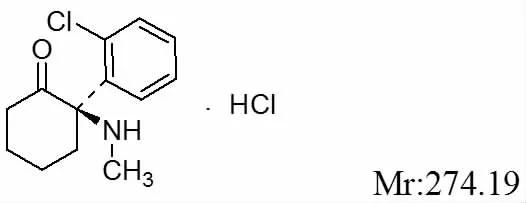
Janssen 公司在其申请的专利CN107750245A 中涉及(R)-氯胺酮的拆分方法:将外消旋氯胺酮与(R)- 樟脑磺酸在水环境下反应,得到R- 氯胺酮的(R)- 樟脑磺酸盐的一水合物;之后与无机碱反应,得到呈游离碱的R- 氯胺酮;R- 氯胺酮游离碱与HCl 反应,得到R 氯胺酮盐酸盐[2]。该法于水环境中反应,污染小,适用于大规模或商业制造。
2 非临床研究
药理学:
(1)抗抑郁。
在地塞米松暴露致抑郁小鼠模型中,R 氯胺酮表现出比S氯胺酮更明显和持久的抗抑郁作用[3];在社会挫败应激及习得性无助抑郁模型研究中R 氯胺酮也表现出比S 氯胺酮更持久和更安全的抗议与作用,无精神样及成瘾性等不良反应[4];在炎症模型中R 氯胺酮的急性抗抑郁作用没有性别差异[5]。由于两个异构体在啮齿动物大脑中的药物浓度相同,所以抗抑郁的效力的差异并不是由生物利用度的差异造成的[6,7]。Zanos P 认为S和R 氯胺酮发挥抗抑郁作用的机制与AMPA 的早期和持续激活相关[6]。
研究发现R 氯胺酮与S 氯胺酮的作用通路不同,R 氯胺酮无法恢复由压力引起的海马内侧前额皮质、CA3 区域或齿状回磷酸化mTOR 水平的持续下降,而且通过脑室内给予雷帕霉素或AZD8055 抑制mTOR 不能阻止R 氯胺酮的抗抑郁作用却可以阻止S 氯胺酮,另一方面ERK 抑制剂SL327 只阻止了R- 氯胺酮的抗抑郁作用,该研究认为mTOR 通路在S 氯胺酮抗抑郁作用中有重要作用,而R- 氯胺酮抗抑郁作用与之无关,R 氯胺酮可降低应激诱导的小鼠前额皮质海马CA3 区磷酸化MEK 水平其到抗抑郁作用[8]。
Todd Gould 的报道,认为R 异构体的特定代谢产物(2S,6S;2R,6R)-HNK 可以发挥持续的抗抑郁作用,并且也与AMPA 通路相关[9]。
海马结构的可塑性被认为是严重抑郁的中心机制之一[10],研究表明脑源性神经营养因子(BDNF)、胶质细胞源性神经营养因子(GDNF)和碱性成纤维细胞生长因子(bFGF)水平在抑郁症患者大脑中的减少与海马神经再生减少有关,Yang B 等研究发现R- 氯胺酮可能通过前额叶皮质和海马区域的BDNF-TrkB信号转导,影响突触的形成来维持抗抑郁作用。
基础研究和临床观察证实肠道微生物的改变与神经和精神疾病具有重大关联,研究发现重度抑郁症患者存在肠道微生物中拟杆菌、变形菌、放线菌、肠杆菌、另枝菌明显增加。Yang 等发现,慢性社交失败压力抑郁小鼠使用R 和S 氯胺酮后,小鼠在抑郁状态改善的同时,δ 变形菌的含量减少,而δ 变形菌可能通过炎症反应促成小鼠的抑郁样表型,认为氯胺酮的抗抑郁作用与肠道菌恢复有关;此外R 氯胺酮比S 氯胺酮更能诱导丁酸单胞菌水平的升高,从而产生更多具有抗炎作用的丁酸盐,从而降低抑郁症发病机制中的炎症性作用。
(2)麻醉。
氯胺酮脊麻机制极其复杂,主要包括阻断位于于腰背部浅背角神经元上的Na+、KDR通道,从而降低神经元的兴奋性发挥局麻作用。Rose Schnoebel 等人报道,氯胺酮对上述离子通道的作用强度存在立体选择性差异,R 氯胺酮的麻醉效力只有S 氯胺酮的三分之一,S 氯胺酮在阻断Na+通道的作用强度上比R异构体强约2.1 倍;对KDR通道的阻断R 氯胺酮略高于S 氯胺酮。
(3)镇痛。
1978 年,Ryder 等人首次报道了氯胺酮的两个异构体在小鼠身上具有不同的镇痛效应。S 异构体与NMDA 受体的PCP 位点亲和力约为R 异构体的3-4 倍。
(4)支气管扩张。
氯胺酮对支气管平滑肌有舒张作用,其中两种异构体可能由于对受体门控钙离子通道的作用不同而使得R 氯胺酮在乙酰胆碱介导的ASM收缩产生更强的舒张作用。
(5)循环系统抑制。
消旋氯胺酮可兴奋心血管系统,引起血压升高、心律增快和心排血量增高,而R 氯胺酮却呈现负性肌力作用,并伴有细胞内钙离子浓度降低。
消旋氯胺酮可提高脑代谢率(CMR)和脑血流(CBF),尤其是在前扣带回和额叶皮质、丘脑和壳核,而R 氯胺酮同时降低CBF 和CMR。
(6)其他。
精神药物可绕过大脑本身的神经递质而直接刺激脑内的受体,引起多巴胺释放和受体的脱敏,达到比自然释放更加强烈的奖赏效果,从而开始滥用、成瘾和戒断的恶性循环。通过正电子发射断层扫描(PET)技术研究表明亚麻醉剂量S 氯胺酮可促进猴大脑纹状体多巴胺释放,并伴随有29%的D2/3 受体可用性降低,而R 氯胺酮则无影响,预示着R 氯胺酮在此方面具有比S 氯胺酮更高的安全性。
3 临床研究
3.1 药代动力学
R 氯胺酮的清除率和分布容积小于S 氯胺酮,R 氯胺酮经细胞色素P450 酶CYP2B6 和CYP3A4 代谢为R 去甲氯胺酮,CYP2B6 和CYP2C9 等也有少量参与,后续代谢产物发生葡萄糖醛酸化。
3.2 有效性
多项小鼠抗抑郁药物疗效测试中显示R 氯胺酮的效力比S氯胺酮更强,量效差异高达30 倍。R 氯胺酮与NMDA 受体亲和力相比S 氯胺酮低,产生的由NMDA 受体介导的拟精神病样反应也更少,也不会导致前额皮质中PV 免疫反应的丧失,因此将有潜力成为比S 氯胺酮更安全的快速起效抗抑郁药,但目前缺乏公开临床试验数据报道。
R 氯胺酮的麻醉效力只有S 氯胺酮的三分之一(所需诱导麻醉剂量分别为429±37mg 和140±21mg)。
3.3 安全性
R 氯胺酮在人体试验中表现出比S 氯胺酮更高的安全性。文献报道在听觉、视觉和本体感觉上的改变以及幻觉经历是由于S- 氯胺酮造成,而放松的感觉与R 氯胺酮有关。特别是在等剂量条件下,R 氯胺酮与拟精神病反应无关,反而可以诱导产生“幸福感”,R 氯胺酮相对S 氯胺酮具有更少的迷幻效果。Mathisen 等人的给予口腔和面部疼痛患者分别采用S 和R 氯胺酮进行治疗,其中使用S 氯胺酮的患者(剂量为0.45mg/kg,最大血清浓度为120ng/ml 或0.5nM)有56%的出现幻觉,而使用R氯胺酮的患者(剂量为1.8mg/kg,最大血清浓度为590ng/ml 或2.5nM)中仅有22%出现了幻觉,值得注意的是该试验中R 氯胺酮的剂量是S 氯胺酮的4 倍。
R 氯胺酮对脑电图的抑制作用低于S 氯胺酮。Pfenninger 等招募24 例健康受试者,分别给予三次R 氯胺酮和S 氯胺酮注射,之后进行认知功能检测,结果表明,S 氯胺酮三次注射后出现认知功能损害,而R 氯胺酮没有出现。
由于R 氯胺酮比S 氯胺酮晚开发,因此尚需进一步的临床试验探索其机制、有效性和安全性。
