活血止痛丸质量标准研究
2020-06-08陶思宇张永萍陈晓兰徐帮会刘纯纯刘政岑
陶思宇,张永萍,陈晓兰,徐帮会,刘纯纯,刘政岑
(贵州中医药大学,贵阳 550025)
活血止痛方是遵义市刘端方骨伤医院临床经验方,源于贵州苗族,用于治疗骨伤病早期损伤。活血止痛方由丹参、当归尾、赤芍、茯苓、连翘等27味中药组成,具有行气活血、化瘀止痛之功效,可使瘀血得散、气血得通,促进骨折的愈合[1-3]。本试验对赤芍、西红花、木香、连翘、栀子进行了薄层鉴别,测定了本方组成中赤芍的丹酚酸B含量,以准确、可靠、专属性强为基准,建立了该苗药组方的质量控制方法。
1 仪器与试药
1.1 仪器 高效液相色谱仪(日本岛津2030,LabSolutions,LC-2030C 3D),DZ-20可倾式多功能制丸机(温岭市林大机械有限公司);AUW120D十万分之一电子天平(岛津制作所),TGL-16B高速离心机(上海安亭科学仪器厂),紫外分析仪(型号:WD-9403C,上海金鹏分析仪器有限公司)。
1.2 药品与试剂 丹酚酸B对照品(批号:111562-201716);赤芍对照药材(批号:121093-201303);西红花对照药材(批号:121009-201704);木香对照药材(批号:0921-200104);连翘对照药材(批号:120908-201216);上述对照药材均购于中国食品药品检定研究院。阴性对照品除去处方中所含鉴别药材后按该制剂工艺制备而成;活血止痛丸(自制);甲酸、正丁醇等试剂均为分析纯;乙腈、磷酸为色谱纯;水为娃哈哈纯净水。
2 定性鉴别
2.1 赤芍的薄层鉴别
2.1.1 供试品溶液的制备 取活血止痛丸约4.0 g,研细,加蒸馏水50 mL,超声60 min,滤过,取滤液10 mL,加水饱和正丁醇(1:1)溶液萃取2次,每次10 mL,取正丁醇层,加氨试液2.5 mL,萃取,取正丁醇层,加正丁醇饱和水(1:1)溶液萃取2次,每次7.5 mL,取正丁醇层,挥干,加2 mL甲醇溶解,备用[4]。
2.1.2 对照药材溶液的制备 取赤芍对照药材约0.5 g,按“2.1.1”项下供试品溶液的制备方法制备。
2.1.3 阴性对照溶液的制备 取缺赤芍和牡丹皮的双阴性活血止痛丸样品约4.0 g,按“2.1.1”项下供试品溶液的制备方法制备。
参考2015版《中国药典》第4部通则0502上面的质量控制检识方法,吸取供试品溶液15 μL,赤芍的对照药材溶液10 μL及赤芍和牡丹皮的双阴性对照溶液各15 μL,采用TLC进行检识,三氯甲烷—乙酸乙酯—甲醇—甲酸(20:2.5:5:0.5)作为展开剂进行展开,待溶剂前沿到达板的顶端时取出,随后用5%香草醛硫酸乙醇溶液润湿该薄层板,放置几分钟后放入恒温烘箱中用105 ℃加热至斑点显色清晰,在与对照药材色谱相应的位置上,显相同颜色的斑点,阴性对照无干扰[4]。见图1。

图1 活血止痛丸(赤芍)TLC鉴别图
2.2 西红花的薄层鉴别
2.2.1 供试品溶液的制备 取活血止痛丸样品约0.36 g,研细,加甲醇1 mL,超声处理10 min,放置使澄清,取上清液作为供试品溶液[5]129。
2.2.2 对照药材溶液的制备 取西红花对照药材约20.0 mg,按“2.2.1”项下供试品溶液的制备方法制备。
2.2.3 阴性对照溶液的制备 取缺西红花的阴性活血止痛丸样品约0.36 g,按“2.2.1”项下供试品溶液的制备方法制备。
参照2015版《中国药典》第4部通则方法,取上述3种溶液各5 μL进行薄层定性分析,以展开剂乙酸乙酯—甲醇—水 (100:16.5:13.5)进行展开,然后记录在紫外灯的显示情况[5]。见图2。
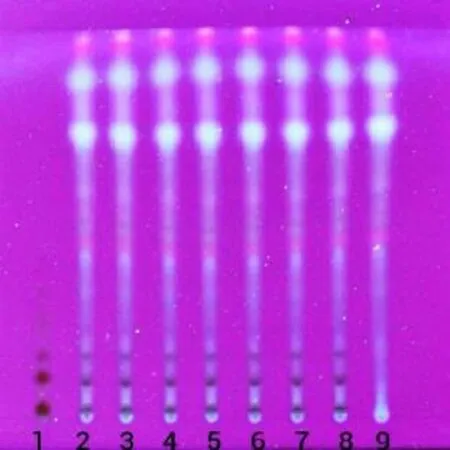
图2 活血止痛丸(西红花)TLC鉴别图
2.3 木香的薄层鉴别
2.3.1 供试品溶液的制备 取活血止痛丸样品约5.0 g,研细,加三氯甲烷10 mL进行超声30 min后过滤,将滤液收集备用[5]62。
2.3.2 对照药材溶液的制备 取对照药材粉末约0.5 g,加甲醇10 mL,超声30 min后滤过,滤液即为对照药材溶液。
2.3.3 阴性对照溶液的制备 取缺木香的阴性活血止痛丸样品约5.0 g,按“2.3.1”项下供试品溶液的制备方法制备。
参照2015版《中国药典》第4部通则方法,对上述3种溶液各3~5 μL进行薄层检识,以展开剂三氯甲烷—环己烷(5:1)进行展开,待溶剂前沿到达板的顶端时取出,随后采用1%的香草醛硫酸乙醇溶液润湿该薄层板,最后将该薄层板放置105 ℃恒温烘箱中直到样品的点清晰取出。见图3。
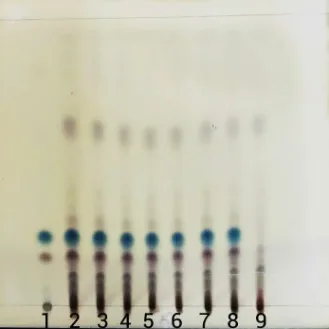
图3 活血止痛丸(木香)TLC鉴别图
3 含量测定
本丸剂由27味药组成,丹参为方中君药,丹酚酸B作为丹参主要成分之一。故以丹酚酸B为指标建立HPLC含量测定方法,经方法学验证表明该方法简便、稳定可行。
3.1 色谱条件 色谱柱:ZORBAX SB-C18(250 mm×4.6 mm,550);流动相:乙腈-0.1%磷酸溶液(21:79);流速:1.2 mL/min;检测波长:286 nm;柱温20 ℃;进样量10 μL。
3.2 对照品溶液的制备 精密称取丹酚酸B对照品适量,加甲醇-水(8:2)的混合溶液制成浓度为0.1 mg/mL的对照品溶液。
3.3 供试品溶液的制备 称取研细的活血止痛丸约0.5 g,精密称定,于25 mL容量瓶中,加入25 mL 80%甲醇后称重,超声提取60 min,取出,冷却,用80%甲醇补足重量,离心10 min,取上清液,即得。
3.4 阴性对照溶液的制备 按活血止痛丸的制备方法制成不加丹参的阴性丸,同“3.3”项下供试品溶液的制备方法制成缺丹参的阴性对照溶液。
3.5 系统适用性试验 分别取丹酚酸B对照品溶液、供试品溶液及缺丹参药材阴性供试品溶液各10 μL,按“3.1”项下色谱条件进行测定,记录色谱图,结果丹酚酸B的保留时间约为28.5 min,分离度均在1.5以上,理论塔板数为6 000,阴性对照溶液和空白对照溶液均无干扰。见图4~图6。
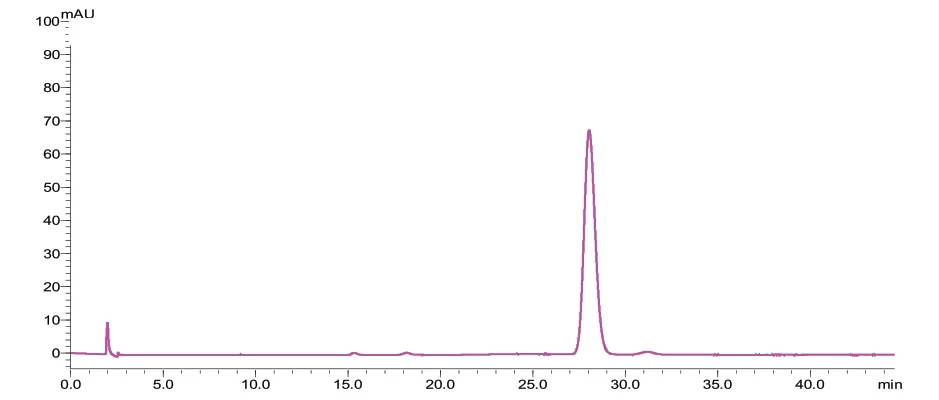
图4 丹酚酸B对照品溶液
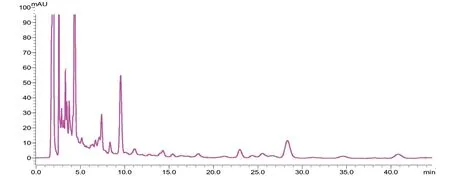
图5 供试品溶液
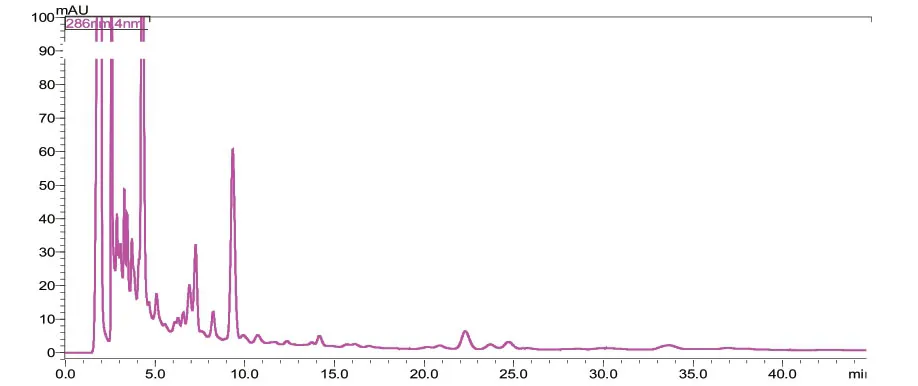
图6 阴性对照溶液
3.6 线性关系考察 分别取1.0、1.2、1.4、1.6、1.8、2.0、2.2 mL 配好的丹酚酸B对照品溶液(C对=0.382 8 mg/mL),定容到 10 mL,精密吸取10 μL,按“3.1”项下色谱条件进行测定,以峰面积为纵坐标(y),丹酚酸B质量浓度为横坐标(x,mg/mL),得线性回归方程:y=8E+06 x -4719.8(r=0.999 8)。结果表明在0.038 28~0.084 22 mg/mL范围内峰面积与丹酚酸B对照品溶液浓度呈良好的线性关系。
3.7 精密度试验 精密吸取对照品溶液10 μL按“3.1”项下色谱条件进行测定,连续进样6次,记录峰面积,结果RSD=0.058 8%<3%,表明仪器精密度良好。
3.8 稳定性试验 按“3.3”项下供试品溶液的制备方法制备1份供试品,放置0、1、2、4、6、8 h后,分别按“3.1”项下色谱条件进行测定,记录峰面积结果RSD=0.830%,说明供试品中丹酚酸B在8 h内稳定,用此方法测活血止痛丸中丹酚酸B的含量时,供试品放置时间不宜超过8 h。
3.9 重复性试验 精密称取研细的活血止痛丸6份,分别按“3.3”项下供试品溶液的制备方法制备供试品溶液,按“3.1”项下色谱条件进行测定,记录峰面积并计算活血止痛丸中丹酚酸B的含量,结果测得酚酸B的平均含量为3.206 mg/mL,RSD=0.506%,表明重复性良好。
3.10 回收率试验 精密称取约0.25 g研细的活血止痛丸9份,分别置于25 mL容量瓶中,精密加入相当于0.5 g中丹酚酸B的质量的50%、100%、150%的丹酚酸B对照品溶液,各3份,按“3.3”项下供试品溶液的制备方法制备供试品溶液,按“3.1”项下色谱条件进行测定,结果每个回收率都在95%~105%范围内,RSD=0.78%<2%,回收率达到要求,表明活血止痛丸中的其它成分对丹酚酸B的含量测定影响不大或建立的此方法对丹酚酸B的含量无显著影响。见表1。
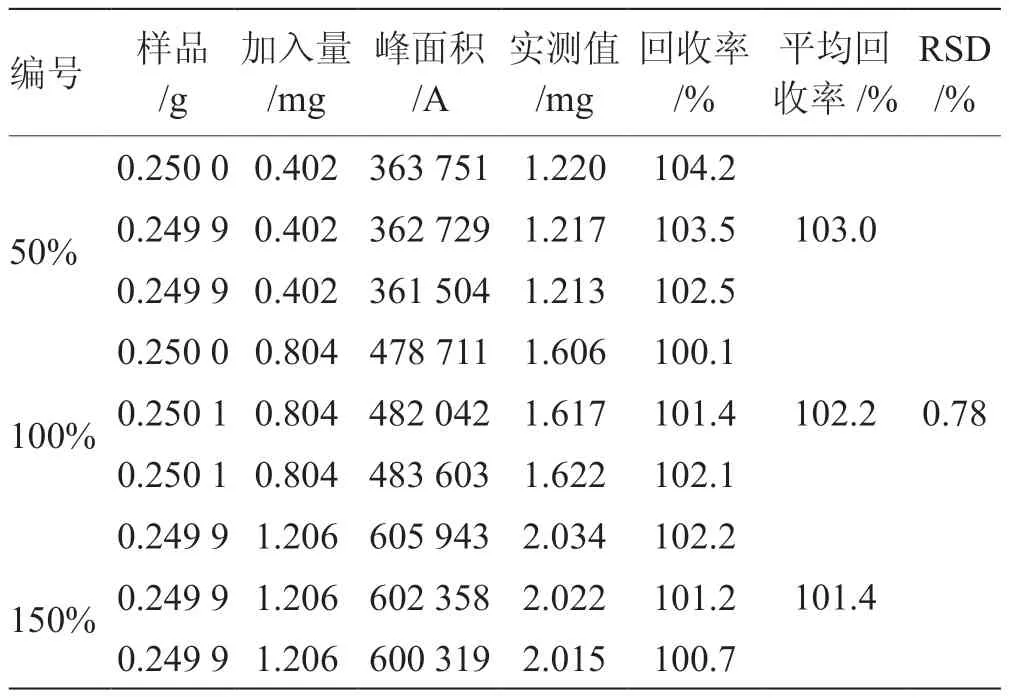
表1 丹酚酸B对照品回收率试验表
3.11 活血止痛丸中丹酚酸B的含量 取3个不同批次的活血止痛丸,按“3.3”项下制备供试品溶液,得3份供试品溶液。分别进样10 μL,按“3.1”项下色谱条件进行测定。见表2。
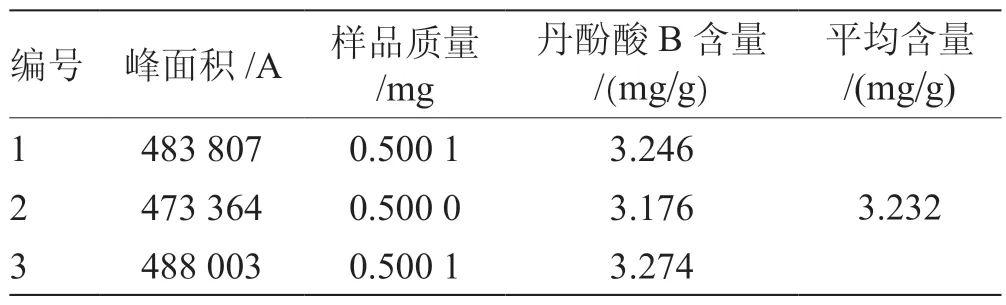
表2 活血止痛丸中丹酚酸B的含量
4 讨论
本试验因活血止痛丸处方药味较多,成分复杂,易出现阴性干扰,故赤芍供试品与阴性对照采用了正丁醇萃取去除杂质,而木香的供试品与阴性对照采用了三氯甲烷代替甲醇超声滤过提取的方法。含量测定供试品制备纯化过程中发现,供试品超声后用0.45试验的微孔滤膜过滤,经过多次方法学考察,丹酚酸的回收率均在80%左右,怀疑是滤膜的滞留作用导致。经过摸索发现采用高速离心纯化相较于微孔滤膜过滤丹酚酸B含量要高且回收率达到要求,证实微孔滤膜对丹酚酸B具有截留作用。所以确定供试品的纯化方法为超声后直接高速离心。综上所述,建立了活血止痛丸的质量标准,为其质量控制提供参考。
