晚期非小细胞肺癌一线吉非替尼治疗后的耐药时间分析
2020-06-08徐佳欢王新年徐小嫚
徐佳欢,王新年,黄 新,赵 立,徐小嫚
0 引言
在中国,肺癌的发病率和死亡率居各种恶性肿瘤之首,而肺癌中又以非小细胞肺癌(NSCLC)多见。大多数患者在发现肺癌时已处疾病晚期,失去最佳手术机会。传统的放化疗作用有限,且不良反应较大。相比之下,选择肺癌靶向药可缓解临床症状、减少治疗的不良反应、使用方便、可延长无进展生存时间(PFS),受到临床青睐。EGFR突变是精确治疗中最常见的靶点,占亚洲晚期NSCLC患者的50%~60%[1]。然而,靶向药不可避免地在几个月到几年内出现耐药问题。在肺癌靶向药中最常用的是Ⅰ代表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKI)中的吉非替尼。本文旨在通过收集选择吉非替尼一线治疗的晚期NSCLC患者的数据,从病史、检验学、影像学、基因检测等方面分析与耐药时间的关系,为临床提供参考。
1 资料与方法
1.1 研究对象 本研究为回顾性分析。选取2015年1月至2019年10月中国医科大学附属盛京医院就诊的晚期NSCLC,并选取吉非替尼为一线治疗的患者作为研究对象。纳入标准:①病理学诊断明确的NSCLC患者,且有EGFR基因突变;②第8版国际肺癌TNM分期为ⅢB期~Ⅳ期;③至少有一个可测量的肿瘤病灶;④选择吉非替尼一线治疗并按说明书剂量正确服药;⑤无重要脏器功能障碍。排除标准:①有其它恶性肿瘤病史;②同时期联合手术、放化疗、免疫、中药等其它治疗;③既往使用过EGFR-TKI;④非严重不良反应而自行减量或停药者;⑤未按医嘱定期复查。
1.2 研究内容 收集患者吉非替尼治疗前的资料,包括:①一般资料:姓名、性别、年龄、吸烟史;②检验参数:癌胚抗原(CEA)、细胞角蛋白19片段(CY211)、神经元特异性烯醇化酶(NSE)、中性粒/淋巴细胞比值(NLR)、乳酸脱氢酶(LDH)、血红蛋白(Hb);③影像学参数:肿瘤最大径、是否有胸腔积液、器官转移情况(肺、骨、肝、肾上腺);④EGFR突变类型;⑤肿瘤TNM分期。
1.3 研究方法 按RECIST1.1标准,患者在吉非替尼治疗期间,每1~2个月对肺、骨、脑、腹部等常见转移部位进行影像学复查,若靶病灶(所有累及器官)最长径总和增加≥20%,且绝对值增加5 mm,或出现新病灶,则认为疾病进展(PD),即对吉非替尼产生耐药。依据Jackman等[2]发表的关于EGFR-TKI获得性耐药标准,接受EGFR-TKI单药治疗后客观上的临床获益包括完全缓解、部分缓解或是超过6个月的疾病稳定(依照RECIST或WHO标准)。且研究发现,大多数患者在口服吉非替尼约12个月后出现PD[3-5]。将患者吉非替尼单药一线治疗后的耐药时间分为耐药(耐药时间≤6个月)、中度敏感(6个月<耐药时间≤12个月)、敏感(耐药时间>12个月)3组,研究上述各因素在不同耐药时间分组间是否有统计学意义。
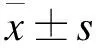
2 结果
最后纳入符合标准对象110例,其中男31例,女79例;年龄33~86岁,平均年龄(60.85±9.98)岁;耐药组20例,中度敏感组54例,敏感组36例。
2.1 单因素的组间差异性分析 结果见表1。其中,3例EGFR罕见突变中2例为21外显子L861Q突变,1例为18外显子突变;1例EGFR多重突变为21外显子联合20外显子突变。由表1可看出,年龄≥65岁、CY211、NLR≥4、高LDH、肝转移均满足P<0.05,这些指标在不同耐药时间分组间有显著性差异。
2.2 相关性分析 将上述5个组间有显著差异的指标与耐药时间分组进行Spearman相关性分析,结果见表2。

表1 吉非替尼治疗晚期NSCLC耐药时间的单因素分析

表2 吉非替尼治疗晚期NSCLC耐药时间的相关危险因素分析
由表2可以看出,这5个指标的P值均<0.05,均与耐药时间存在显著的相关关系。其中,年龄≥65岁与耐药时间呈正相关关系,年龄大者预示着耐药时间较长。CY211、NLR≥4、高LDH、肝转移与耐药时间呈负相关关系,高CY211、高NLR、高LDH、肝转移预示着耐药时间较短。
2.3 回归分析 将上述5个相关指标与耐药时间分组进行多元有序Logistic分析,筛选出P<0.05的指标,结果见表3。

表3 吉非替尼治疗晚期NSCLC耐药时间的独立危险因素分析
由表3可以看出,年龄<65岁、NLR≥4、肝转移是耐药时间短的独立危险因素。
3 讨论
吉非替尼自2003年成为首个FDA(美国食品和药品监督管理局)批准的用于EGFR突变阳性的晚期NSCLC患者一线治疗的靶向药物后,在临床上的有效性和安全性得到广泛认可,但其耐药问题仍然棘手,个体患者的耐药时间差异性较大。随着对吉非替尼的耐药机制探索地不断深入,科研者们发现EGFR-TKI耐药是因为产生了新的EGFR突变位点,并依据耐药靶点相继研发了Ⅱ代、Ⅲ代EGFR-TKI,但NSCLC对Ⅲ代EGFR-TKI也产生了耐药,目前Ⅳ代EGFR-TKI正在研发中。由于取材、技术、经济等问题限制,不能满足所有患者均可获取合格标本进行一系列分子生物检测,故总结临床参数与耐药时间的关系,在临床实践中发现有效、快速、方便的参数用于预后评估,为临床医生提供参考价值。
在本研究中,我们得出年龄<65岁是耐药时间短的独立危险因素,与既往研究结果相似。国内、国外均有Meta分析得出,具有EGFR敏感突变(19外显子缺失、21外显子L858R点突变)的晚期NSCLC老年(≥65岁)患者,与年轻患者相比,在接受EGFR-TKI治疗后PFS更长[6-7]。Tsai等[8]发现具有EGFR罕见突变(18外显子G719X突变、20外显子S768I突变、21外显子L861Q等,20外显子T790M突变、20外显子插入突变除外)的Ⅳ期肺腺癌患者中,老年(≥65岁)患者与年轻患者相比,在接受EGFR-TKI治疗后PFS更长。这可能与老年人机体代谢缓慢,肿瘤生长速度相对较慢相关。但对于EGFR突变的NSCLC,不同年龄阶段的肿瘤生物学行为差异仍需进一步研究。
本研究得出高CY211与耐药时间短相关,但不是独立相关,提示治疗前血中高CY211可能是影响PFS短的重要因素,这与既往研究相符。有研究表明,血清肿瘤标志物能反映肿瘤细胞转化的过程,检测肿瘤标志物的表达对肿瘤的诊断、疗效及预后评价有良好的作用[9]。血清中CY211是检测NSCLC,特别是肺鳞状细胞癌的一种肿瘤标志物,与肿瘤TNM分期、病程及预后有关,可作为疾病判断的参考指标[10]。Ren等[11]通过多因素Cox回归分析证实了CY211高表达是影响晚期NSCLC生存的重要因素,但不是影响OS的独立因素。研究发现,外周血中高水平的CY211(超过正常上限)者预后较差[12]。一些研究还指出,治疗前后CY211水平下降幅度≥30%可作为晚期NSCLC患者的独立预后因素[11]。
本研究得出NLR≥4与耐药时间短独立相关,提示血NLR升高预示着PFS更短,这与既往研究类似。外周血NLR升高,是全身非特异性炎症反应的替代标志物,已被证明是多种恶性肿瘤(包括NSCLC在内)的不良预后因素[13]。Lin等[14]证实了在接受Ⅰ代EGFR-TKI治疗的EGFR突变阳性的NSCLC患者中,NLR升高(≥3.5)是PFS和OS更差的独立预后因素。Aguiar-Bujanda等[15]则发现接受EGFR-TKI的EGFR突变阳性的晚期NSCLC患者中,NLR≥4.39者预后不佳。NLR升高作为癌症患者预后不良因素的机制尚未得到证实。越来越多的证据揭示了涉及炎症和癌症的分子和细胞途径,表明炎症有助于肿瘤细胞的增殖、血管生成和转移。体外研究表明,中性粒细胞可以抑制淋巴细胞诱导的细胞毒性活性,当中性粒细胞和淋巴细胞共同培养时,抑制程度与中性粒细胞数目成正比[16]。中性粒细胞和淋巴细胞之间的相互作用可能是另一个潜在的机制。然而,NLR的界值因研究而异,研究范围为2.11~5.00,尽管有Meta分析得出最佳界值为4,但目前最佳界值仍无统一定论[17-19]。
本研究得出高LDH与耐药时间呈负相关关系,但不是独立相关,提示治疗前血中高LDH可能是影响PFS短的重要因素,与既往研究符合。研究表明,高血清LDH水平与NSCLC预后不良相关[20-21]。Inomata等[22]发现,在Ⅰ代EGFR-TKI治疗前血清高LDH水平的EGFR突变阳性的NSCLC患者,与血清LDH水平较低的患者相比,PFS、OS均较短。LDH是一种胞质酶,可逆地催化丙酮酸转化为乳酸,完成糖酵解的最后步骤。由于肿瘤细胞的高代谢需求,造成相对低氧,尤其在肿瘤中心。LDH由低氧诱导因子(HIF)和myc翻译上调,HIF与LDH之间存在正反馈环,HIF活化上调LDH活性,而高乳酸浓度又进一步促进HIF活化。LDH在肿瘤细胞中广泛表达,即使在正常氧浓度下,丙酮酸转化为乳酸也会上调。肿瘤微环境酸化可促进肿瘤的进展和转移[23]。Fiala等[24]研究发现,在厄洛替尼治疗的第1个月LDH血清水平的变化(增长≥0.3 μkat/L)与疾病控制率(DCR)低、PFS短和OS短独立相关。对于EGFR突变阳性的晚期NSCLC患者,吉非替尼治疗期间血清LDH水平的动态变化与预后的相关性仍需大数据验证。
本研究发现,肝转移者与耐药时间短独立相关,与既往研究结果符合。但入组的肝转移患者数量偏少,仍需大数据验证。Wu等[25]研究接受一线吉非替尼治疗的EGFR突变的Ⅳ期肺腺癌患者,发现肝转移预示PFS和OS较差,是PFS和OS的独立预后不良因素。吉非替尼被肝细胞色素P450 CYP3A4和CYP2D6广泛代谢,但有药代动力学研究[26-27]显示,肝转移引起的不同程度肝损害患者的药代动力学特征相似。研究表明,具有CD133标记物(肺癌干细胞最常用的标记物之一)的A549细胞显示出很高的肝转移潜能[28]。肝脏是免疫系统的重要组成部分,转移的癌细胞可能阻碍免疫监视机制,损害肿瘤免疫。有关肝转移影响预后的机制尚待进一步研究,以寻找改善预后的治疗方法。
此外,在特定的转移器官影响预后方面,研究发现,在接受吉非替尼治疗的NSCLC患者中,脑转移与耐药密切相关[29-30]。由于吉非替尼在脑脊液中的浓度相对较低,一般认为吉非替尼对中枢神经系统转移性肺癌的疗效较低。脑转移患者更多选用Ⅲ代EGFR-TKI,或Ⅰ代EGFR-TKI联合放疗,不符合本研究纳入标准,故本研究中脑转移患者例数较少,脑转移因素未纳入研究范围。
本文分析所得预测因子检测方便、无创、费用相对较低,因此对于EGFR突变阳性的晚期NSCLC患者,若年龄≥65岁、NLR<4、无肝转移,可较积极地选用吉非替尼;若年龄<65岁、NLR≥4、有肝转移,则需积极复查,及时发现耐药,及时更换治疗方案。但本研究仍存在不足:第一,入选病例研究因素倾向于既往得出阳性结果且临床数据收集完整的因素,可能存在选择性偏移;第二,此研究未纳入因口服吉非替尼出现严重不良反应而减量或停药的患者,对此部分患者的用药方案仍需进一步探讨;第三,本研究为回顾性分析,样本来自单一机构,样本数量小,所得结论还需多中心、前瞻性研究来证实。
