一株鸭源H6N6 亚型禽流感病毒的全基因组序列分析及对小鼠的感染性研究
2020-06-05范威峰崔鹏飞崔嘉琦谷文丽张元成孔兴天彭大新邓国华陈化兰
范威峰,崔鹏飞,崔嘉琦,谷文丽,张元成,邢 鑫,孔兴天,彭大新,邓国华*,陈化兰
(1.扬州大学,江苏 扬州 225009;2. 中国农业科学院哈尔滨兽医研究所 兽医生物技术国家重点实验室/农业部动物流感重点开放实验室,黑龙江 哈尔滨 150069)
禽流感病毒(Avian influenza virus, AIV)属于正黏病毒科A 型流感病毒属,其表面糖蛋白为血凝素(Haemagglutinin, HA)和神经氨酸酶(Neuraminidase,NA),共可划分为16个HA亚型和9个NA亚型。1965年首次从火鸡体内分离到H6 亚型AIV,随后在野鸭和其它多种水鸟中陆续分离到H6 亚型AIV[1]。1997年,在我国香港暴发人感染H5N1 亚型AIV 疫情期间,一株感染人的H5N1 亚型AIV(A/HongKong/156/97)的6 条内部基因与一株H6N1 亚型AIV(A/teal/HongKong/W312/97)的核苷酸同源性大于98%,表面基因NA 与该H6N1 亚型AIV NA 基因同源性大于97%,提示该H6N1 亚型AIV 可能是H5N1 亚型AIV的基因供体[2]。2013 年我国台湾出现首例人感染H6N1 亚型AIV,这也是人可以感染H6 亚型AIV 的直接证据[3]。H6 亚型AIV 对家禽呈低致病性,2010年法国火鸡场暴发了H6N1 亚型禽流感疫情,表明H6 亚型AIV 对家禽的致病性有增强的趋势[4]。本实验室对2008 年~2011 年分离的257 株H6 亚型AIV 进行系统研究,受体结合检测结果显示,有34%的病毒株(87/257)获得了结合人源受体的能力,大部分病毒株(37/38)在没有预先适应的情况下就能在小鼠肺脏内有效复制,其中部分病毒(5/10)还能够在豚鼠间发生高效的接触传播[5],这些事件表明H6 亚型AIV 具有跨越物种屏障感染人类并在人群间传播的潜在风险。因此,加强H6 亚型AIV 的监测具有重要的公共卫生学意义。
本研究对2015 年从广东家鸭中分离的一株H6N6 亚型AIV 进行全基因组测序、进化分析和BALB/c 小鼠的感染性试验,初步评价该分离株对哺乳动物的潜在风险,为AIV 的监测和禽流感防控提供数据支持。
1 材料与方法
1.1 病毒株及实验动物 病毒株DK/GD/S1182/2015(H6N6)由国家禽流感参考实验室分离、鉴定并保存;10 日龄SPF 鸡胚购自哈尔滨兽医研究所实验动物中心;6 周龄雌性BALB/c 小鼠购自北京维通利华实验动物有限公司。
1.2 主要试剂 病毒RNA 提取试剂盒购自天根生化科技(北京)有限公司;反转录试剂盒购自东洋纺生物科技有限公司;Easy Taq DNA 聚合酶购自北京全式金生物技术有限公司;胶回收试剂盒购自OMEGA 公司,测序反应试剂盒Big Dye Terminator
3.1 购自美国ABI 公司。
1.3 病毒纯化及鸡胚半数感染量(EID50)的测定 将DK/GD/S1182/2015(H6N6)株病毒原液用PBS 10 倍倍比稀释后接种于10 日龄SPF 鸡胚,置于37 ℃培养72 h 之后4 ℃过夜,收取最高稀释度、最高血凝价鸡胚尿囊液,连续纯化3 代之后,再10 倍倍比稀释至105接种于10 日龄SPF 鸡胚,用同样方法收获尿囊液将其分装于冻存管中保存-70 ℃备用,EID50按照常规方法进行测定。
1.4 分离病毒的全基因组序列测定及分析 提取病毒核酸反转录为cDNA 后,以其为模板,参照Hoffmann 等[6]的反应条件和引物PCR 扩增该分离株的各基因节段,PCR 产物经回收纯化后,采用测序反应试剂盒BigDye Terminator 3.1 对病毒全基因组序列测定,得到的基因序列经SeqMan 软件拼接,通过Blast 比对得到与DK/GD/S1182/2015(H6N6)株各基因节段同源性最高的病毒株,利用MEGA 6.0 软件绘制HA 和NA 基因进化树。
1.5 小鼠的感染性试验 选取6 周龄体质量在15 g~16 g的BALB/c 雌性小鼠作为感染组和对照组。感染组8 只小鼠用干冰轻微麻醉后将DK/GD/S1182/2015(H6N6)株病毒以106EID50的剂量通过鼻腔感染,对照组5 只小鼠用相同方式接种50 μL PBS。3 d 后对感染组小鼠随机挑选3 只迫杀,无菌采集其脑、鼻甲、脾脏、肾脏和肺脏后研磨、离心。取每只小鼠的各脏器上清10 倍倍比稀释后接种10 日龄鸡胚进行脏器的病毒滴定,对照组和感染组剩余小鼠连续14 d 每天观察并记录体质量变化情况。
2 结果和讨论
2.1 分离病毒基因组序列测定及分析 将病毒株DK/GD/S1182/2015(H6N6)株的各基因节段经PCR 扩增后测序,得到的基因序列用SeqMan 软件拼接,通过NCBI 数据库经Blast 比对,得到与DK/GD/S1182/2015(H6N6)株各基因节段同源性最高的病毒株如表1 所示,表面基因HA 和NA 与在广东分离的一株猪流感病毒(SIV)A/swine/Guangdong/K6/2010(H6N6)核苷酸同源性最高,而内部基因与广西分离的一株AIV A/pigeon/Guangxi/164/2014(H6N6)核苷酸同源性最高(表1)。表明该病毒可能是由AIV 和SIV 重组产生,这种形式的重组可能会产生新的变异株引发新的流感大流行的潜在风险。
2.1.1 HA 基因序列分析 分离的DK/GD/S1182/2015(H6N6)AIV 经RT-PCR 扩增获得HA 表面基因,全长1 701 bp,编码566 个氨基酸,HA 蛋白裂解位点处氨基酸为339PQIETR↓GL346,仅存在一个碱性氨基酸,符合低致病性AIV分子特征。HA蛋白含有7 个潜在糖基化位点,分别为26NNS28、27NST29、39NVT41、306NKT308、311NVS313、498NGT500和557NGS559。该 分 离 株 与受体结合特性相关的氨基酸位点为151L、183H、186I、190E、191Q、194L、196G、220R、222V、225G、226Q、227R、228S和229R,该分离株HA 蛋白与之前的H6 亚型AIV 相比具有A222V 和G228S 的突变,尤其G228S 的突变可以促进H6 亚型AIV 对α-2, 6-唾液酸受体结合能力,而A222V 单独突变时,对病毒的受体结合能力影响不大,当这两个突变同时存在时,对病毒受体结合能力的影响远远大于单独突变的影响,表明HA 蛋白氨基酸位点A222V 和G228S 的突变可能会使该病毒具备结合α-2,6-唾液酸受体的能力[7-9]。H6 亚型AIV 分为北美和欧亚两个分支,该病毒HA 基因属于欧亚分支(图1),且与广东分离的一株SIV A/swine/Guangdong/K6/2010(H6N6)株HA 基因核苷酸同源性最高,为98.5%,表明,DK/GD/S1182/2015(H6N6)株病毒表面基因HA 可能来源于SIVA/swine/Guangdong/K6/2010(H6N6)株,同时具备结合人类受体α-2, 6-唾液酸受体的能力。
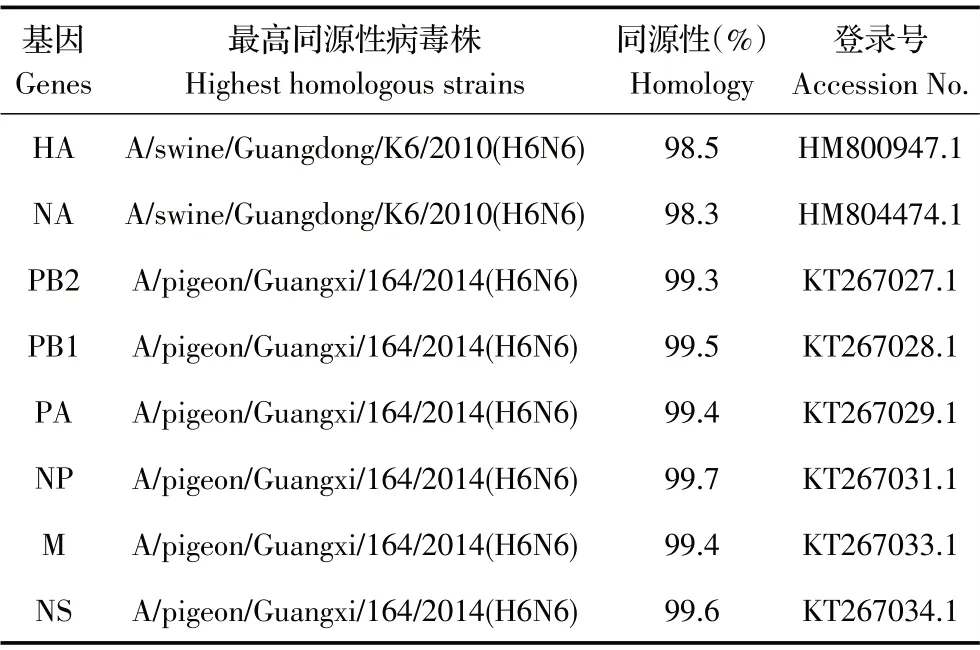
表1 与病毒株A/DK/GD/S1182/2015(H6N6)各基因节段最高同源性的BLAST 分析Table 1 The BLAST analysis of genes of A/DK/GD/S1182/2015(H6N6)

图1 A/DK/GD/S1182/2015(H6N6)分离株HA 基因进化树Fig.1 The phylogenetic tree based on the hemagglutinin(HA)gene of the A/DK/GD/S1182/2015(H6N6)virus
2.1.2 NA 基因序列分析 DK/GD/S1182/2015(H6N6)病毒株NA 基因编码区全长1 380 bp,编码459 个氨基酸,潜在糖基化位点有6 个,分别为54NPT56、59NIT61、75NLT77、135NGT137、190NAS192和391NWS393,在NA 颈 部有11 个氨基酸缺失,NA 颈部氨基酸的缺失可能会增强该病毒与受体的结合特性[10]。流感病毒NA 颈部区域氨基酸序列和长度均具有较大的可变性,目前对NA 颈部和所在糖基化位点的缺失相关机制还不清楚,而且这种NA 颈部缺失在某些亚型病毒中较为普遍,有人认为这可能是NA 酶活性在鸡细胞中存在缺陷,而NA 颈部缺失在某种程度上可以弥补这种缺陷[9],另种可能是先前水禽流感病毒在陆生家禽复制和传播中NA 酶活性相对太高,而NA 颈部缺失会降低NA 酶活性,这均从侧面表明这种NA颈部缺失可能是AIV 由水禽到陆生家禽的一种适应性突变[11-12]。NA 亚型也分为北美和欧亚分支,该病毒NA 基因属于欧亚分支(图2),且与广东分离的一株SIVA/swine/Guangdong/K6/2010(H6N6)株NA 基因同源性最高为98.3%,与该病毒NA 基因同源性较高的病毒以最近几年的H5N6 亚型居多,表明H5 与H6亚型AIV 可能在猪体内不断重组。
2.1.3 内部基因序列分析 内部序列分析显示,该分离株的聚合酶PB2 蛋白中并未出现与病毒传播性和致病性相关的氨基酸位点627K 和701N 的突变[13-14],在聚合酶PB1 和PA 蛋白中也未发现与病毒毒力相关的氨基酸436H(PB1)和515T(PA)的突变[15]。在M2 蛋白中也未出现抗金刚烷胺的关键氨基酸位点27A 和31N的突变[16],表明该病毒对金刚烷胺仍然敏感;但在NS1 蛋白中发生了与小鼠致病性增强相关的42S 和149A 氨基酸位点突变[17-18],这表明该分离株对哺乳动物可能具有一定的致病力。
2.2 小鼠的感染性试验结果 以106EID50病毒剂量通过鼻腔对BALB/c 小鼠进行人工感染,小鼠并没有表现明显的临床症状和体质量下降,表明该分离株对小鼠呈现低致病性;脏器病毒滴定结果显示,该分离株在没有预先适应的情况下就能够在小鼠肺脏内高效复制(图3),这与之前王国俊等人的研究一致[5]。大量的监测数据显示,H6 亚型AIV 的宿主范围从水禽过渡到陆生家禽,同时还有文献显示其还能够感染猪,甚至感染人的证据,这表明H6 亚型AIV 在进化过程中不仅逐渐适应了陆生家禽,同时也具有感染哺乳动物甚至人的能力。

图2 A/DK/GD/S1182/2015(H6N6)分离株NA 基因进化树Fig.2 The phylogenetic tree based on the neuraminidase(NA)gene of the A/DK/GD/S1182/2015(H6N6)virus
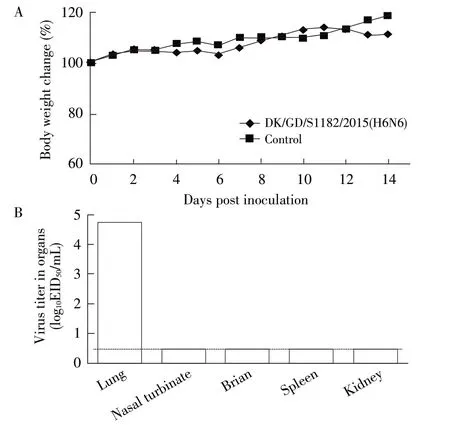
图3 病毒感染后小鼠体质量变化(A)和感染3 d 后脏器病毒滴定结果(B)Fig.3 Body weights of mice after inoculated with the virus(A)and virus titers in mice organs at 3 days post infection(B)
通过对DK/GD/S1182/2015(H6N6)株病毒进化关系分析表明,该病毒株表面基因HA 和NA 与广东分离的SIVA/swine/Guangdong/K6/2010(H6N6)株相应基因核苷酸同源性最高,而内部基因与广西分离的AIVA/pigeon/Guangxi/164/2014(H6N6)株 同 源 性 最高,表明该病毒可能是SIV 和AIV 重组产生。猪作为流感病毒的“混合器”,对人流感和AIV 均易感,而SIVA/swine/Guangdong/K6/2010(H6N6)株最早来源于禽类,在感染猪期间发生了适应性突变,尤其是在其HA 发生了G228S 的突变,该突变显著增强病毒对α-2,6-唾液酸受体结合能力,如果这种突变病毒再回归到禽类,无疑会增加AIV 对人类的感染风险。虽然DK/GD/S1182/2015(H6N6)株病毒发生了G228S 的突变,但对哺乳动物模型小鼠仍呈低致病性,并没有引起小鼠明显的临床症状和体质量下降;脏器病毒滴定结果显示,该病毒仅在小鼠肺脏复制,表明该病毒在哺乳动物中不具备传播能力。自从2013 年发生人感染H6N1 亚型AIV 事件,表明H6 亚型AIV 已经具有感染人的能力,因此,有必要继续加强对H6 亚型AIV 的监测及其相关生物学特性研究,为我国禽流感的监测预警以及防控提供数据支持。
