聚肽HVLPs 的制备与载药性能
2020-06-03王红权续文恒姜翔宇陈家琛蔡春华林嘉平
王红权, 续文恒, 张 朔, 姜翔宇, 李 慧, 陈家琛, 蔡春华, 林嘉平
(华东理工大学材料科学与工程学院,上海市先进聚合物材料重点实验室,上海 200237)
自然界中的病毒以DNA 或RNA 为核,蛋白质在外层有序排列形成衣壳。病毒的衣壳蛋白质通常形成规整有序的表面纳米结构,这些结构使病毒表现出高效的细胞内化能力[1]。模仿病毒的结构特征,人们通过聚合物自组装构建了一系列仿病毒粒子(VLPs),这些VLPs 在药物载体、基因工程等领域具有广阔的应用前景[2,3]。聚肽由氨基酸构成,具有良好的生物相容性;聚肽共聚物可以自组装形成形貌丰富的结构,在构筑VLPs 方面具有独特的优势[4-6]。近期,本课题组[7-10]研究表明,聚(γ-苄基L-谷氨酸酯)-b-聚乙二醇(PBLG-b-PEG)嵌段共聚物与PBLG 均聚物或聚苯乙烯(PS)均聚物共混自组装,可以形成棒状或球状VLPs:均聚物形成棒状或球状内核,嵌段共聚物构成外壳,并有序排列形成规整的表面纳米结构。这些聚集体的形态、结构与天然病毒相似,可以作为仿病毒材料开展性能研究。
中空纳米粒子具有高负载特性,在药物释控、催化等领域具有广泛的应用与研究价值[11-13]。模板法是制备中空纳米粒子的常用方法[14,15]。制备过程常以交联或者聚合的方式固定壳结构,经溶剂溶解除去模板后得到中空纳米粒子,这种方法简单高效、纳米粒子的结构可调控性强[16]。目前,已报道的利用模板法制备的中空纳米粒子通常缺乏规整的表面纳米结构。
本文基于聚肽共聚物自组装,制备了一种具有规整表面纳米结构的中空仿病毒粒子(HVLPs),并研究了其载药性能。利用聚(γ-苄基L-谷氨酸酯-co-肉桂基L-谷氨酸酯)-b-聚乙二醇(P(BLG/CLG)-b-PEG)嵌段共聚物与PBLG 均聚物或PS 均聚物共混自组装,形成具有核-壳结构的棒状或球状VLPs(其中均聚物构成内核,嵌段共聚物构成外壳并形成有序纳米结构);通过紫外光照射交联VLPs 壳层中肉桂酰氧基上的碳碳双键固定壳层纳米结构,并用N,N′-二甲基甲酰胺(DMF)溶解球状VLPs 的PS 均聚物内核,制备出表面具有条纹的球状HVLPs。以阿霉素(DOX)为模型药物,研究了球状HVLPs 对DOX 的负载和释放性能。本研究为制备具有规整表面纳米结构的HVLPs 提供了新策略,所制备的表面带有条纹的HVLPs 有望在药物载体等领域得到应用。
1 实验部分
1.1 试剂与仪器
PBLG-b-PEG 嵌段共聚物:PBLG 链段Mn= 3.0×104,聚合度为137,PEG 链段Mn= 5.0×103,聚合度为113,Mw/Mn= 1.12,自制[17];PBLG 均聚物:Mn= 1.7×105,Mw/Mn= 1.23,自制[18];PS 均聚物,Mn= 7.2×103,Mw/Mn=1.04,自制[7];四氢呋喃(THF)、 DMF、碳酸氢钠、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(EDC·HCl)、4-二甲氨基吡啶(DMAP)、肉桂醇(CA)、二甲基亚砜(DMSO):上海泰坦科技有限公司,直接使用;二氯乙酸(DCA):w=99%,Sigma-Aldrich 上海贸易有限公司;氢溴酸的醋酸溶液:w=33%,上海百灵威技术有限公司;实验用超纯水:电阻率为18.2 MΩ·cm,Millipore 超纯水系统制备;透析袋:截留分子量为3 500,Serva Electrophoresis GmbH 公司。
核磁共振氢谱(1H-NMR):美国布鲁克公司 Avance 400 型核磁共振仪,CDCl3-CF3COOD(体积比为5/1)为溶剂,TMS 为内标物;红外吸收光谱(FT-IR):美国热电Nicolet 5700 型傅里叶变换红外光谱仪,采用涂膜制样,测试范围是4 000~400 cm−1;紫外-可见光光谱(UV-Vis):美国瓦里安公司Lambda 950 型紫外-可见光分光光度计;扫描电子显微镜(SEM):日本日立公司(Hitachi)S-4800 型场发射扫描电镜,加速电压为10 kV,将样品溶液滴于硅片上,自然风干,测试前喷铂处理;透射电子显微镜(TEM):日本电子公司(JEOL)JEM-1400 型透射电子显微镜,加速电压100 kV,将样品滴于铜网上,自然风干。
1.2 P(BLG/CLG)-b-PEG 嵌段共聚物的合成
1.2.1 P(BLG/LGA)-b-PEG 嵌段共聚物的制备 将0.3 g PBLG-b-PEG 嵌段共聚物置于100 mL 的单口烧瓶中,加入10 mL 二氯乙酸,室温下磁力搅拌2 h。然后,取0.3 mL 氢溴酸的醋酸溶液加入到单口烧瓶中,磁力搅拌20 min 后,加入饱和的碳酸氢钠溶液,将反应液调至弱酸性。经透析、冷冻干燥后得到白色固体粉末P(BLG/LGA)-b-PEG。
1.2.2 P(BLG/CLG)-b-PEG 嵌段共聚物的制备 取0.15 g P(BLG/LGA)-b-PEG 嵌段共聚物于干燥洁净的茄型反应瓶中,以5 mL 无水DMSO 溶解。加入2 mL EDC·HCl(0.055 g/mL)和2 mL DMAP(0.025 g/mL)的DMSO溶液,磁力搅拌30 min 后,加入2 mL CA 的DMSO 溶液(0.08 g/mL)。室温下反应3 d 后,经乙醇、纯水透析并冷冻干燥得到白色粉末状固体P(BLG/CLG)-b-PEG,反应流程如图1 所示。
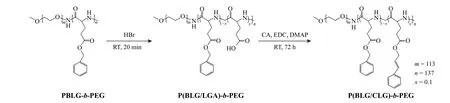
图 1 可光交联的P(BLG/CLG)-b-PEG 嵌段共聚物的合成路线Fig. 1 Synthetic route of photo-crosslinkable P(BLG/CLG)-b-PEG block copolymer
1.3 仿病毒组装体的制备
1.3.1 毛线球状仿病毒组装体的制备 将P(BLG/CLG)-b-PEG 嵌段共聚物和PS 均聚物分别以THF-DMF 混合溶剂(体积比为1/1)溶解,质量浓度均为0.5 g/L。取P(BLG/CLG)-b-PEG 嵌段共聚物溶液2 mL 与PS 均聚物溶液2 mL 混合,振荡过夜。在磁力搅拌下,以0.12 mL/min 的速率滴加1.2 mL 超纯水,通过纯水透析3 d,得到约6.4 mL“毛线球”状组装体水溶液。
1.3.2 螺旋棒状仿病毒组装体的制备 将P(BLG/CLG)-b-PEG 嵌段共聚物和PBLG 均聚物分别以THF-DMF混合溶剂(体积比为3/7)溶解,质量浓度均为0.2 g/L。取P(BLG/CLG)-b-PEG 嵌段共聚物溶液2.4 mL与PBLG 均聚物溶液1.6 mL 混合,振荡过夜。在磁力搅拌下,以0.12 mL/min 的速率滴加1.2 mL 超纯水,通过纯水透析3 d,得到约6.8 mL“螺旋棒”状组装体水溶液。
1.4 HVLPs 的制备与性能
1.4.1 HVLPs 的制备 将得到的“毛线球”状组装体水溶液(约6.4 mL)浓缩至2 mL,并加入石英试管中,置于波长λ = 254 nm 的紫外光下照射1 h(试管与紫外灯源之间的距离约15 cm),交联球状VLPs 的壳结构。取1 mL 组装体水溶液加到8 mL DMF 中,室温下搅拌15 min,以除去组装体内部的均聚物内核,得到9 mL 球状HVLPs 母液。
“螺旋棒”状组装体水溶液制备HVLPs 过程与上述操作类似。
1.4.2 载药HVLPs 的制备 向7 个样品瓶中各加入0.9 mL 球状HVLPs 母液(经计算HVLPs 的质量约50 μg),再依次加入质量浓度为0.2 g/L 的DOX 的DMF 溶液0.025、0.05、0.1、0.2、0.4、0.8 mL 和1.2 mL。分别再补加适量DMF 至各个样品瓶中,使溶液的总体积为2.1 mL,室温下搅拌4 h,然后以0.04 mL/min 的速率向各个样品瓶中滴加0.4 mL 纯水,制备负载DOX 的VLPs。此时,溶液中含有2 mL DMF 和0.5 mL 水。
将负载DOX 的VLPs 溶液以孔径为0.20 μm 的聚四氟乙烯滤膜过滤,除去VLPs,得到各个样品的滤液。通过紫外分光光度计测定吸光度,得到各滤液中游离的DOX 质量,计算出负载到VLPs 中的DOX 质量。
1.4.3 载药HVLPs 的药物释放行为 取0.9 mL 球状HVLPs 母液加入到棕色样品瓶中,加入质量浓度为0.2 g/L的DOX 的DMF 溶液1.2 mL。室温下搅拌4 h,然后以0.04 mL/min 的速率滴加0.4 mL 超纯水,得到负载DOX的VLPs。将负载DOX 的VLPs 溶液装入透析袋中,用超纯水透析3 d,得到负载DOX 的VLPs 水溶液。
将负载DOX 的VLPs 水溶液转移至装有40 mL 磷酸盐(PBS)缓冲溶液(pH = 7.4)的烧杯中,37 ℃下振荡,振荡频率100 r/min。定时取5 mL 样品,并补充5 mL PBS 缓冲液。以紫外分光光度计测定样品溶液在485 nm 的吸光度,根据DOX 在PBS 缓冲液(pH = 7.4)中的标准曲线,计算出相对应的药物累计释放量。
1.5 测试与表征
1.5.1 P(BLG/CLG)-b-PEG 嵌段共聚物的交联性能测定 将P(BLG/CLG)-b-PEG 嵌段共聚物以THF-DMF 混合溶剂(体积比为3/7)溶解,质量浓度为0.2 g/L。取该溶液20 mL,以0.6 mL/min 的速率滴加6 mL 的超纯水,经透析后得到P(BLG/CLG)-b-PEG 嵌段共聚物的聚集体水溶液。
将P(BLG/CLG)-b-PEG 嵌段共聚物的聚集体水溶液置于波长λ= 254 nm 的紫外光下照射,每隔一段时间取样,用紫外分光光度计测定样品在200~400 nm 的吸收光谱,表征其交联反应程度。
1.5.2 HVLPs 的载药性能测定 (1)DOX 标准曲线测定:以DMF-H2O(体积比4/1)为溶剂,分别配制质量浓度(ρ)为25、50、75、100、125 μg/mL 的DOX 溶液,使用紫外分光光度计测定各个溶液在485 nm 处的吸光度(A),经拟合得到DOX 吸光度和质量浓度关系的标准曲线:ρ= 53.713 06 A,R2= 0.999 3。以PBS 为溶剂,得到DOX 在pH = 7.4 的PBS 缓冲液中的标准曲线:ρ= 64.614 19 A,R2= 0.999 9。(2)VLPs 相对载药量和包封率的计算:用紫外分光光度计测定各个滤液在485 nm 处的吸光度,得到游离的DOX 质量,以DOX 投入量与游离量的差值,推出载入VLPs 的DOX 质量。通过公式(1)计算出负载于HVLPs 的DOX 质量(ms),根据公式(2)计算VLPs 的相对载药量(D),根据公式(3)计算药物的包封率(N):
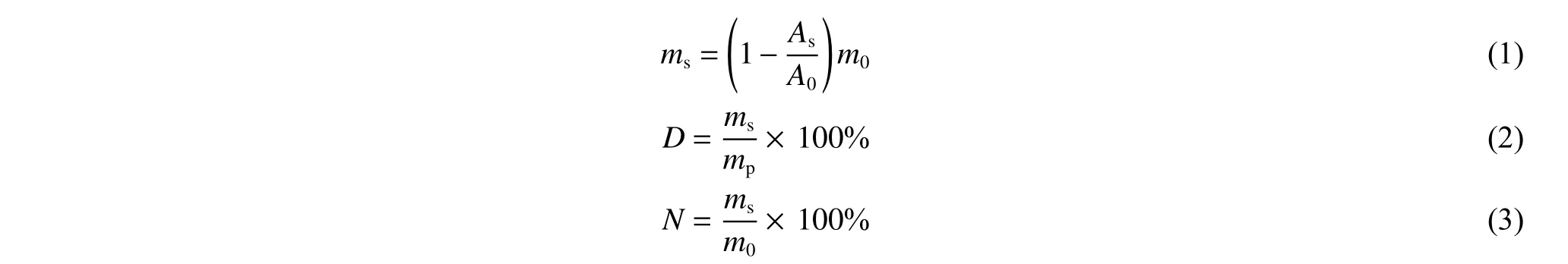
其中:A0为由标准曲线计算出DOX 对应质量浓度的吸光度;As为各个滤液的吸光度; m0为初始投入的DOX质量;ms为载入HVLPs 中的DOX 质量;mp为球状VLPs 的质量(50 μg)。
1.5.3 HVLPs 药物释放性能测定 根据不同时间DOX 的累计释放量(mt)与载入HVLPs 中的DOX 质量的比值 计算得到药物释放百分比(R):
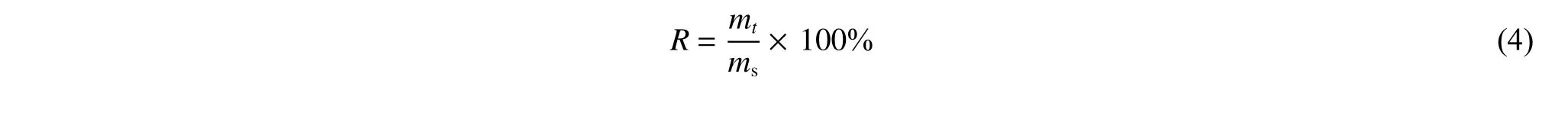
2 结果与讨论
2.1 聚合物表征
图2 为PBLG-b-PEG 和P(BLG/CLG)-b-PEG 嵌段共聚物的1H-NMR 谱图。P(BLG/CLG)-b-PEG 的谱图中在化学位移6.70、6.31 处出现了新吸收峰,这两处吸收峰分别对应于肉桂酰氧基上―CH=CH―的质子。此结果表明肉桂醇成功接枝到共聚物上。根据P(BLG/CLG)-b-PEG 谱图中化学位移5.05 与2.42 处的峰面积比值计算出脱苄基率为10.0%;再根据化学位移6.70、6.31 与2.42 处的峰面积比值,计算出肉桂酰氧基的接枝率为10.0%,表明酯化完全。
2.2 P(BLG/CLG)-b-PEG 嵌段共聚物的交联性能研究
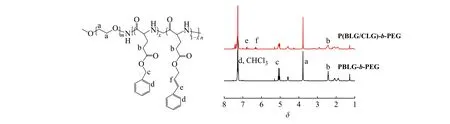
图 2 样品的1H-NMR 谱图Fig. 2 1H-NMR spectra of samples
经波长254 nm 的紫外光照射后,肉桂酰氧基上的C=C 双键之间发生[2 + 2]环加成反应[19-21],实现了聚肽链与链之间交联(图3(a))。P(BLG/CLG)-b-PEG 嵌段共聚物的紫外吸收光谱如图3(b)所示,由图可见,随着紫外光照射时间延长,284 nm 和293 nm 处归属于肉桂酰氧基上C=C 的特征吸收峰逐渐降低,说明C=C双键相互之间不断发生环加成反应,使体系中的C=C 双键不断减少。
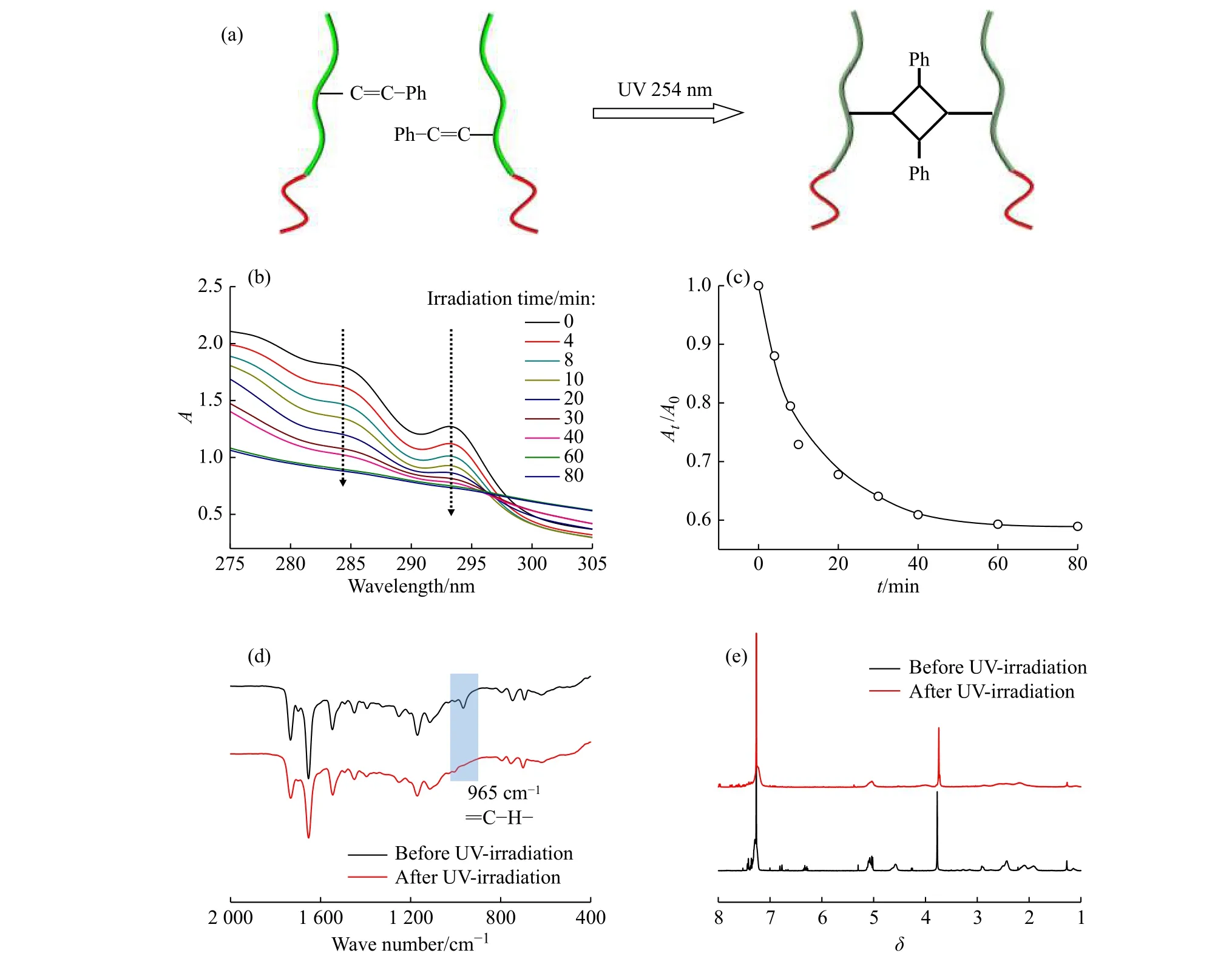
图 3 P(BLG/CLG)-b-PEG 嵌段共聚物[2+2]环加成反应示意图(a);P(BLG/CLG)-b-PEG 聚集体的紫外光照射时间-紫外吸收光谱图(b);At /A0 与紫外光照射时间的关系图(c);P(BLG/CLG)-b-PEG 紫外光照射前后的红外光谱图(d)与1H-NMR 谱图(e)(紫外光照射40 min)Fig. 3 Schematic illustration of [2 + 2] cycloaddition reaction of P(BLG/CLG)-b-PEG copolymer(a); UV-Vis spectra of aqueous solution of P(BLG/CLG)-b-PEG aggregates subjected to UV-irradiation at 254 nm as a function of irradiation time(b); Plot of At /A0 against irradiation time(c); FT-IR(d) and 1H-NMR(e) spectra of P(BLG/CLG)-b-PEG before and after UV-irradiation for 40 min
图3(c)中, A0为未经紫外光照射,紫外吸收光谱中293 nm 处的吸光度;At为t 时刻紫外吸收光谱中293 nm处的吸光度。P(BLG/CLG)-b-PEG 嵌段共聚物环加成反应过程中,在0~40 min,A /A 迅速降低,表明环加成反应迅速进行;当紫外光照射时间超过60 min 后,At/A0就趋于稳定,表明C=C 双键已经基本反应完全。
C=C 双键的交联反应也由红外光谱得到证实,如图3(d)所示。965 cm−1处为肉桂酰氧基上的=C―H 的弯曲振动峰,1 650 cm−1处为C=C 的伸缩振动峰。交联后,965 cm−1处肉桂酰氧基上=C―H 的弯曲振动吸收峰消失,这是由于紫外光照射后,PBLG 嵌段侧基上C=C 的环加成反应使肉桂酰氧基上的=C―H 消失导致;而1 650 cm−1处的峰稍有减弱,是由于1 650 cm−1处肉桂酰氧基上C=C 的伸缩振动峰与PBLG 链段的α-螺旋构象峰重叠[22]。
图3(e)为紫外光照射交联前后的P(BLG/CLG)-b-PEG 嵌段共聚物1H-NMR 谱图。由图可见,交联后,6.70、6.31 处肉桂酰氧基上的―CH=CH―质子吸收峰均消失,这也进一步证实了PBLG 嵌段侧基上的C=C双键发生了环加成反应。此外,由于环加成反应导致高分子链间发生交联,使交联的共聚物在氘代试剂中的溶解性变差,导致侧链上位于2.42、2.10、1.91 处的质子吸收峰以及主链上4.60 处的质子吸收峰出峰变得不明显。
2.3 HVLPs 的形貌表征与分析
P(BLG/CLG)-b-PEG 嵌段共聚物与PS 均聚物共混自组装得到表面具有条纹的球状VLPs(图4(a)),经254 nm 的紫外光照射后,得到壳结构固定的球状VLPs(图4(b))。将球状VLPs 水溶液加到DMF 中浸泡15 min 后,得到了球状HVLPs(图4(c))。从SEM 图可以看出,聚集体结构呈塌缩态且表面为褶皱状,表明球状VLPs 的PS 均聚物内核已被去除。TEM 观察也证实了其中空结构,如图4(d)所示,在TEM 图中聚集体呈纵横交错的明暗条纹状态,衬度差异明显。这是由于球状HVLPs 壳结构中的条纹结构相互叠加导致。
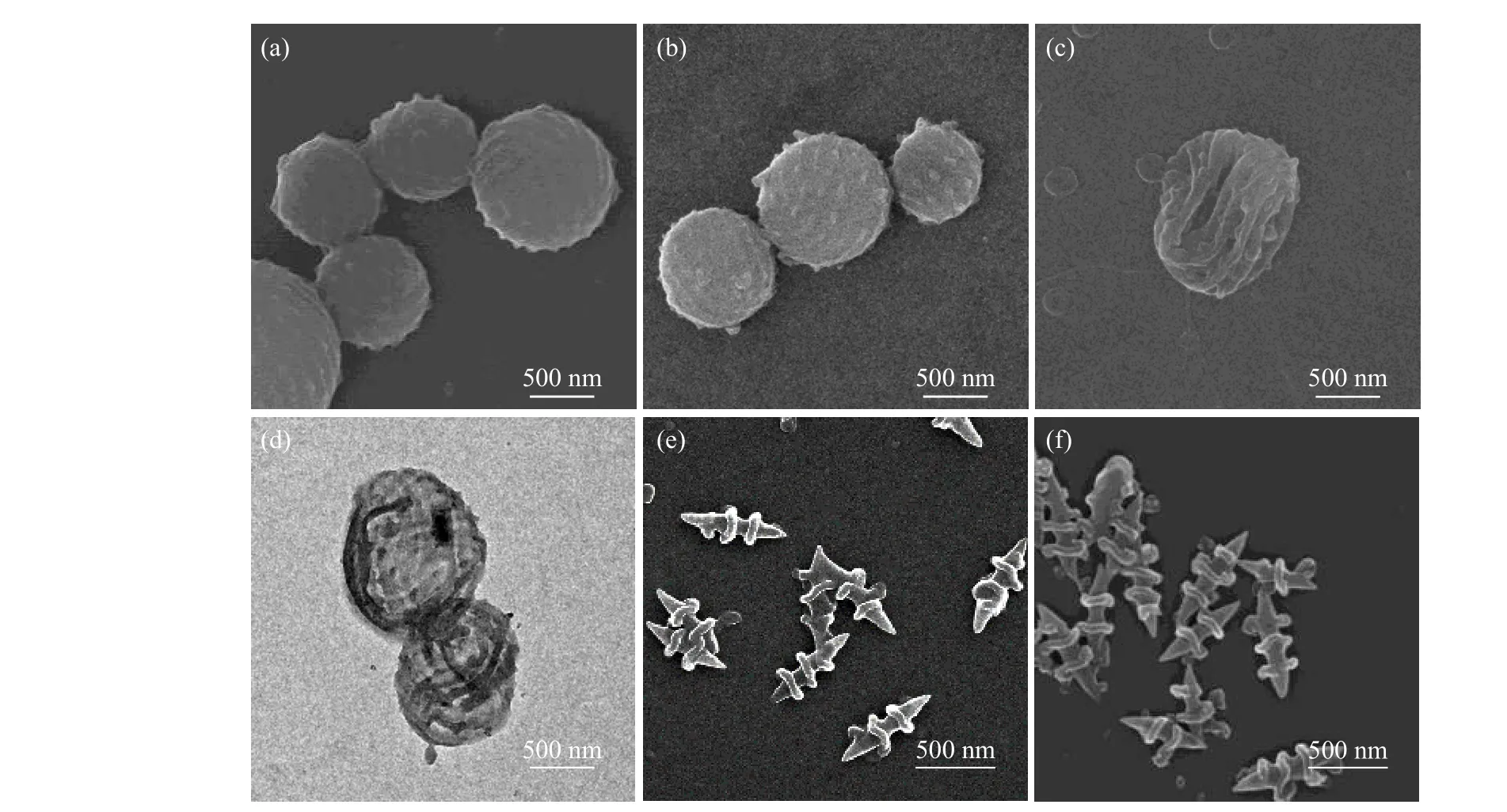
图 4 SEM 表征P(BLG/CLG)-b-PEG/均聚物共混自组装形成的聚集体形貌:交联前(a)后(b)球状VLPs;球状HVLPs 的SEM图(c)和TEM 图(d);交联前(e)后(f)棒状VLPsFig. 4 SEM images of aggregates formed by P(BLG/CLG)-b-PEG/homopolymer mixtures: Spherical VLPs before(a) and after(b) UVirradiation; Typical SEM(c) and TEM(d) images of spherical HVLPs; Rod-like VLPs before(e) and after(f) UV-irradiation
P(BLG/CLG)-b-PEG 嵌段共聚物与PBLG 均聚物共混自组装得到螺旋棒状VLPs(图4(e)),经紫外光照射后,得到壳结构固定的棒状VLPs(图4(f))。按照球状VLPs 的制备流程,将棒状VLPs 的聚集体水溶液加到大量DMF 中,观察到DMF 不能溶解棒状VLPs 的PBLG 内核,无法制备出棒状HVLPs。分析原因如下:(1)相较于“毛线球”聚集体的内核PS 均聚物,螺旋棒的内核PBLG 均聚物分子链为刚性链,运动能力较差;(2)构成“毛线球”聚集体内核的PS 均聚物分子量较小,经DMF 溶解后,易穿过交联的壳结构,而构成螺旋棒内核的PBLG 均聚物分子量较大,穿过壳结构较难。
2.4 HVLPs 载药性能研究
以DOX 为模型药物,研究了球状HVLPs 的载药性能。向球状HVLPs 和DOX 的混合溶液中加水后,疏水药物DOX 载入到HVLPs 内。DOX 在DMF-H2O(体积比为4/1)溶剂中的最大吸收波长为485 nm(图5(a));在此条件下,DOX 吸光度和质量浓度的标准曲线如图5(b)所示。
利用拟合的标准曲线计算了VLPs 的相对载药量和包封率与相对投药量之间的关系。相对投药量以DOX 的质量与DOX 和球状HVLPs 总质量的比值(fDOX)来表示。本文中,根据DOX 与VLPs 的质量,fDOX为0.09~0.83。如图5(c)所示,随着fDOX的增大,VLPs 的相对载药量也会明显增大,而包封率会降低;当fDOX=0.83 时,VLPs 的相对载药量达到230%,包封率达到48%。
在fDOX= 0.83 条件下制备得到的载药VLPs 的药物释放性能如图5(d)所示。载药VLPs 对DOX 具有较好的缓释效果,在37 ℃,pH = 7.4 条件下,0~12 h 内VLPs 的药物释放速率较快;而在12 h 以后,VLPs 的药物释放速率逐渐降低,72 h 的累计药物释放量达到80%。
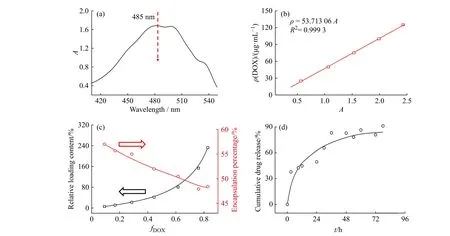
图 5 DOX 在DMF-H2O(体积比为4/1)溶剂中的紫外吸收光谱(a);DOX 在DMF-H2O(体积比为4/1)溶剂中吸光度和质量浓度的标准曲线(485 nm)(b);VLPs 的相对载药量和包封率与投药量的关系曲线(c);在fDOX = 0.83 条件下制得的载药VLPs的药物缓释曲线(d)Fig. 5 UV-Vis spectrum of DOX in DMF-H2O(Volume ratio 4/1)(a); Mass concentration-absorbance profile of DOX in DMF-H2O(Volume ratio 4/1)(485 nm)(b); Plots of drug-loading content and encapsulation percentage of DOX-loaded VLPs as a function of fDOX(c);Drug release of DOX from drug-loaded VLPs prepared with fDOX = 0.83(d)
3 结 论
(1)制备出了可光交联的P(BLG/CLG)-b-PEG 嵌段共聚物,以P(BLG/CLG)-b-PEG 分别与PBLG、PS 共混自组装,制备出具有表面纳米结构的核-壳型棒状和球状VLPs。
(2)通过有机溶剂溶解可以除去球状VLPs 的PS 均聚物内核,得到球状HVLPs;有机溶剂不能溶解除去棒状VLPs 的PBLG 均聚物内核。
(3)球状HVLPs 对DOX 具有良好的负载能力,相对载药量可以达到230%;载药的VLPs 具有一定的药物缓释性能,72 h 的药物累计释放量达到80%。
