血清炎症因子水平与进展性脑卒中的相关性分析
2020-06-02周涛侯宇峰
周涛,侯宇峰
进展性脑卒中(progressive stroke,PS)指发病1周内经过治疗后症状和体征仍逐渐加重的脑卒中,影响脑卒中患者预后[1]。PS常导致患者严重而持久的神经功能缺损,可作为预测卒中死亡的独立危险因素[1]。影响PS 的因素包括感染、血压下降、发热和糖尿病等[2]。近年来,越来越多的研究证实,PS与免疫炎症密切相关[3-5]。有研究检测202例缺血性卒中患者入院24 h、发病48 h和72 h的血清超敏C-反应蛋白(hypersensitive C-reactive protein,hs-CRP)水平,发现hs-CRP持续增长和PS的发生有关[6]。脂蛋白相关磷脂酶A2(Lipoprotein-associated phospholipase A2,Lp-PLA2)是血小板活化因子乙酰水解酶,由血管内膜中的T细胞、肥大细胞和巨噬细胞分泌。Lp-PLA2可刺激血管生成,导致斑块内出血和斑块不稳定[7]。Yang 等[7]发现血清Lp-PLA2 与CRP呈正相关,可预测前循环脑梗死颈动脉斑块的形成及其易损性。血管生成素-1(angiopoietin-1,Ang-1)是血管生长素家族成员之一,可激活酪氨酸激酶Tie抑制内皮细胞凋亡,并促进内皮细胞出芽、稳定血管[8]。Ang-1 在内皮细胞的炎症反应中发挥重要作用[9]。Lp-PLA2和Ang-1在PS中发挥何种作用,既往报道较少。本研究分析Lp-PLA2、Ang-1和hs-CRP的关系,并分析PS与Lp-PLA2、Ang-1、hs-CRP的关系。
1 资料与方法
1.1 一般资料
回顾性分析2017年4月至2018年12月本院收治的首次发作并于3 d 内住院的缺血性卒中患者326 例,均经头颅CT 或MRI 扫描证实,符合中华医学会神经病学分会制定的《中国急性缺血性脑卒中诊治指南2018》脑梗死诊断标准[10]。男215 例,女111 例;年龄38~82 岁,平均(67.25±6.39)岁。分别于入院时及发病第7天进行美国国立卫生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)评分,NIHSS 评分增加≥3 分诊断为PS[11]。根据诊断标准将326 例缺血性卒中患者分为PS 组(n=124)和非PS 组(n=202)。排除标准:出血性卒中;瘤卒中;急慢性感染性疾病;免疫系统疾病;严重的心肝肾等重要脏器功能障碍。本研究经医院伦理委员会审批通过,所有受试者知情同意。
1.2 方法
记录所有患者的临床资料,包括入院时血压、血糖、血脂、基础疾病。入院时进行NIHSS 评分[12]。采用Vivid7 全数字彩色多普勒超声诊断仪(美国GE 公司)检测颈动脉狭窄情况。患者发病后72 h内采用采用瑞士进口罗氏cobas8000全自动生化分析仪检测血清中hs-CRP 水平,采用美国伯腾仪器有限公司生产的ELX800 酶标仪检测血清Lp-PLA2和Ang-1。相关试剂盒均购于上海生物工程有限公司。根据四分位数水平将PS 患者分为低水平组、中水平组和高水平组。
1.3 统计学处理
采用SPSS19.0统计学软件分析数据。正态分布的计量资料以(±s)表示,t检验;计数资料以例或百分比表示,χ2检验或Fisher确切概率法;相关性检验用Pearson分析,单因素分析有统计学意义的则纳入多因素分析,多因素分析采用Logistic回归模型。P<0.05为差异有统计学意义。
2 结果
2.1 2组一般资料比较
PS 组合并高血压例数、颈动脉狭窄例数、入院时收缩压、入院时血糖和入院时NIHSS评分均高于非PS组,差异有统计学意义(P<0.05),见表1。
2.2 2组入院时Lp-PLA2、Ang-1、hs-CRP水平比较
PS 组入院时Lp-PLA2 和hs-CRP 水平均高于非PS 组(P<0.05),Ang-1水平低于非PS组(P<0.05),见表1。对326例患者Lp-PLA2、Ang-1 和hs-CRP 水平进行相关性分析,结果表明Lp-PLA2 与hs-CRP 呈 正 相 关(r=6.354,P=0.002),Ang-1 与hs-CRP呈负相关(r=-4.002,P=0.038)。
2.3 多因素Logistic回归分析结果
多因素Logistic回归分析结果显示,高血压、颈动脉狭窄、入院时收缩压、血糖、NIHSS评分、Lp-PLA2、Ang-1和hs-CRP水平是影响PS的独立影响因素(P<0.05),见表2。
3 讨论
PS目前并无统一定义,本研究分别于入院时及发病第7天进行NIHSS 评分,NIHSS 评分增加≥3 分诊断为PS,这是国内外较为公认的PS定义[13-15]。既往研究发现,PS的发病可能与合并基础疾病、梗死部位、梗死体积、出血性转换、血糖水平和兴奋性中毒等有关[16]。既往研究已证实,炎症与PS 发生有关[17]。hs-CRP 是由肝脏合成的一种全身性炎症反应急性期的非特异性标志物,是心血管事件危险最强的预测因子之一。李进军等[18]发现hs-CRP与缺血性脑卒中患者早期神经功能恶化有关,并且hs-CRP 与NIHSS 评分及纤维蛋白原有关。本研究将326 例缺血性卒中患者分为PS组和非PS组,发现hs-CRP是预测PS的独立影响因素,提示炎症是影响PS的重要因素。
Lp-PLA2是缺血性脑卒中发病的危险因素,可成为缺血性脑卒中的预测指标和评估病情严重程度的指标[19,20]。Lp-PLA2水平的变化与炎症反应和氧化应激反应密切相关[21],其作为血管炎症关键启动子的作用与hs-CRP相互协同[21]。抑制Lp-PLA2的药物可以降低动脉粥样硬化斑块形成及心脑血管疾病风险[7]。Lp-PLA2水平与PS关系的研究较少,本研究发现,Lp-PLA2水平与Hs-CRP水平呈正相关。进一步Logistic分析发现,Lp-PLA2是影响PS的独立预测因素。李善敬等[22]采用醒脑静注射液治疗PS后,Lp-PLA2水平明显下降,一定程度上反映Lp-PLA2与PS有关。
Ang-1 是血管生长素家族成员之一,在内皮细胞的炎症反应中发挥重要作用[9]。方丽萍等[23]发现预后良好的急性缺血性脑卒中患者血清Ang-1表达水平高于预后不良患者,提示Ang-1与急性缺血性脑卒中良好预后有关。本研究发现Ang-1表达水平与hs-CRP呈正相关,并且与PS密切相关。Ang-1水平与颈动脉粥样硬化性质及狭窄程度密切相关,随着动脉粥样硬化斑块严重性增加,Ang-1 水平逐渐降低[24]。因此笔者推测,Ang-1 水平降低可能作为一个间接因素,通过促进动脉硬化发展以促进高血压和糖尿病的发展,增加PS风险。
综上所述,炎症是PS 发病的重要因素。本研究发现,Lp-PLA2、Ang-1、hs-CRP 与PS 有关,Lp-PLA2、Ang-1、hs-CRP是PS的独立危险因素,三者联合检测可能会提高预测价值,未来需要进一步开展前瞻性研究以证实本研究结论。
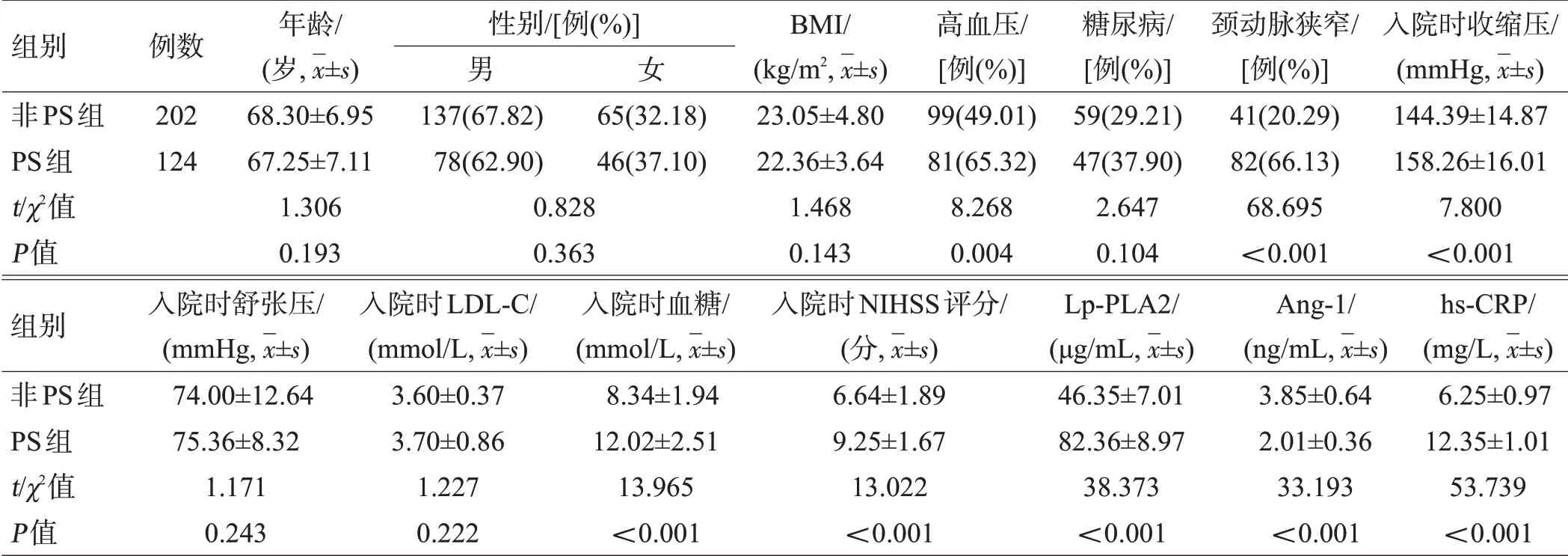
表1 2组一般资料比较
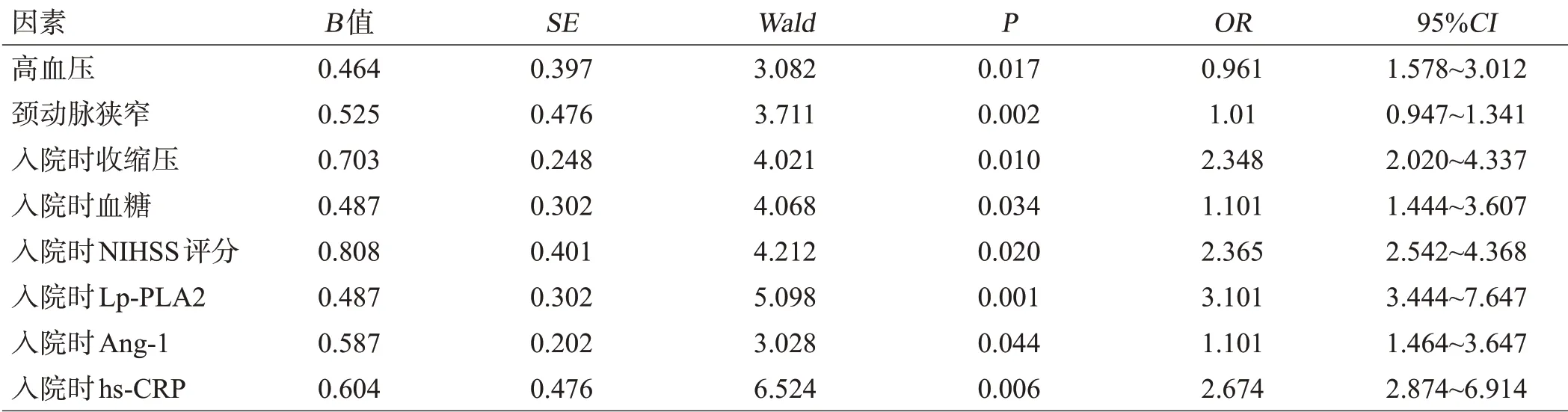
表2 多因素Logistic回归分析血清Lp-PLA2、Ang-1、hs-CRP水平与PS关系
