多西他赛联合顺铂同期放化疗治疗宫颈癌的临床疗效及急性毒性反应评价
2020-06-01王斌张圳妙曾志坚
王斌 张圳妙 曾志坚
【摘要】 目的 观察多西他赛联合顺铂同期放化疗治疗宫颈癌的临床疗效及急性毒性反应。
方法 96例宫颈癌患者, 随机分为单独组和联合组, 各48例。单独组给予顺铂单药参与化疗, 联合组给予多西他赛联合顺铂同期放化疗。对比两组患者急性毒性反应(血液学毒性及下消化道反应)发生情况、临床疗效。结果 單独组血液学毒性反应分级0级6例、Ⅰ级4例、Ⅱ级20例、Ⅲ级18例、Ⅳ级0例;联合组血液学毒性反应分级0级7例、Ⅰ级10例、Ⅱ级21例、Ⅲ级10例、Ⅳ级1例;两组血液学毒性反应分级情况对比, 差异无统计学意义(P>0.05)。单独组下消化道反应分级0级13例、Ⅰ级21例、Ⅱ级0例、Ⅲ级0例、Ⅳ级0例;联合组下消化道反应分级0级0例、Ⅰ级34例、Ⅱ级11例、Ⅲ级3例、Ⅳ级0例;两组下消化道反应分级情况对比, 差异具有统计学意义(P<0.05)。联合组治疗总有效率95.8%高于单独组的83.3%, 差异具有统计学意义(P<0.05)。结论 在宫颈癌治疗中使用多西他赛联合顺铂同期放化疗不会增加机体血液学毒性反应, 但会导致机体产生腹胀、便血等下消化道反应。总体来说, 患者对联合用药化疗有一定的耐受性, 不会导致治疗时间的延长, 治疗效果也较好。
【关键词】 宫颈癌;顺铂;多西他赛;放化疗;急性毒性反应
DOI:10.14163/j.cnki.11-5547/r.2020.13.056
放化疗是宫颈癌治疗的主要手段[1]。进一步探索同期放化疗方案, 减少机体急性毒性反应产生, 增强放疗效果, 缩短放疗疗程, 是当下宫颈癌放化疗研究的重点[2]。基于此, 本文研究了多西他赛联合顺铂同期放化疗治疗宫颈癌的临床疗效及急性毒性反应, 总结报告如下。
1 资料与方法
1. 1 一般资料 选取2018年1月~2019年7月本院收治的96例宫颈癌患者。纳入标准:①比照国际妇产科协会修订的国际妇产科联盟(FIGO)2009分期标准, 符合宫颈癌诊断标准;②经>2个医生妇科查体, 联合磁共振成像(MRI)、CT检查, 证实属于宫颈癌;③患者均知情同意。排除标准:①合并精神障碍者;②治疗依从性差者;③合并其他系统的严重疾患危及生命者;④中途退出者。将患者随机分为单独组和联合组, 每组48例。单独组:年龄32~58岁, 平均年龄(37.85±6.72)岁;联合组:年龄35~71岁, 平均年龄(39.75±10.42)岁。两组患者一般资料对比, 差异无统计学意义(P>0.05), 具有可比性。
1. 2 方法 所有患者采用适形放疗(IM-RT)技术或三维适形放疗(3-DCRT)进行化疗, 5次/周, 放疗结束后, 间隔2~3周, 行宫颈癌根治术。根治方式, 全盆50 Gy/25 F, 配合后装治疗。1次/d, 一周连续治疗5 d。
单独组给予顺铂单药(山东凤凰制药股份有限公司, 国药准字H20056422, 规格:20 mg)参与化疗。给药前2~16 h, 给予水化治疗。以无菌生理盐水或浓度为5%葡萄糖溶液稀释, 行静脉滴注。1次/周, 40 mg/(m2·次)。持续治疗5~6周。
联合组除顺铂外, 添加多西他赛(江苏奥赛康药业有限公司, 国药准字H20064301, 规格:0.5 ml∶20 mg)联合化疗。给药参与化疗前, 连续3 d口服地塞米松等糖皮质激素类, 避免发生过敏反应和体液潴留。多西他赛使用剂量为? mg/(m2·次), 顺铂使用剂量同单独组, 遵医嘱混合多西他赛与顺铂。将混合液注入浓度为5%葡萄糖注射液或浓度为0.9%氯化钠注射液的注射瓶或注射袋中, 轻轻摇动, 混合均匀, 最终浓度≤0.9 mg/ml。治疗:1次/3周, 持续治疗2个周期。
1. 3 观察指标及判定标准
1. 3. 1 急性毒性反应发生情况 依据急性放射性损伤分级标准(RTOG)评估患者血液学毒性及下消化道反应等急性毒性反应发生情况。①血液学毒性反应分级标准:0级:无出血, 血红蛋白(g/L)≥110, 白细胞(×109/L)≥4.0, 粒细胞(×109/L)≥2.0, 血小板(×109/L)≥100;Ⅰ级:有瘀点, 血红蛋白(g/L)在95~109之间, 白细胞(×109/L)在3.0~3.9之间, 粒细胞(×109/L)在1.5~1.9之间, 血小板(×109/L)在75~99之间;Ⅱ级:轻度出血:血红蛋白(g/L)在80~94之间, 白细胞(×109/L)在2.0~2.9之间, 粒细胞(×109/L)在1.0~1.4之间, 血小板(×109/L)在50~74之间;Ⅲ级:明显失血, 血红蛋白(g/L)在65~79之间, 白细胞(×109/L)在1.0~1.9之间, 粒细胞(×109/L)在0.5~0.9之间, 血小板(×109/L)在25~49之间;Ⅳ级:严重失血, 血红蛋白(g/L)<65, 白细胞(×109/L)<1.0, 粒细胞(×109/L)<0.5, 血小板(×109/L)<25。②下消化道反应分级标准:0级:无变化;Ⅰ级:大便次数增多或大便习惯改变, 无需用药;Ⅱ级:腹泻, 腹痛, 粘液分泌增多;Ⅲ级:腹泻或重度分泌粘液、血液分泌物增多;Ⅳ级:急性或亚急性肠梗阻或胃穿孔。
1. 3. 2 临床疗效 以完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)4个等级评估患者的初步治疗效果。其中, CR:靶向病灶完全消失, 且未产生新病灶, 肿瘤标志物持续4周以上表现正常;PR:靶向病灶最大直径缩小≥30%, 且持续4周以上;SD:靶向病灶最大直径缩小<30%或增大≤20%;PD:靶向病灶最大直径增加>20%, 或是由新病灶产生。总有效率=(CR+PR+SD)/总例数×100%。
1. 4 统计学方法 采用SPSS22.0统计学软件对数据进行统计分析。使用K-S检验确定变量的分布类型, 符合正态分布的计量资料以均数±标准差( x-±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验, 等级计数资料采用秩和检验。P<0.05表示差異具有统计学意义。
2 结果
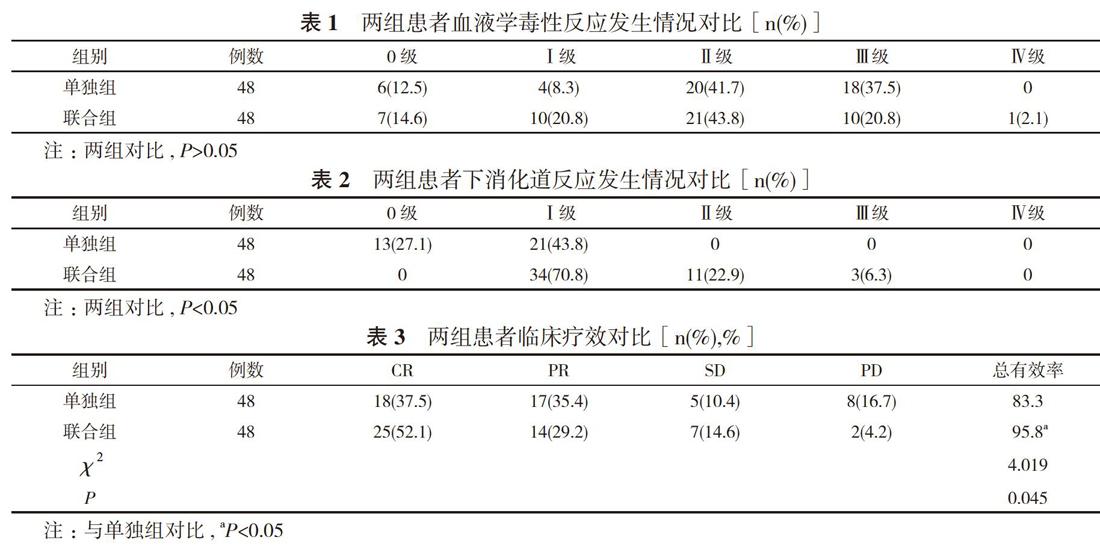
2. 1 两组患者急性毒性反应发生情况对比 两组血液学毒性反应分级情况对比, 差异无统计学意义(P>0.05);两组下消化道反应分级情况对比, 差异具有统计学意义(P<0.05)。见表1, 表2。
2. 2 两组患者临床疗效对比 联合组治疗总有效率高于单独组, 差异具有统计学意义(P<0.05)。见表3。
3 讨论
化疗药物的剂量高低直接影响机体产生的急性毒性反应的强弱[3]。在既往宫颈癌治疗中, 常以75 mg/m2剂量, 每隔3周实施一次多西他赛联合顺铂开展放化疗同期治疗[4-6]。有相关文献表明[7], 在这样的剂量下, Ⅲ度、Ⅳ度的骨髓抑制发生率高达48.8%, 而粒细胞减少发生率为11.4%。在下消化道反应方面, 发生Ⅲ度腹泻的几率为15.9%[8]。这些急性毒性反应均会导致放疗中断, 延长放疗时间。而经过对宫颈癌细胞系的放化疗研究发现, 使用多西他赛参与到同期放化疗过程, 会显著提升放疗效果, 但对于联合化疗的剂量高低, 临床研究尚未有明确定论[9, 10]。
本文研究显示, 在急性毒性反应方面, 两组血液学毒性反应分级情况对比, 差异无统计学意义(P>0.05);两组下消化道反应分级情况对比, 差异具有统计学意义(P<0.05)。在临床疗效方面, 联合组治疗总有效率高于单独组, 差异具有统计学意义(P<0.05)。证明与单独使用顺铂实施放化疗相比, 多西他赛联合顺铂实施同期放化疗, 不会增加急性毒性反应, 不会影响放疗总疗程, 有较好的疗效。
综上所述, 在宫颈癌治疗中使用多西他赛联合顺铂同期放化疗, 不会增加机体血液学毒性反应, 但会导致机体产生腹胀、便血等下消化道反应增加。总体来说, 患者对联合用药化疗有一定的耐受性, 不会导致治疗时间的延长, 治疗效果也较好。
参考文献
[1] 周晖, 白守民, 林仲秋. 《2019 NCCN宫颈癌临床实践指南(第1版)》解读. 中国实用妇科与产科杂志, 2018, 34(9):1002-1009.
[2] 田鲜艳, 李荣岗, 曾涌波. 高危宫颈癌术后调强放疗同期化疗与序贯化疗的对比研究. 广东医科大学学报, 2018, 36(4):460-462.
[3] 欧宝权. 紫杉醇联合奈达铂同期放化疗及巩固化疗治疗中晚期宫颈癌的临床疗效观察. 现代医学与健康研究电子杂志, 2017, 1(9):73-75.
[4] 蔡蕊. 苦参碱注射液对宫颈癌患者化疗增敏作用及对血清IL-6和T细胞免疫的影响. 现代中西医结合杂志, 2016, 25(26):2937-2939.
[5] 董格, 张文先, 罗琼, 等. 局部晚期宫颈癌患者化疗前后血清VEGF、CEA和SCC-Ag水平变化及其与化疗敏感性的相关性分析. 标记免疫分析与临床, 2019(3):45-67.
[6] 雷婷, 李明, 蔡宗波, 等. 多西他赛或紫杉醇联合奈达铂在宫颈癌辅助化疗中的疗效及安全性分析. 现代生物医学进展, 2018, 18(11):172-176.
[7] 赵昌芹, 张瑞林. 局部晚期宫颈癌化疗及预后与化疗前免疫功能及血小板的相关性. 热带医学杂志, 2019, 19(1):82-85.
[8] 王琰, 申沛. 顺铂与洛铂联合紫杉醇应用于宫颈癌辅助化疗的毒副反应对比研究. 山西医药杂志, 2018, 47(20):57-59.
[9] Matsuo K, Shimada M, Aoki Y, et al. Comparison of adjuvant therapy for node-positive clinical stage IB-IIB cervical cancer: Systemic chemotherapy versus pelvic irradiation. International Journal of Cancer, 2017, 141(5):1042-1051.
[10] 余一锋. 奈达铂与顺铂同期放疗治疗中晚期宫颈癌的疗效及不良反应观察. 中国实用医药, 2018, 13(25):105-106.
[收稿日期:2019-10-16]
