鞣花酸提升小鼠肌肉功能的研究及机制探讨
2020-06-01芦宇婷周仙杰吕裕霞鲁飞翔刘庆春
芦宇婷,李 军,周仙杰,吕裕霞,鲁飞翔,刘庆春
机体骨骼肌随着疾病、衰老等因素发生结构和功能的衰退,使骨骼肌持续流失,通常表现为肌肉在运动乃至日常行为中无法保持正常的力量水平,引起机体生物调节紊乱,导致机体疲劳感增强等问题[1,2]。营养干预是预防肌肉衰退、提升抗疲劳性的重要手段之一,因此,发掘能够增强肌肉功能、抗疲劳的营养物质尤为重要[3]。鞣花酸(ellagic acid,EA)是植物中存在的一种天然多酚化合物,经肠道微生物代谢产生尿石素,通过被动扩散的吸收机制发挥生物学效应[4-7]。作为一种植物性天然化合物,EA药理活性丰富[8-12],有研究表明,健康志愿者通过补充富含EA的石榴汁使得力量恢复能力得以提升,减轻了运动引起的肌肉酸痛[13,14],因此,研究EA对肌肉功能的影响具有实际意义。但目前EA对机体肌功能及抗疲劳等方面的研究尚少,仍需进一步研究。
本研究旨在通过对小鼠肌肉量、肌力、疲劳掉落次数,肌纤维横截面积大小及与蛋白质降解相关的基因肌肉特异性环指蛋白1(muscle RING finger 1,MuRF1)和肌肉萎缩基因Fbox-1(muscle atrophy f-box,MAFbx/Atrogin-1)相对表达量的检测[15],探讨EA对正常小鼠体成分、肌肉功能、运动耐力,以及抗疲劳性等方面的作用。
1 材料与方法
1.1 实验动物及分组 16只6周龄雄性清洁级ICR小鼠,体重(30.7±2.9) g,购自北京维通利华实验动物技术有限公司,许可证编号SCXK(京)2016-0006,饲养于灾害救援基础医学中心。按照国家标准啮齿类试验动物饲养,在(23±2)℃恒定室温、12 h明暗交替环境下,实验动物自由饮水、摄食。动物实验经动物福利委员会审批。
1.2 实验动物EA干预 实验动物适应性饲养一周后进行简单随机分组,实验组和对照组,每组各8只。精准称量体重后,利用Echo MRITM小动物体成分分析仪(中国汇佳生物股份有限公司)检测体实验动物成分。检测结束当天,给予实验组动物纯度99.3%的EA(南京道斯夫生物科技有限公司),用0.5%的羟甲基纤维素钠(北京索莱宝科技有限公司)溶液配制EA干预溶液,每毫升EA干预溶液中含10 mg EA,实验组和对照组小鼠分别给予EA溶液和等体积的0.5%羟甲基纤维素钠溶液进行灌胃干预。参考以往试验剂量[16],EA灌胃剂量为10 mg/100 g体重,灌胃体积为1 ml/100 g体重,1次/d,干预溶液现用现配。
1.3 实验动物体成分检测 实验动物称重后,放置于相应规格的透明塑料动物仓中,将动物仓插入Echo MRITM分析仪内,设置精度3,即6次信号采集,通过扫描得到小鼠的肌肉含量。EA干预前和干预结束12 h后各进行一次检测。
1.4 小鼠四肢肌力测定 用YLS-13A大小鼠抓力仪(北京众实迪创科技发展有限责任公司)测定小鼠四肢肌力,测定抓力前让小鼠在抓力仪上适应3 min,将抓力仪设置为测定状态,确定小鼠四只脚掌都完全抓牢后,抓住小鼠尾巴末梢平稳向后拉动,记录抓力仪读数。每只小鼠测定3次抓力(g),取3次抓力平均值作为评估肌力的指标,EA干预前和干预结束12 h后各进行一次检测。
1.5 小鼠肌肉功能测定 用YLS-4C轮转式疲劳仪(北京众实迪创科技发展有限责任公司)测定小鼠肌肉功能,预实验摸索出YLS-4C轮转式疲劳仪最佳轮转速度和时间,仪器启动前将小鼠置于滚轮上,启动仪器,设置轮转式疲劳仪转速为35 r/min,待转速稳定后,使小鼠适应1 min,开始计时,10 min计为一周期,每个周期结束后休息1 min,记录小鼠在10 min内的掉落次数,重复3次[17]。EA干预前和干预结束12 h后各进行一次检测。
1.6 HE染色测定腓肠肌横截面积 干预结束后,分离小鼠后腿两侧腓肠肌。将腓肠肌浸入10%甲醛固定液(北京索莱宝科技有限公司)中固定用于制作石蜡切片。HE染色后,应用LEICA图像采集系统随机选取5个视野进行图像采集。每个图像选取10个肌纤维,利用Image J软件计算各个肌纤维横截面积。
1.7 qRT-PCR检测实验动物腓肠肌中MuRF1基因表达 小鼠单侧腓肠肌放入RNase-Free管中加液氮充分研磨,根据组织总RNA提取试剂盒说明进行总RNA提取。利用琼脂糖凝胶电泳、NanoDrop微量分光光度计评估RNA的完整性和纯度。将总RNA反转录为cDNA,并在逆转录过程中将RNA浓度调整一致(100 ng/20 μl)。构建25 μl qRT-PCR反应体系,采用以下条件进行qRT-PCR实验:94 ℃预变性2 min,94 ℃ 20 s、58 ℃ 20 s、72 ℃ 20 s条件下35个循环,72 ℃总延伸2 min。引物序列参照以往文献[15],其中GAPDH为内参基因,每个样品设置3个平行组。

2 结 果
2.1 小鼠干预前后体重和体成分比较 EA干预前,两组小鼠体重和体成分(肌肉含量、脂肪含量)差异无统计学意义。干预后两组间小鼠体重和体成分也未观察到统计学差异,与之前报道的结果相似[3, 18]。由此可见,EA对小鼠体重和体成分无明显影响(表1)。


观察指标例数实验前实验后P体重 对照组830.03±3.1333.58±4.020.425 实验组831.29±2.9335.15±3.63脂肪含量 对照组82.53±0.943.38±0.990.393 实验组82.24±0.442.91±1.11肌肉质量 对照组822.49±3.0724.31±3.450.534 实验组823.99±2.1425.28±2.56
2.2 小鼠干预前后四肢抓力和肌肉功能比较 EA干预前,两组小鼠抓力无统计学差异。干预结束后,与对照组相比,实验组小鼠抓力增强,差异有统计学意义(P<0.001)。实验开始前,两组小鼠30 min轮转疲劳仪掉落次数没有差异。EA干预后,与对照组相比,实验组掉落次数减少,差异有统计学意义(P<0.001,表2)。

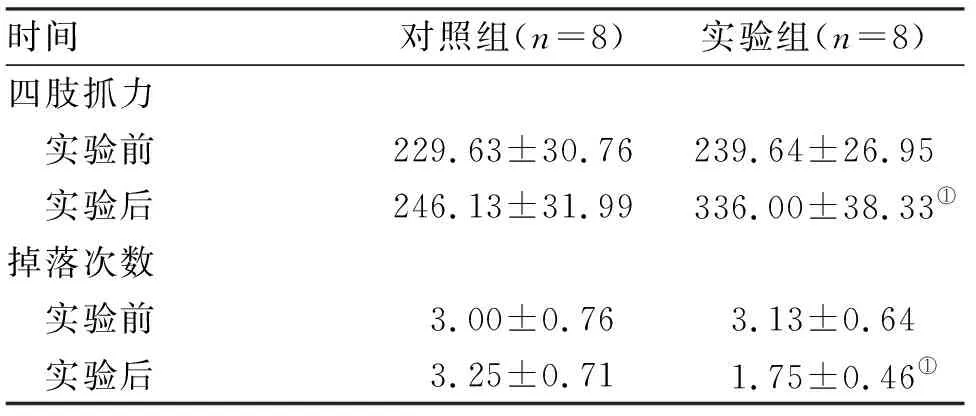
时间对照组(n=8)实验组(n=8)四肢抓力 实验前229.63±30.76239.64±26.95 实验后246.13±31.99336.00±38.33①掉落次数 实验前3.00±0.763.13±0.64 实验后3.25±0.711.75±0.46①
注:与对照组比较,①P<0.001
2.3 小鼠干预后腓肠肌肌纤维横截面积比较 干预后,实验组腓肠肌肌纤维排列较对照组更加紧密(图1)。实验组肌纤维横截面积为(1248.96±103.57)μm2,对照组为(1167.43±82.53)μm2,与对照组相比,实验组小鼠横截面积增加,差异有统计学意义(P<0.05)。

A.对照组;B.实验组
2.4 小鼠干预后腓肠肌中MuRF1和Atrogin-1基因的相对表达量比较 实时荧光定量PCR的结果显示,实验组MuRF1和Atrogin-1基因的相对表达量(0.99±0.15、0.96±0.16)(1.48±0.39、1.45±0.09)均低于对照组,差异有统计学意义(P<0.05)。
3 讨 论
骨骼肌是人体非常重要的肌群,多种疾病的发生都伴随着骨骼肌质量的流失和功能的退化[19]。肌肉量降低导致肌肉功能受损,对老年人而言会使其活动能力下降,并伴随着多种慢性病的发生,严重者甚至导致平衡障碍、起坐困难、跌倒骨折等意外风险,严重影响了老年人生存质量。对于中等及以上体力劳动的成人而言,肌肉质量减少会引起疲惫乏力、免疫功能下降、记忆力衰退、睡眠质量不佳等多方面危害,影响了日常生活和工作效率[3]。有研究表明[20],萎缩或者废用的肌肉可以在不同辅助治疗后得以再生,辅助性营养治疗可以减轻肌肉损伤、增强肌功能以及缓解疲劳[21]。
本实验通过给予小鼠EA干预,研究其对小鼠肌肉功能的影响。结果显示,EA干预后,小鼠的抓力增加和疲劳仪掉落次数减少,同时小鼠腓肠肌肌纤维横截面积增加。其中实验组小鼠腓肠肌肌纤维横截面积增加,可能原因:一是腓肠肌以Ⅱ型肌纤维为主[22],本实验条件下EA的干预可能导致Ⅱ型肌纤维变大,使肌纤维横截面积增加。Ⅱ型肌纤维与肌肉力量相关,本实验中EA干预后实验组小鼠抓力增强,便验证了这种可能性。二是腓肠肌虽然以Ⅱ型肌纤维为主,但也含有Ⅰ型肌纤维,且小鼠Ⅰ型肌纤维较Ⅱ型肌纤维粗。在特定条件下,Ⅰ型肌纤维会向Ⅱ型肌纤维转化[23],当Ⅰ型肌纤维向Ⅱ型肌纤维转化速度降低时,可能也会出现肌纤维横截面积增加的情况,这与本研究EA干预后实验组小鼠肌纤维横截面积大于对照组的结果相一致。Ⅰ型肌纤维与肌肉的耐力和抗疲劳性呈正相关[22],与正常速度转化的对照组比较,实验组Ⅰ型肌纤维在肌肉中的比例相对较大,我们猜测EA干预后Ⅰ型肌纤维向Ⅱ型肌纤维转化速度降低,本实验中实验组小鼠掉落次数降低,即实验组小鼠抗疲劳性和耐力更好。
此外, MuRF1和Atrogin-1基因在mRNA水平表达明显上调,常作为骨骼肌萎缩早期的分子标记物,本研究对腓肠肌中MuRF1和Atrogin-1基因的表达进行了检测。实验结果显示,EA干预后,实验组小鼠MuRF1和Atrogin-1基因的相对表达量降低。这表明本实验条件下EA的干预对小鼠肌肉的代谢可能具有有益作用。
综上所述,在行为学水平上,EA可以增加小鼠肌力,提升小鼠耐力及抗疲劳性;在组织病理学水平上,EA的干预可以增加肌纤维横截面积;在基因水平上,EA干预可能通过泛素蛋白酶途径,下调控制肌肉代谢的MuRF1和Atrogin-1的基因表达水平,缓解肌肉分解代谢,进而改善肌肉功能。未来我们将研究重心放在临床,进一步探究EA对不同人群肌肉质量、肌力以及肌肉功能等方面的影响,为以EA为主要原料的功能性食品的研发以及肌肉代谢疾病的预防与治疗提供基础研究及临床试验依据。
