含硼替佐米的化疗方案对多发性骨髓瘤患者的效果与不良反应研究
2020-05-28罗泉芳王薇陈钦玭庞爱萍
罗泉芳 王薇 陈钦玭 庞爱萍
多发性骨髓瘤(multiple myeloma)是由于浆细胞恶性增殖而引起的血液系统肿瘤,可导致机体血液中异常免疫球蛋白大量增生,不断引发患者出现贫血、骨破坏、机体感染以及高钙血症和肾功能不全等[1]。其发病率仅次于淋巴瘤,约占全部恶性血液系统肿瘤的10%~15%,占所有癌症的1%[2]。中老年人群是多发性骨髓瘤的高发人群,然而,此疾病目前还无法治愈,传统治疗方案针对于多发性骨髓瘤的临床效果有限,如完全缓解率较低,生存时间较短等,严重影响患者的日常生存质量和生命周期[3]。近年来,以硼替佐米为代表的一系列蛋白酶体抑制剂的新型药物相继问世,显著地是提高了多发性骨髓瘤患者的临床疗效及预后效果,尤其是以硼替佐米+环磷酰胺+地塞米松组合而成的BCD化疗方案,更是具有不良反应小、性价比高、疗效确切等特点,被广泛用于多发性骨髓瘤的临床治疗。2017年美国NCCN癌症指南中将BCD方案推荐为初诊多发性骨髓瘤的一线治疗方案,推荐级别为2A类[4]。因此,本文探讨BCD方案治疗多发性骨髓瘤的临床效果以及可能发生的不良反应,报告如下。
1 资料与方法
1.1 一般资料 选取2015年4月至2018年4月在我院住院治疗的52例多发性骨髓瘤患者作为研究对象,根据治疗方案选择的不同分为观察组和对照组,每组26例。观察组:男16例,女10例;年龄44~78岁,平均年龄(66.23±3.47)岁;Durie-Salmon分期:ⅡA期2例,ⅢA期16例,ⅢB期8例。对照组:男15例,女11例;年龄42~77岁,平均年龄(67.88±4.15)岁;Durie-Salmon分期:ⅡA期1例,ⅢA期17例,ⅢB期8例。2组患者性别比、年龄和Durie-Salmon分期差异无统计学意义(P>0.05),具有可比性。
1.2 纳入与排除标准
1.2.1 纳入标准:患者需符合《中国多发性骨髓瘤诊治指南(2017版)》[5]的相关要求,均为初发活动型(症状性)骨髓瘤:①骨髓中的浆细胞比例>30%,或组织病理检测为浆细胞瘤;②血清单克隆免疫球蛋白(M蛋白):IgG≥35 g/L,IgA≥20 g/L,或者24 h尿蛋白>1 g。
1.2.2 排除标准:①临床表现为骨痛,影像学检查发现有虫蚀样溶骨性损害病灶;②属于无症状性骨髓瘤或不分泌型骨髓瘤以及浆细胞白血病者;③近期接受过输注血液制品者;④存在其他免疫疾病或者过敏性疾病等;⑤合并有其他肿瘤或者脏器功能障碍者。
1.3 治疗方法 对照组患者采用常规疗法,即硫酸长春新碱+地塞米松+盐酸表柔比星,以静脉滴注方式给药,设定硫酸长春新碱的日用量为0.4 mg,于治疗第1~4天时连续给药;地塞米松的日用量为20 mg,于治疗第1~4、9~12、17~20天时连续给药;盐酸表柔比星的日用量为10 mg,在治疗第1~4天时连续给药;按照上述治疗方式持续28 d为1个疗程,连续3个疗程进行治疗[6]。观察组患者采用BCD(硼替佐米+地塞米松+环磷酰胺)方案进行治疗,设定硼替佐米的日用量为1.0~1.3 mg/m2,于治疗第1、4、8、11天时给药;环磷酰胺的日用量为400 mg/m2,于治疗第1、8天时给药;地塞米松的日用量为20~40 mg,于治疗第1~2天、第4~5、第8~9、第11~12时给药。同样以28 d为1个疗程,连续3个疗程进行治疗[7]。2组患者在治疗期间均给予止吐护肝等支持性治疗,以及服用双磷酸盐治疗骨损伤。
1.4 评价指标
1.4.1 参照国际多发性骨髓瘤工作组制定的评价标准进行短期疗效评估[8]:①完全缓解(CR):血尿指标呈现阴性,软组织浆细胞瘤消失,M蛋白阴性,骨髓浆细胞比例<5%;②基本完全缓解(VGPR):M蛋白水平下降>90%,24 h尿蛋白水平<0.1 g;③部分缓解(PR):M蛋白水平下降>50%,24 h尿蛋白<0.2 g;④疾病稳定(SD):不符合上述CR、VGPR、PR和PD者;⑤疾病进展(PD):各项指标升高为基线水平的25%以上者,或软组织浆细胞瘤增大或者出现新的溶骨病变。总体反应率(ORR)=VR+VGPR+PR,未缓解率(NRR)=SD+PD。
1.4.2 对所有患者进行随访,随访时间截止为2019年4月,可以采取资料查阅、电话、微信以及实地随访,为联系到本人者需通过其亲属掌握相关信息。评价2组患者的总生存期(OS)和无进展生存期(PFS),并且依据NCI常见不良反应事件评价标准(CTCAE)第4版评估治疗期间患者出现的毒副反应。
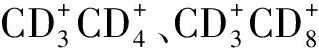
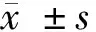
2 结果
2.1 2组患者短期疗效比较 观察组的ORR为84.6%(22/26)显著高于对照组的57.7%(15/26),差异有统计学意义(χ2=4.591,P=0.032)。见表1。
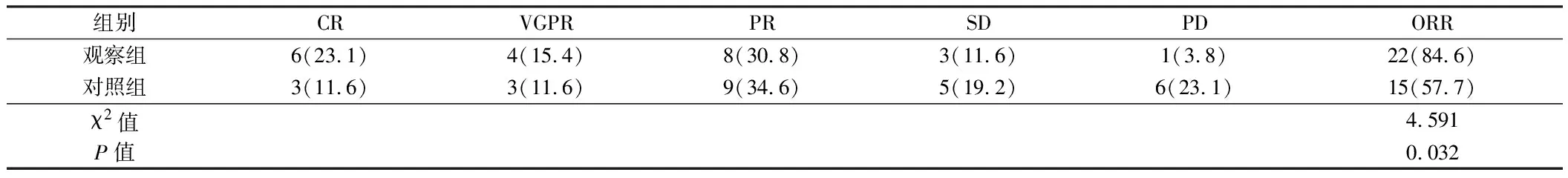
表1 2组患者短效疗效比较 n=26,例(%)
2.2 2组免疫抑制因子和淋巴细胞水平比较 治疗前,2组患者的各项免疫抑制因子和淋巴细胞指标差异无统计学意义(P>0.05);治疗后,2组患者的各项免疫抑制因子和淋巴细胞指标相比于治疗前均显著改善,且观察组的改善幅度显著优于对照组,差异有统计学意义(P<0.05)。见表2。
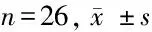
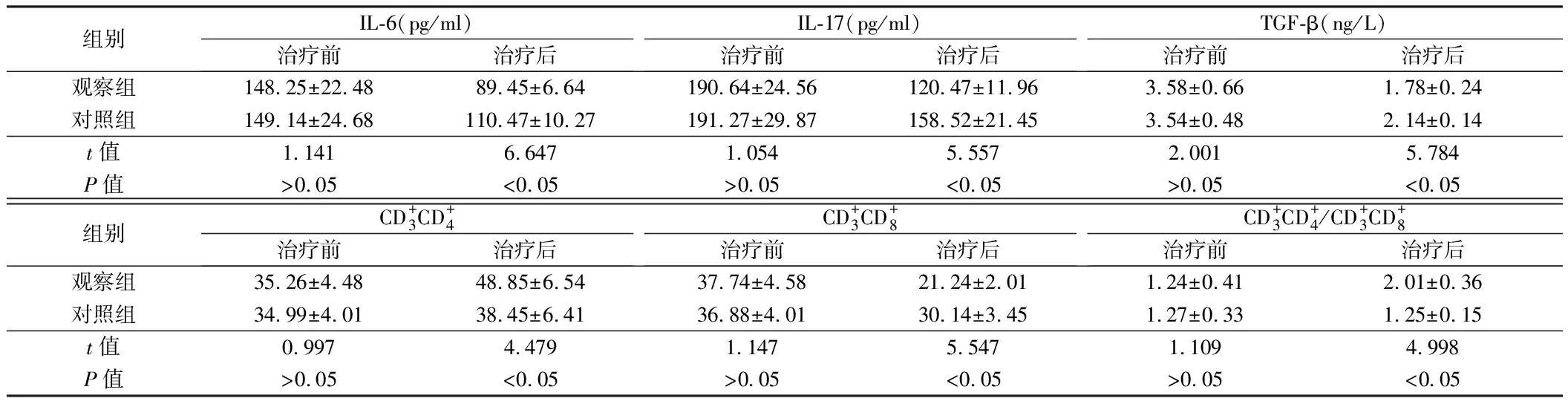
组别IL-6(pg/ml)治疗前治疗后IL-17(pg/ml)治疗前治疗后TGF-β(ng/L)治疗前治疗后观察组148.25±22.4889.45±6.64190.64±24.56120.47±11.963.58±0.661.78±0.24对照组149.14±24.68110.47±10.27191.27±29.87158.52±21.453.54±0.482.14±0.14t值1.1416.6471.0545.5572.0015.784P值>0.05<0.05>0.05<0.05>0.05<0.05组别CD+3CD+4治疗前治疗后CD+3CD+8治疗前治疗后CD+3CD+4/CD+3CD+8治疗前治疗后观察组35.26±4.4848.85±6.5437.74±4.5821.24±2.011.24±0.412.01±0.36对照组34.99±4.0138.45±6.4136.88±4.0130.14±3.451.27±0.331.25±0.15t值0.9974.4791.1475.5471.1094.998P值>0.05<0.05>0.05<0.05>0.05<0.05
2.3 2组不良反应比较 研究期间患者发生的不良反应有血液学毒性、外周神经毒性、消化道反应、部分感染感染、心脏毒性、水肿以及肝功能损伤等。大多数为2级以下的毒性反应,试验过程中给予对症治疗后均可缓解。观察组的各类型毒性反应发生率均显著低于对照组,差异有统计学意义(P<0.05)。见表3。
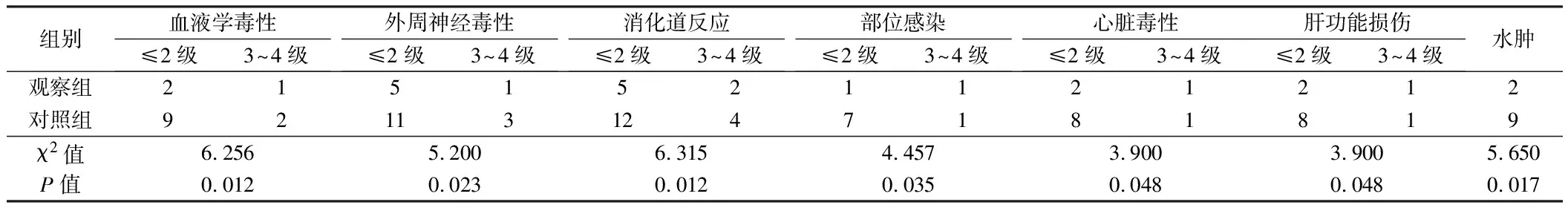
表3 2组不良反应比较 n=26,例
2.4 2组患者生存分析 观察组的中位OS为34个月(95%Cl:30.669,37.331),中位PFS为20个月(95%Cl:17.002,22.998);对照组的中位OS 为25个月(95%Cl:22.501,27.499),中位PFS为16个月(95%Cl:14.577,17.423)。观察组的OS和PFS显著高于对照组,差异有统计学意义(P=0.001,0.000)。见图1。
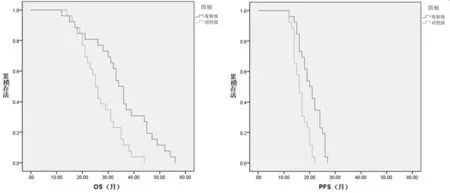
图1 2组生存函数分析(OS和PFS)
3 讨论
多发性骨髓瘤是一种很难实现完全被治愈的恶性血液系统肿瘤,其诱发因素很多,我国每年有2~5万人罹患多发性骨髓瘤,而且以老年人群为主。据统计,多发性骨髓瘤的发病率随着年龄的增长而不断地上升[9]。多发性骨髓瘤引起分泌单克隆免疫球蛋白,可导致相关靶器官受损,后续引发高钙血症、溶骨性破坏、感染以及肾脏贫血等临床病症[10]。如若治疗不及时就会导致更为严重的骨组织破坏。在医学上,多发性骨髓瘤治疗的核心仍然是自体干细胞移植,但大多数患者由于受到年龄的限制而无法接受该疗法,当前的医学技术水平尚无法满足该病的治疗需求,然而随着基础研究的不断深入和新型药物的相继问世,为多发性骨髓瘤的临床治疗提供了很多种方案,而且患者的治疗效果以及预后情况与治疗方案的选择密切相关[11]。近年来随着蛋白酶体抑制剂的新药开发研究,包括硼替佐米在内的治疗方案可以有效地改善多发性骨髓瘤患者的疾病缓解及总体生存情况。而且,相关指南也推荐硼替佐米联合化疗方案作为多发性骨髓瘤的有效治疗手段[12]。
硼替佐米作为新型蛋白酶体抑制剂的代表性药物,与环磷酰胺和地塞米松联合作为化疗方案可以发挥协同增效的作用,其主要通过诱导肿瘤周围细胞对环境反应的应激性,进而提高了化疗的敏感性。再者,硼替佐米可以特异性的降解蛋白质20S亚单位蛋白酶的活性,以减少骨髓瘤细胞内核因子的抑制因子的降解,从而抑制了骨髓瘤细胞内核因子的活性,发挥出抗肿瘤的功效。在上述过程中,通过调节细胞因子以阻断骨髓微环境中细胞的自分泌和旁分泌作用,抑制新血管的生成、DNA修复及破骨细胞的活性等[13]。在临床应用过程中,BCD化疗方案(硼替佐米+环磷酰胺+地塞米松)针对于初诊的多发性骨髓瘤患者具有良好的响应率[14],本研究采用BCD方案治疗多发性骨髓瘤患者的ORR可达84.6%,OS和PFS也优于传统治疗方案,并且在细胞因子和淋巴细胞改善方面也具有一定的优势,安全性良好,该研究结果也与报道[15]基本一致。
不良反应情况方面,含硼替佐米在内的BCD化疗方案的不良反应发生率显著优于传统方案,临床治疗过程中应对症处理。其中,出现血小板水平下降时需要及时补充血小板;针对于周围神经病变者需要进行营养神经保护和改善局部循环;有感染现象发生时可以选择不同的抗菌药物进行治疗,或者给予丙球蛋白以提高机体免疫水平,继而严重感染的发生[16]。
多发性骨髓瘤的预后与患者自身的年龄、骨髓浆细胞浸润程度以及疾病分期密切相关,本研究中2组患者的临床基线资料基本一致,因此,可以认为观察组的OS和PFS的延长、以及ORR的提升和不良反应的发生改善方面归于含硼替佐米在内的化疗方案的使用。
