超临界CO2萃取牡丹籽粕多酚工艺及其抗氧化性评价
2020-05-25顾仁勇陈晓娟
顾仁勇 陈晓娟
(吉首大学化学化工学院,吉首 416000)
牡丹籽为毛茛科芍药属灌木牡丹的种子,含油量高达30%,并且富含不饱和脂肪酸[1],是近年来大力发展的新木本油料资源。牡丹籽油于2011年被我国卫生部批准为新资源食品,进一步促进了牡丹籽油产业的快速发展。牡丹籽粕是牡丹籽制油后的主要副产物,含有多种营养成分及多糖、黄酮类化合物、单萜苷类、多酚等功能活性物质[2,3],因而具有重要的开发利用价值。
植物多酚类物质因具有良好的抗氧化、降血压、抗肿瘤、抗动脉粥样硬化、清除体内自由基等生理和药理活性[4-6],成为研究热点。多酚类物质提取主要有溶剂提取、金属离子沉淀、树脂分离法和超临界萃取等方法[7-10]。目前牡丹籽粕多酚的提取仅有溶剂提取的报道[11],单纯的溶剂浸提提取率较低,通常需要微波或超声波辅助以提高提取效率。超临界CO2萃取技术具有工艺简单、萃取高效、产品性质稳定等优点,在植物多酚的提取中得到了广泛应用,但用于牡丹籽粕多酚提取及其抗氧化性研究鲜有报道。另外,由于多酚类物质分子极性强,在CO2流体中的溶解度相对较低,添加乙醇等极性夹带剂能有效提高对酚类的溶解能力,从而提高萃取效果。
本研究采用超临界CO2萃取技术提取牡丹籽粕多酚,重点探讨了夹带剂、萃取温度和萃取压力对提取效果的影响,优化了工艺参数,并测定了其体外抗氧化能力,可为牡丹籽粕多酚综合利用提供参考。
1 材料与方法
1.1 原料与试剂
牡丹籽粕:湖南优镒农业开发有限公司。
福林-酚试剂(BR,1.0 mol/L);没食子酸标准品;DPPH;ABTS;其他试剂均为分析纯。
1.2 仪器与设备
UV-2450紫外-可见分光光度计;HA121-50-01超临界CO2萃取装置;F1-130药物粉碎机;YZF-6250L真空干燥箱。
1.3 方法
1.3.1 超临界CO2萃取牡丹籽粕多酚
牡丹籽粕真空干燥至含水量10%左右,粉碎,控制粉末粒度为80目[12]。称粉料200 g,装入萃取罐,按原料:夹带剂(g/mL)=1∶1.2的量加入乙醇夹带剂240 mL,浸润30 min[13],超临界萃取2.5 h,收集萃取产物。按公式计算多酚提取量:

1.3.2 多酚含量测定1.3.2.1 标准曲线绘制[14]
配制质量浓度为2.0、4.0、6.0、8.0、10.0、12.0 mg/100 mL的没食子酸标准品溶液,各取1.0 mL分别加入6支比色管中,依次加入0.5 mol/L的福林-酚试剂4.0 mL,再依次加入质量分数12.0%的Na2CO3溶液5.0 mL,静置2 h,于765 nm波长处测吸光度,绘制标准曲线,得吸光度(A)与没食子酸质量浓度(C)与的线性方程:A=1.004 3C-0.058(R2=0.997 5),用于样品中多酚含量测定。
1.3.2.2 产品多酚含量测定
取提取物样品1.0 mL,加蒸馏水稀释使其质量浓度处于标准曲线的有效浓度范围,吸取1.0 mL稀释液,加入比色管,如标准曲线测定方法处理,于765 nm波长处测吸光度,重复3次,带入回归方程计算多酚含量。
1.3.3 萃取条件优化实验
选取乙醇(夹带剂)体积分数(50%、60%、70%、80%、90%)、萃取温度(40、45、50、55、60 ℃)和萃取压力(20、25、30、35、40 MPa)3个因素的变量水平,进行单因素实验,以多酚提取率为响应值,初步优选萃取条件。在单因素实验结果的基础上,采用Box-Behnken响应面实验设计对乙醇(夹带剂)体积分数、萃取温度和萃取压力3个条件组合进行优选。实验因素水平见表1。

表1 因素水平表
1.3.4 抗氧化实验1.3.4.1 DPPH·清除能力
参考文献[15]方法略改动,配制不同质量浓度牡丹籽粕多酚溶液,各取2.0 mL,加入0.1 mmol/L的DPPH乙醇溶液2.0 mL,充分混合,室温下避光反应30 min,517 nm波长处测吸光度A1。按此法以等体积无水乙醇代替多酚溶液,测吸光度A2;以等体积无水乙醇代替DPPH溶液,测吸光度A3。以VC为参照,每组重复3次。计算DPPH·清除率。
1.3.4.2 ABTS+·清除能力
参考文献[16]方法略改动,将7 mmol/mL的ABTS原液与2.45 mmol/L过硫酸钾溶液等体积混合,常温避光反应12~16 h,使用前用无水乙醇稀释,使ABTS溶液在734nm处吸光值为(0.7±0.02)。取牡丹籽粕多酚提取液0.2 mL与2.4 mL ABTS溶液充分混匀,避光反应6 min,在734 nm处测吸光度A1,以无水乙醇代替多酚提取液测吸光度A。以VC为参照,每组重复3次。计算ABTS+·清除率。

1.3.5 数据处理
采用Minitab16进行数据的方差分析及显著性检验,采用Design-Expert 8.05进行Box-Behnken实验设计及数据处理。
2 结果与分析
2.1 单因素实验结果
2.1.1 乙醇(夹带剂)体积分数对多酚提取量的影响
萃取温度50 ℃、萃取压力30 MPa,乙醇体积分数分别为50%、60%、70%、80%、90%时牡丹籽粕多酚提取量见图1。

注:不同字母表示差异显著(P<0.05),相同字母表示差异不显著(P>0.05),余同。图1 乙醇体积分数对多酚提取量的影响
由图1可见,乙醇体积分数由50%逐步增加至80%时,多酚提取量由10.72 mg/g逐步提高至18.44 mg/g,提升效果显著(P<0.05),并达到最大值。酚类分子极性大,加入乙醇等极性夹带剂能提升CO2流体对酚类的溶解能力,利于萃取[17,18]。乙醇体积分数大于80%,提取量反而有所降低,这可能是体积分数过大的夹带剂也会使超临界流体密度降低,而影响酚类的提取。因此,乙醇体积分数最佳为80%。
2.1.2 萃取温度对多酚提取量的影响
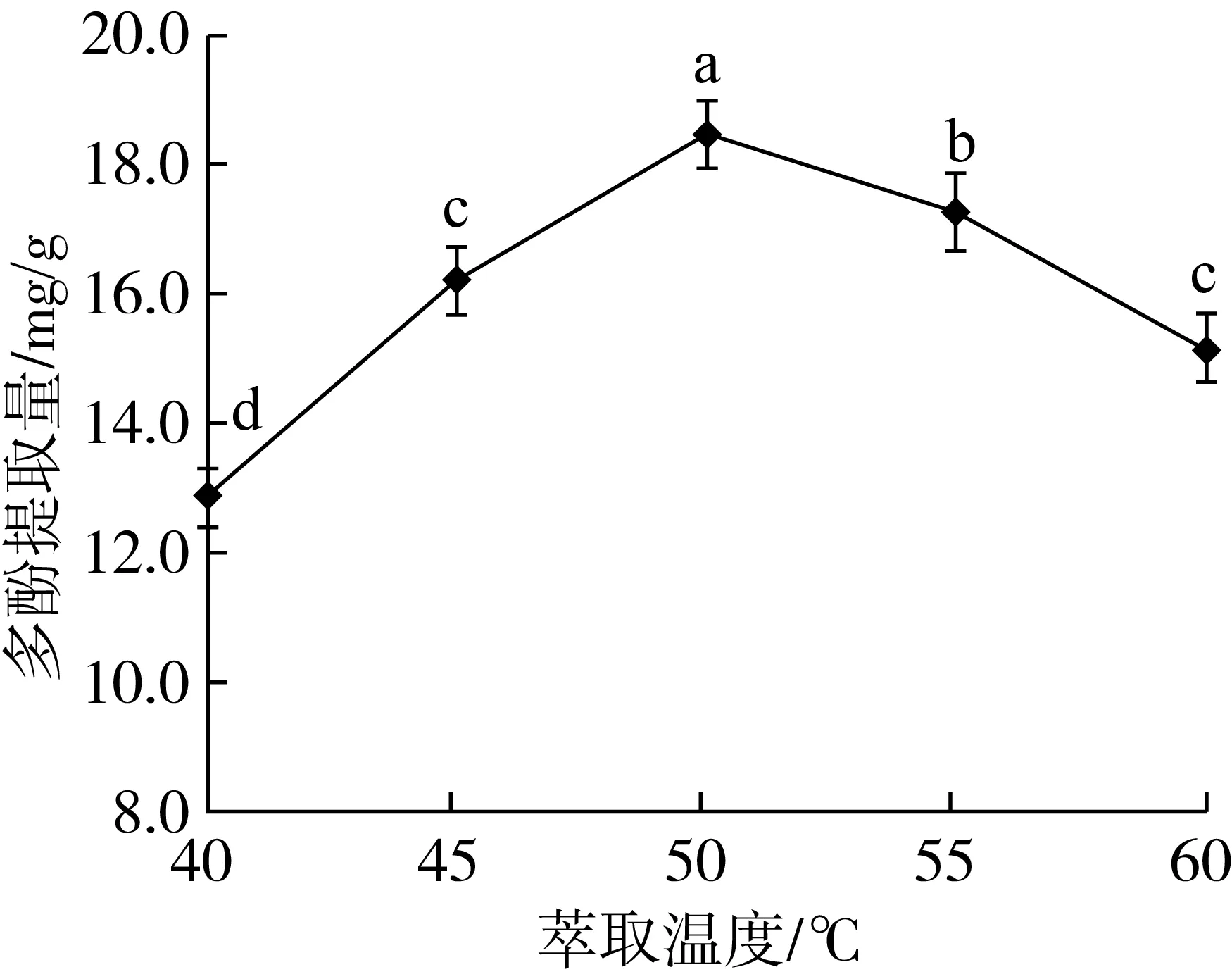
图2 萃取温度对多酚提取量的影响
乙醇体积分数80%、萃取压力30 MPa,萃取温度分别为40、45、50、55、60 ℃时牡丹籽粕多酚提取量见图2。萃取温度由40 ℃逐步增大至50 ℃时,多酚提取量由12.86 mg/g逐步提高至18.43 mg/g,提升效果显著(P<0.05),并达到最大值;温度继续由50 ℃增至60 ℃,提取量反而显著降低(P<0.05)。温度升高一方面可增大被萃取物质的扩散系数而提高提取量,同时也会降低CO2和夹带剂密度,使被萃取物质溶解度降低而降低萃取效果[17,18]。因此,选择萃取温度为50 ℃。
2.1.3 萃取压力对多酚提取量的影响
乙醇体积分数80%、萃取温度50 ℃,萃取压力分别为20、25、30、35、40 MPa时牡丹籽粕多酚提取量见图3。萃取压力由20 MPa逐步增大至30 MPa时,多酚提取量由13.23 mg/g逐步提高至18.47 mg/g,提升效果显著(P<0.05),并达到最大值;压力继续增大时,提取量反而显著降低(P<0.05)。萃取压力升高,CO2流体密度增大,增加多酚类物质的溶解及缩短分子间的传质距离,利于萃取;但压力过高,溶质的扩散系数减小,传质阻力增大,导致提取量降低[17,18]。因此,最优萃取压力为30 MPa。
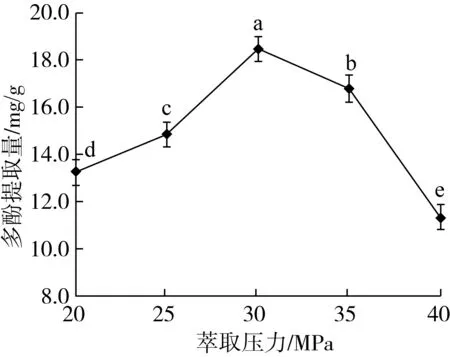
图3 萃取压力对多酚提取量的影响
2.2 响应面优化实验结果
2.2.1 实验方案及结果
依据单因素实验结果,采用Box-Behnken响应面法,以多酚提取量为响应值,优化乙醇(夹带剂)体积分数、萃取温度和萃取压力3个条件。实验结果见表2。

表2 响应面实验设计及结果
2.2.2 方差分析
对表2中的数据进行多元回归拟合,得牡丹籽粕多酚提取量(Y)与各因素回归方程:
Y=18.22+0.53A+0.88B+0.74C+0.16AB-0.46AC-0.71BC-0.62A2-0.93B2-0.42C2

表3 回归方程的方差分析

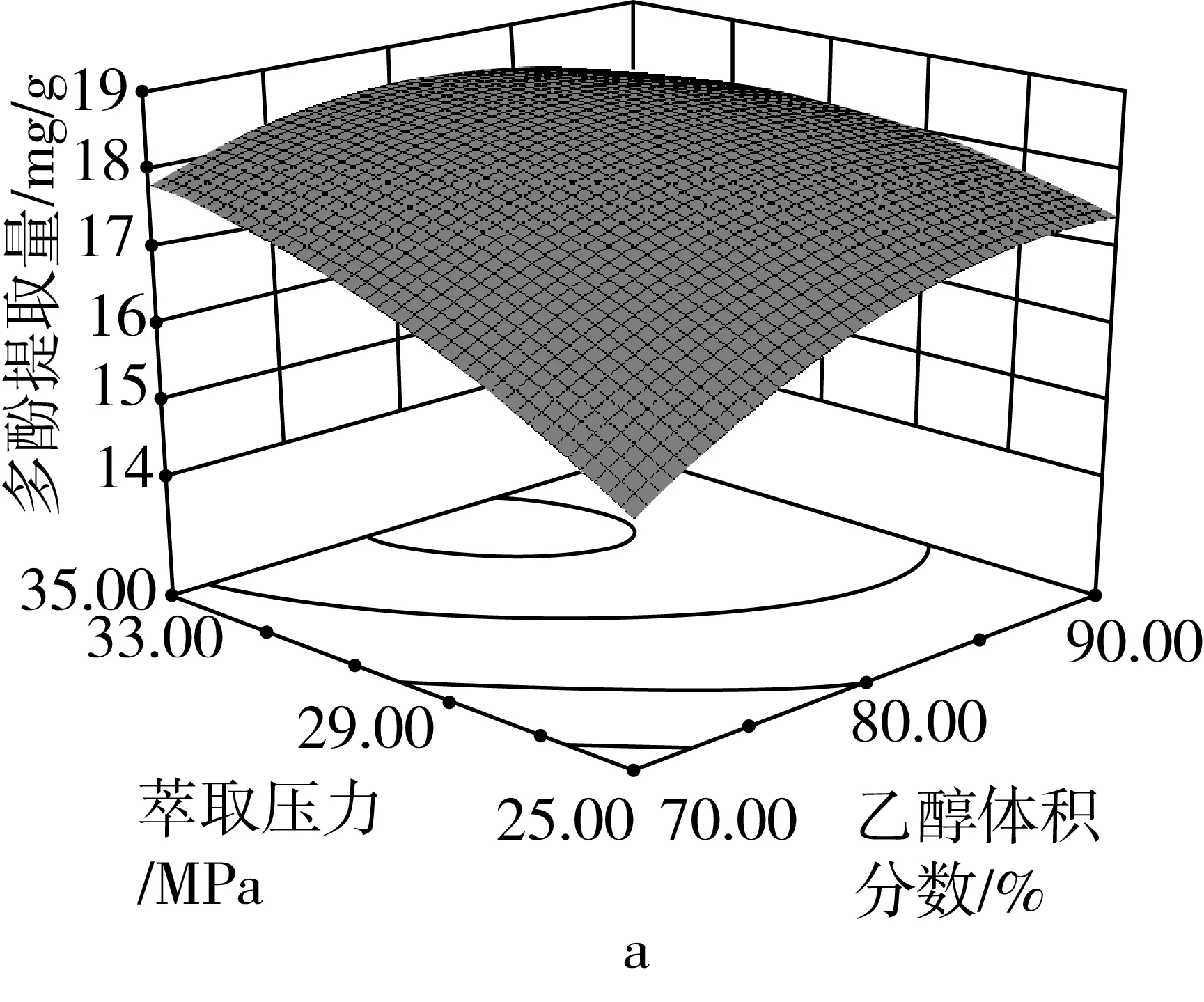
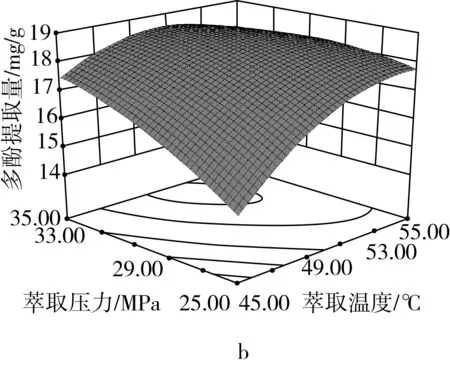

图4各因素交互作用的响应面
据方差分析结果可判断,因素A(乙醇体积分数)、B(萃取温度)、C(萃取压力)对提取量均有极显著影响(P<0.01);二次项A2、B2存在极显著影响(P<0.01),C2存在显著影响(P<0.05),表明各因素对提取量存在显著的曲线效应;因素交互项AC、BC对提取量影响极显著(P<0.01),AB影响不显著(P>0.05),表明因素AC、BC间存在极显著的交互效应,AB间无交互效应;由F值可判断,因素影响主次顺序为:萃取温度>萃取压力>乙醇(夹带剂)体积分数。
2.2.3 响应面分析
3个因素间交互作用响应面及等高线图见图4。响应面图中某因素图形变化坡度大,等高线密集,则表明该因素对响应值影响大;等高线接近椭圆表明两因素交互影响大,接近圆形表示交互效应小[19]。
由图4a可见,响应面图中沿萃取压力方向图形坡度更为陡峭,等高线变化更加密集,表明萃取压力的影响大于乙醇体积分数,对多酚提取量贡献更大;等高线接近椭圆,表明乙醇体积分数和萃取压力间交互效应明显。同理,图4b中萃取温度的影响大于萃取压力,对多酚提取量的贡献更大,萃取温度与萃取压力间交互效应明显;图4c中,萃取温度对提取量的影响和贡献大于乙醇体积分数,等高线近圆形,表示两因素交互效应不明显。
2.2.4 最优萃取条件的预测及验证
利用回归方程预测牡丹籽粕多酚最优萃取条件为:乙醇体积分数83.34%、萃取温度51.76 ℃、萃取压力31.97 MPa,预测多酚提取量为18.61 mg/g。为了便于实际操作,将提取条件调整为:乙醇体积分数83%、萃取温度52 ℃、萃取压力32 MPa,以此条件进行验证实验,重复3次,提取量平均值18.58 mg/g,与预测值接近,表明回归方程可靠,所得最优萃取条件可用于牡丹籽粕多酚的提取。
2.3 抗氧化实验结果
2.3.1 DPPH·清除实验结果
配制质量浓度30、60、90、120、150 μg/mL的牡丹籽粕多酚及VC溶液,测定其对DPPH·清除率,结果见图5。在质量浓度30~150 μg/mL范围内,牡丹籽粕多酚对DPPH·具有良好的清除能力,且随着质量浓度的增大,清除率由13.3%显著增强至56.1%(P<0.05)。质量浓度30~60 μg/mL间,同质量浓度下牡丹籽粕多酚与VC对DPPH·的清除率无显著差异(P>0.05);质量浓度大于90 μg/mL时,同质量浓度下牡丹籽粕多酚对DPPH·的清除率显著强于VC(P<0.05),且两者清除率的差异随质量浓度增大而增大。
分析表明牡丹籽粕多酚和VC质量浓度与DPPH·的清除率间均存在极显著的直线正相关(P<0.01,R2分别为0.982 6、0.986 2),表明两者抗氧化活性均存在明显的量效关系。利用回归方程计算抑制率为50%时牡丹籽粕多酚和VC的质量浓度IC50分别为128.22 μg/mL和147.72 μg/mL,也表明牡丹籽粕多酚对DPPH·的清除能力显著强于VC(P<0.05)。

图5 牡丹籽粕多酚对DPPH·的清除率
2.3.2 ABTS+·清除实验结果
配制质量浓度30、60、90、120、150 μg/mL的牡丹籽粕多酚及VC溶液,测定其对ABTS+·清除率,结果见图6。在质量浓度30~150 μg/mL范围内,牡丹籽粕多酚对ABTS+·表现出良好的清除能力,且随质量浓度的增大清除率由25.1%显著增强至64.2%(P<0.05)。同质量浓度下牡丹籽粕多酚对ABTS+·的清除率显著强于VC(P<0.05),且两者清除率的差值随质量浓度增大而增大。

图6 牡丹籽粕多酚对ABTS+·的清除率
分析表明牡丹籽粕多酚和VC质量浓度与ABTS+·清除率间均存在极显著的直线正相关(P<0.01,R2分别为0.996 0、0.993 6),表明两者抗氧化活性存在明显的量效关系。利用回归方程计算牡丹籽粕多酚和VC对ABTS+·的IC50分别为109.18 μg/mL和142.66 μg/mL,也表明牡丹籽粕多酚对对ABTS+·的清除能力显著强于VC(P<0.05)。
3 结论
超临界萃取牡丹籽粕多酚最优条件为:乙醇体积分数83%、萃取温度52 ℃、萃取压力32 MPa,此条件下提取量为18.58 mg/g。在超临界CO2萃取牡丹籽粕多酚工艺条件中,萃取温度与萃取压力、乙醇(夹带剂)体积分数与萃取压力之间存在协同效应,合理优化参数有利于提高牡丹籽粕多酚的提取量及产品的稳定性。牡丹籽粕多酚对DPPH·和ABTS+·的清除能力均显著强于VC。超临界CO2萃取技术适用于牡丹籽粕多酚的提取,牡丹籽粕多酚可作为天然抗氧化活性剂和自由基清除剂开发利用。
