高灵敏度HCV RNA检测在术前筛查中的应用
2020-05-24何宇婷陈雪芳陈培松黄浩余学高黄彬
何宇婷 陈雪芳 陈培松 黄浩 余学高 黄彬★
丙型病毒性肝炎(viral hepatitis type C,HC),简称丙型肝炎,由丙型肝炎病毒(hepatitis C virus,HCV)引起,是世界性重大卫生问题之一。据报道,丙型肝炎病毒在2015年全球的流行率达到1%,相当于全球有7 110 万丙肝患者[1]。HCV 感染后,基因组RNA 只在宿主细胞中复制翻译,并不会把病毒基因组整合到宿主染色体上,经过有效治疗,丙型肝炎可以被彻底治愈[2]。HCV 多呈隐匿性感染,少数表现为急性肝炎,易向慢性肝炎转变,75%~85%的急性丙肝可发展为慢性肝炎,甚至进一步发展为肝硬化和肝癌[3]。HCV 主要通过血液传播,同时医源性传播的风险也较高,特别是对于器官移植的病人及血透与腹膜透析的病人。为有效防止医源性HCV 感染,术前必须对HCV 感染进行筛查。目前临床上在术前筛查中主要通过免疫学方法对HCV 抗体进行检测,从而达到对丙型肝炎的初步筛查。该方法可反映患者HCV 感染的免疫状态,但易漏检隐匿性感染或感染初期机体未产生特异性抗体的窗口期感染者。HCV RNA 检测能直接反映体内HCV 的复制情况,对丙型肝炎患者做出正确诊断。本研究对术前筛查患者分别采用高灵敏度实时荧光定量聚合酶链式反应(Polymerase Chain Reaction,PCR)法检测HCV RNA 和化学发光微粒子免疫分析法(chemiluminescence microparticle immunoassay,CMIA)检测HCV 抗体,对检测结果进行比较,分析两种方法的优势和劣势,探讨高灵敏度HCV RNA 检测在术前筛查中的应用价值,为临床医生准确诊断丙型肝炎和区分现症和既往感染提供依据。
1 材料与方法
1.1 材料
收集2019年1月至10月间中山大学附属第一医院术前筛查患者血清标本1 005例。血清标本分成两份,一份用于HCV 抗体检测,另一份保存于-80℃备用,用于HCV RNA 检测,避免反复冻融。
1.2 主要试剂与仪器
Architect anti-HCV 试剂盒购自美国Abbott 公司;高灵敏度HCV RNA 检测试剂盒与核酸提取纯化试剂购自中山大学达安基因股份有限公司,高灵敏度HCV RNA 检测试剂盒灵敏度为20 IU/mL,线性范围50~108IU/mL;Architect-i2000SR 免疫分析仪购自美国Abbott 公司,ABI 7500 型荧光定量PCR 仪购自美国Life Technologies 公司,Smart 32 型半自动核酸提取仪购自中山大学达安基因股份有限公司。
1.3 方法
1.3.1 血清中HCV 抗体的检测
根据试剂盒说明书,采用CMIA 法,用Architect-i2000SR 对HCV 抗体进行检测,当HCV 抗体的S/CO 值大于或等于1 时,判断为HCV 抗体阳性。
1.3.2 高灵敏度HCV RNA 检测
按照核酸提取纯化试剂说明书,应用Smart 32半自动核酸提取仪对收集到的血清进行核酸提取。HCV RNA 的扩增程序为:50℃15 min 1 个循环;95℃15 min,1 个循环;94℃15 s,55℃45 s,45个循环。高灵敏度HCV RNA 试剂盒的最低检测限为20 IU/mL,羧基荧光素(carboxy-fluorescein,FAM)荧光检测通道无明显对数增长,或定量结果低于高灵敏度HCV RNA 试剂盒检测下限,判断为HCV RNA 阴性;若FAM 检测通道和VIC 检测通道均有对数增长期,且定量结果大于20 IU/mL,判断为HCV RNA 阳性。
1.3.3 统计学分析
采用SPSS 22.0 软件进行分析;应用Spearman进行相关性分析,采用受试者工作特征曲线(receiver operating characteristic curve,ROC)对指标的诊断效能进行评价。P<0.05 为差异有统计学意义。
2 结果
2.1 高灵敏度HCV RNA 检测与CMIA 法抗体检测结果的比较
在收集的1 005例术前筛查样本中,HCV 抗体阳性22.7%(228/1005)。228例HCV 抗体阳性的样本中HCV RNA 检测阳性为36.4%(83/228),HCV RNA 检测阴性为63.6%(145/228))。HCV 抗体阴性777例,未在抗体阴性的样本中检测到HCV RNA 阳性的样本。见表1。以高灵敏度HCV RNA 检测作为HCV 病毒血症金标准,CMIA法检测HCV 抗体反映HCV 病毒血症的灵敏度与特异度分别为100%与78.3%,阳性预测值和阴性预测值分别是36.4%和100%,符合率为85.6%。
2.2 HCV 抗体S/CO 值与高灵敏度HCV RNA 检测结果的比较及相关性分析
将HCV 抗体阳性样本按照S/CO 值进行分组,见表1。随着S/CO 值的升高,阳性率有所升高。同时做S/CO 值与HCV RNA 定量值的散点图,进行相关性分析,见图1。线性拟合方程为Y=0.06 617X+4.259。Spearman相关系数r2=0.002,P=0.69,提示HCV 抗体S/CO 值的高低与HCV RNA定量值之间并无相关性。
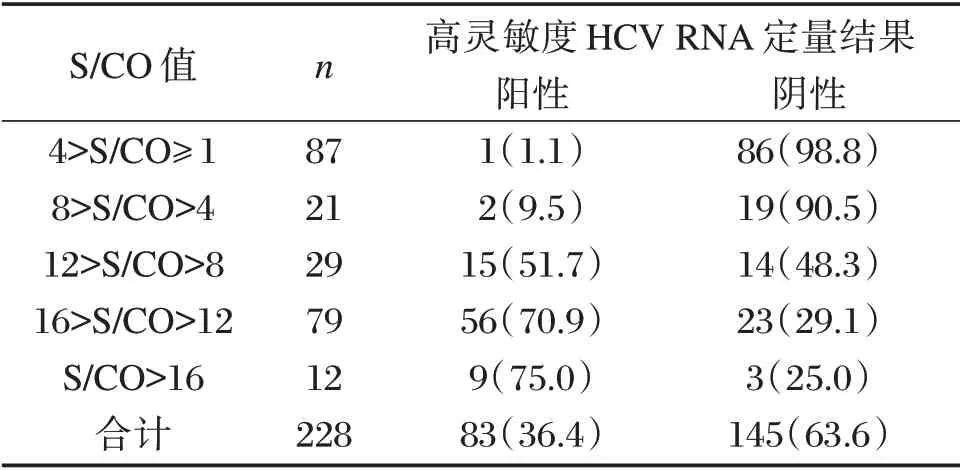
表1 HCV 抗体S/CO 值与高灵敏度HCV RNA 检测结果的分布[n(%)]Table1 Distribution of HCV antibody S/CO value and high-sensitivity HCV RNA detection results[n(%)]
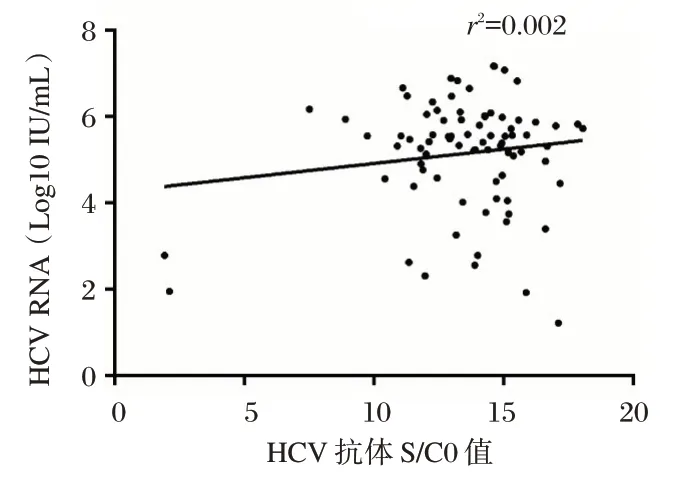
图1 HCV 抗体S/CO 值与高灵敏度HCV RNA 定量检测结果的散点图Figure1 Scatter plot of HCV antibody S/CO value against high-sensitivity HCV RNA quantitative detection results
2.3 HCV 抗体S/CO 值对预测丙型肝炎病毒血症的效能评价
HCV 抗体S/CO 值对丙型肝炎诊断的ROC 曲线下面积(area under the curve,AUC)为0.872 4,由ROC 曲线可算出,以S/CO 值≥10.7 作为预测HCV病毒血症的截断值,即cut-off 值时,最大的约登指数Youden's index 0.705 2,此时的灵敏度与特异度分别为92.59%和77.93%。以S/CO 值≥1 作为初筛HCV 病毒血症的临界值,228例HCV 抗体阳性样本中,HCV RNA 阳性率只有36.4%(83/228)。见图2。

图2 HCV 抗体S/CO 值对预测丙型肝炎病毒血症的ROC 曲线Figure2 ROC curve of HCV antibody S/CO value for predicting hepatitis C viremia
3 讨论
临床上,对于丙型肝炎感染者进行早期、及时、准确的诊断是临床治疗的关键。目前,临床上检测HCV 感染的方法主要有血清学检测技术和分子诊断检测技术。血清学检测即利用病毒抗原或针对病毒抗原的特异性抗体检测患者体内HCV血清标志物,包括HCV 抗体和HCV 抗原[4]。通常情况下,丙型肝炎抗体在患者感染HCV 2 个月后才能被检测出来。因此,丙型肝炎抗体的检测不能早期诊断HCV 感染[5]。HCV 抗体检测易漏检感染窗口期、病毒隐匿性感染或者血清中病毒拷贝数极低的患者,其检测具有一定的局限性。近年来,高灵敏度荧光定量PCR 通过设计针对病毒保守序列的特异性引物对病毒及其变异株进行检测,直接检测病毒核酸,是病毒感染的确诊方法,且PCR 自动化程度随着科技发展越来越高,操作趋于简单化,在临床上应用广泛。
Baleriola C 等[6]通过定量检测储存在-20℃和-70℃的HCV RNA 血浆样本发现,-20℃储存1.2年以及-70℃储存9年才会引起HCV RNA具有统计学差异的变化。本研究将血清标本置于-80℃储存,1年之内检测HCV RNA 并不会影响HCV RNA 定量结果的准确性。在228例HCV 抗体阳性标本中,阳性率为36.4%。这可能是由于某些HCV 慢性感染者,HCV 抗体可持续阳性而血清中HCV RNA 因抗病毒治疗而处于极低复制水平或病毒已被清除,高灵敏度HCV RNA 定量检测不到。之后对不同的S/CO 值范围对应的HCV RNA检测结果进行分析,随着S/CO 值的升高,阳性率似乎有所升高,通过Spearman 相关性分析发现,HCV 抗体S/CO 值与HCV RNA 定量值之间无相关性,S/CO 值的高低不能反映HCV 病毒体内的复制状况。随后ROC 曲线分析表明,当S/CO 的cutoff 值为10.7 时可获得良好的预测价值,临床上以S/CO 值≥1 作为初筛丙型肝炎病毒血症的cut-off值,在判断为HCV 抗体阳性的样本中HCV RNA阳性检出率低,不能对HCV 病毒血症进行较好的预测。Pan J,Kao HH 与Ranjbar Kermani,F 等[7-9]多数研究者通过检测HCV 抗体阳性的样本均发现,以S/CO 值≥1 作为丙型肝炎病毒血症的cutoff 值,存在一定比例的HCV 抗体阳性而HCV RNA 阴性的样本。基于上述优势,HCV 抗体检测可用于HCV 感染者的筛查,而HCV RNA 定量检测适用于HCV 现症感染的确认、HCV 病毒载量分析以及对治疗结束后的疗效评估[10]。高灵敏HCV RNA 定量检测(最低检测限小于15 IU/mL)已被美国疾病控制与预防中心、欧洲肝病学会、我国肝脏病学会和传染病学会推荐对HCV 感染者进行检测[11]。
Ha J 等[12]运用HCV RNA 检测对32 127例Architect anti-HCV 试剂盒检测为HCV 抗体阴性的样本进行检测,发现8例(0.02%,8/32 127)HCV RNA 阳性。陈冬等[13]在148 590 份ELISA 法检测为HCV 抗体阴性的标本中检测出HCV RNA 阳性298例,阳性率为0.2%。叶贤林等[14]在307 440例ELISA 法检测为HCV 抗体阴性的标本中检测出1例HCV RNA 样本,检测率为0.000 325%。这可能是由于患者处于感染窗口期或者患者处于免疫抑制状态,无法产生或产生极低水平的特异性抗体。此外,也可能是HCV 基因变异或亚型感染及隐匿性肝炎[15]。本研究中未发现HCV 抗体阴性而HCV RNA阳性标本,这可能与地区流行率有关,后续需扩大样本量以获得更准确的结果。
综上所述,高灵敏度HCV RNA 的定量检测用于术前筛查丙肝感染者,窗口期短,能准确、及时地反映患者HCV 感染状态,HCV 在患者体内的复制情况,与传统术前筛查方法相比,能区分现症感染与既往感染,可有效防止医源性传播。
