自燃型离子液体点火燃烧机制研究进展
2020-05-13孙常庚唐韶坤
孙常庚,唐韶坤,2
(1.天津大学化工学院绿色合成与转化教育部重点实验室,天津 300072;2.天津化学化工协同创新中心,天津 300072)
1 引言
推进剂是能够通过燃烧释放能量并产生大量气体的含能材料,主要用于为火箭或导弹提供动力。双组元推进剂由液体氧化剂和液体燃料所组成[1],它们在燃烧前分开贮备,燃烧时将两种液体分别注入火箭发动机的燃烧室中,接触并发生化学反应,释放足够的热量,使燃料自发点燃,不需要额外的点火源[2-3]。自燃型燃料用作推进剂最初的发展高潮是二战时期,传统的推进剂燃料主要以肼及其衍生物为主,这类物质具有剧毒、易燃易爆、污染环境等缺点,在生产、运输、加注、发射等过程中容易泄漏,引起人员中毒以及爆炸着火等事故[4]。近年来,随着人们对环境与健康问题的日益重视,寻求性能优异且具有环境友好和良好安全性的推进剂燃料成为当前各国的研究热点。
含能材料与离子液体的交叉孕育了一种新型含能材料的概念,即含能离子液体(Energetic ionic liquids,EILs)[5]。它们具有离子液体的大多数特性,而且拥有特定的含能基团,具有较高的能量密度,同时具有较高的稳定性。2008 年,Schneider 等[6]合成了几种阳离子为咪唑、阴离子为二氰胺([DCA])的含能离子液体,发现它们与白色发烟硝酸(White fume nitric acid,WFNA)接触后可以自发点火,这一发现开辟了含能离子液体作为自燃型推进剂燃料的新应用。在随后不断的研究中,这种与氧化剂接触能自燃的含能离子液体逐渐被归为新的一类,称为自燃型离子液体(Hypergolic ionic liquids,HILs)。 HILs 毒 性 较 低 且 不 易 挥发,具有较宽的液相范围,操作和运输的成本也较低,并且它们的性质和性能可以通过改变阴阳离子的组成和基团结构来进行调控,具有极大的潜力取代肼及其衍生物,成为新一代双组元推进剂燃料[7]。
燃料的自燃性是指其与氧化剂接触后能够自发点火的特性,自燃性的强弱可以用点火延迟时间的长短来衡量,点火延迟时间即燃料与氧化剂自接触直至出现火焰的时间间隔。2008 年至今,超过200 种含有新型阴或阳离子的HILs 被合成和测试[8],其在点火延迟、热稳定性、比冲等各方面的性质已经能够达到应用水平,例如 Zhang 等[9]合成的双硼烷基次磷酸([PB])类离子液体与WFNA 的点火延迟时间短至1 ms,优于偏二甲肼在实际应用中的表现。然而,大多数研究都侧重于HILs 的合成,关于其点火燃烧机制的研究甚少,导致了对HILs 自燃性和燃烧过程的理解不够清晰,严重阻滞了HILs 投入实际应用的进程。近几年,关于HILs 点火燃烧机制方面的研究逐渐涌现。为此,本研究综述了迄今为止HILs 点火燃烧机制方面的重要研究进展,分三个方面进行阐述:自燃反应路线与机理、点火和燃烧过程以及自燃性理论预测。总结了HILs 点火燃烧机制的研究现状和主要问题,并提出其未来可能的研究方向。
2 离子液体的自燃反应路线与机理
2.1 二氰胺类自燃型离子液体与发烟硝酸的自燃反应
探索导致点火的自燃反应是了解HILs 点火燃烧机制的第一步。自燃反应路线的研究难点在于反应过程发生在极短的时间内,其中涉及到复杂的瞬态物质和中间产物。[DCA]类离子液体是第一种被证明与WFNA 接触后能够展现自燃性的离子液体,所以大量的机理研究工作都是以此类离子液体为对象而展开的,研究的重点是关于中间产物的检测和分析。
Chambreau 等[10]首次利用快速扫描傅里叶变换红外光谱(FTIR)研究了二氰胺类离子液体与WFNA反应的产物,在火焰出现之前观测到了CO2、N2O 和HNCO 等物质,测试验证这些物质产生于中间体双硝基缩二脲(DNB)和硝酰胺的复杂反应。根据理论计算,他们提出下述反应路线:第一步初始反应是质子的传递放热,接着是硝酸根的亲核攻击吸热,然后NO2迁移到末端氮放热,质子传递在二氰胺阴离子的另一端同时发生从而产生了中间体DNB,DNB 热降解产物为 CO2、N2O 和 HNCO。此后,Chambreau 等[11]通过溶剂计算模型对反应路线进行了详细分析,认为NO2迁移到末端氮这一步释放的能量是体系温度提升的控制步骤。该结果也得到了其他研究者的验证,Chowdhury 等[12]采用改进的密闭快速热解装置,在等温条件下对预燃凝聚相进行了分析,发现点火过程由中和放热反应引发,接着生成氰基硝基脲和DNB,然后分解形成分子量较小的气体。Nichols 等[13]利用电喷雾离子源产生二氰胺阴离子,计算发现末端氮质子化的能量低于中心氮,认为DNB 是二氰胺类离子液体与硝酸反应路线中的关键中间体。Catoire 等[14]建立了化学反应动力学模型,预测气相中反应途径首先是异氰酸和硝酸之间的放热反应,随后是HONO2热分解产生NO2和OH 自由基作为点火的主要链载体。气相中并没有检测到DNB,其解释为DNB 只存在液相中,并在100 ℃左右发生分解,在点火前气相中的CO2、N2O 和 HNCO 都来自于 DNB 的分解。
另外一些研究并不完全认同这一机理,认为反应中间体 DNB 并没有形成。Litzinger 等[15]利用微探针取样和质谱分析对气相反应产物进行了研究,但是并没有检测出中间体DNB 的存在。他们认为使反应产物在双缩脲测试中呈阳性的不是DNB 而是氰酸二聚形成的二氰酸。Weismiller 等[16]利用 ReaxFF 反应力场通过分子动力学模拟研究了二氰胺阴离子自燃型燃料的反应动力学,当二氰胺阴离子与HNO3混合时,在NVE模拟(N:体系中的粒子数,V:体积,E:总能量)中发生了自燃反应,但是并没有发现中间体DNB 的形成。
在[DCA]阴离子与硝酸的反应过程中,还存在着聚合或环合副反应,产生以三聚氰胺为主的固体残留物,例如 Chingin 等[17]通过电喷雾质谱法发现[DCA]和HNO3之间的反应产生了一种由三嗪类化合物组成的沉淀,主要包括三聚氰胺及其低聚物。粗略测量表明,约25%的二氰胺离子液体在着火过程中转变为这种沉淀,因而会限制燃料的能量释放效率。Brotton等[18-22]通过超声提升器设备研究了多种离子液体悬浮液滴与NO2之间的反应,发现反应过程中NO2的氮原子能够与二氰胺中一个末端氮原子结合并产生O2N—NCNCN 阴离子。该研究也指出,在二氰胺类离子液体的降解过程中,会产生一种棕色的泡沫状物质和浓密的烟雾,被证明是两个或更多的三聚氰胺分子连接形成的,这些反应残留物对于自燃型燃料在火箭发动机中的使用是不利的。
2.2 其他自燃型离子液体与氧化剂的自燃反应
除了上述讨论的二氰胺类离子液体与WFNA 的自燃反应外,关于其他类型离子液体和氧化剂的反应路线的研究较少,这是该领域发展不足的地方。就氧化剂而言,与WFNA 相比,其他类型氧化剂的氧化性较弱,所展现出的点火延迟时间较长。其中,H2O2是一种格外受到重视的氧化剂,其毒性腐蚀性较低、产物清洁,与HILs 能够组合成真正的绿色推进剂。Schneider 等[23]报道了一种以三己基十四烷基磷盐为阳离子的离子液体,其与双氧水可以自燃点火且点火延迟时间低于30 ms,但文中没有涉及反应机理的解释。Wang 等[24]合成了碘代铜酸类离子液体,它们熔点较高,常温下呈固态,自身难以作为液体燃料。研究中将其作为一种促进剂加入到传统的HILs 中,通过碘快速分解H2O2的能力,缩短了HILs 与H2O2的点火延迟时间。这种通过向离子液体中引入第三物质来改变反应路线的方法在[DCA]与WFNA 的自燃反应中也有研究,例如 Vogelhuber 等[25]和 Thomas 等[26]的研究将二氰胺钠作为添加物加入到二氰胺类离子液体中,使反应的能垒显著降低,缩短了点火延迟时间。Jiao等[27]提出了一种新的离子液体-离子液体组合推进剂思路,他们合成了一种具有强氧化性能的离子液体可以作为双推进系统的氧化剂,并以咪唑硼簇离子液体作为燃料进行了点火测试,展现出了可以自燃的特性,虽然最短点火延迟时间长达98 ms,但是这是第一次使用了离子液体作氧化剂的实例,其未来的发展潜力巨大,遗憾的是文中并未提及反应路线和机理方面的解释。
综上所述,就二氰胺阴离子与硝酸的反应而言,质子传递是第一步初始反应,NO2迁移是控制放热的关键步骤,中间体是DNB 还是二氰酸存在着争议,反应过程中产生 CO2、N2O 和HNCO 等物质,且伴随着产生三聚氰胺的副反应。中间体检测困难,只通过双缩脲测试无法确定具体结构,需要更加精确的表征手段。从应用角度讲,副反应的产生是较为严重的问题,严重限制燃烧效率和发动机效率。关于其他类型阴离子与氧化剂的反应机理还需要进一步的研究探索。此外,H2O2作为绿色氧化剂应受到更多的关注,由于H2O2的氧化性比WFNA 弱很多,如何提高离子液体与H2O2的反应性将是研究的重点。
3 自燃型离子液体的点火和燃烧过程
3.1 点火过程的不同阶段
目前对自燃型离子液体点火过程的主要研究手段是进行滴落测试,然后采用高速摄像机测定点火延迟时间。不同的离子液体点火过程不尽相同。点火是燃烧过程的开端,大部分文献只对点火过程进行了详细的分析,但对于后续的燃烧过程的研究则相对较少。
Chowdhury 等[12]采用常规滴落实验装置观测离子液体1-乙基-3-甲基咪唑二氰胺([EMIM][DCA])与WFNA 的点火过程,高速视频显示在点火核形成之前,由于剧烈的凝聚相反应,凝聚相的小液滴被排出到点火区域,反应的剧烈性使液相的温度超过了沸点,形成众多的小气泡。在反应区上方的气相中,经过一定时间的气体和液滴的积累,在液滴撞击后25 ms 形成点火核。该研究的温度检测表明在混合时并没有明显的温度变化。Hooper[28]等利用分子动力学模拟研究也发现在混合区不会因混合热而引起明显的温度升高,因为离子液体和氧化剂的非混合区域可以迅速吸收混合区域产生的热量。
Li等[29]探索了两种自燃型离子液体[EMIM][DCA]和 1-丁基-3-甲基咪唑二氰胺([BMIM][DCA])与三种氧化剂WFNA、红色发烟硝酸(Red fuming nitric acid,RFNA)、N2O4的点火燃烧现象,结果表明离子液体的点火过程与单甲基肼非常相似。首先发生液相反应,形成蒸气空腔,随后,气液相反应也会在气相腔中发生。当气体的量在空腔内显著增加时,就会引起微爆炸,微爆炸后产生的微米级液滴与气相发生反应,产生足够快的热释放速率并自燃着火。Weng 等[30]测试了 8 种基于[BH3(CN)BH2(CN)]阴离子的离子液体与发烟硝酸的点火。其研究认为点火过程存在完全不同的三个阶段:在接触后的第一阶段,观察到从混合层中快速而有力地喷射出钉形液体,其延迟时间与侧链的烷基基团相关;在第二阶段,喷射到氧化剂池中的钉形液体显著增加了液面下的反应表面积。局部温度逐渐升高,气相中间产物和氧化剂/燃料蒸气在液面下由于连续的液相反应而积聚。当局部压力克服表面张力时,观察到二次液滴的喷射,同时释放蒸汽和烟雾;在第三阶段,当局部温度和蒸汽浓度充分增加时,进一步的气相反应导致着火,从最初的混合层不断发出精细而稳定的明亮绿色火焰。
通过这些研究,一个典型的点火过程可以总结为通四个阶段:接触和扩散,反应和放热,温度提升,点火火焰。首先,整个点火过程是自燃料与氧化剂的接触开始。接下来,离子液体燃料在氧化剂中边扩散边反应,扩散过程就会受到黏度的影响,高黏度的离子液体扩散性差,可能只有液滴表面部分与氧化剂接触反应。随着阳离子或阴离子不断的与氧化剂发生反应并放热,反应放热越多,系统温度提升则越快,直至液体开始沸腾,大量的气体产物从液相中释放出来,激烈时产生类似爆炸的现象。当温度达到着火点时,燃烧的火焰将会出现。
3.2 燃烧过程及特征现象
关于燃烧现象的分析主要包括火焰的特征如火焰颜色、形状和强度,以及火焰温度和燃烧的持续时间等。火焰的颜色主要和燃烧物质所含元素有关,例如含硼的HILs 通常展现出淡绿色火焰。而燃烧的强度和持续时间,通常与燃料的含能量和比冲相关。大多研究只关注了点火过程,对燃烧的分析寥寥无几。Wang 等[31]将富氧硝基引入阳离子中,增强阳离子的氧化还原活性,从而改善了燃烧性能。在相同的试验条件下,硝基化的HILs 展现出更加激烈明亮的白色火焰,持续时间也更长,这表明它们能够更有效地剧烈燃烧。火焰大小和燃烧时间的明显改善归因于阳离子的高氧平衡特性。
从实际应用的角度来说,燃烧火焰的特征及燃烧持续时间是非常重要的评价因素,未来的研究应该对离子液体的燃烧过程给以更多的关注。
3.3 影响点火和燃烧过程的因素
从本质上说,HILs 的结构和组成是影响它们点火燃烧过程的根本因素。Khomik 等[32]研究了不同阳离子N-烷基取代基R 对着火特性的影响,其结构如Scheme 1 所示。高速视频记录的分析表明,根据火焰区域的初始位置,所研究的离子液体可分为两类:当R由1 到3 个碳原子时,观察到的点火是气泡内和液体表面上方的辉光;当R 中的碳原子数为4-6 时,气泡内没有观察到辉光。特别地,在庚基取代基的情况下,大约1 min 之内未观察到火焰。
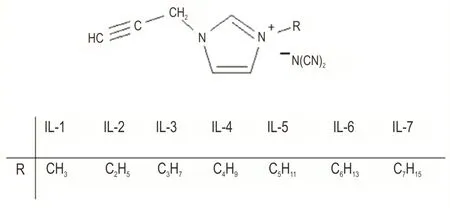
Scheme 1 Structural formula of ILs and n-alkyl substituents R
黏度对点火过程有明显的影响,黏度高的HILs 其扩散速率较慢,在滴入氧化剂后,甚至到点火时,离子液体与氧化剂间仍然存在明显的界面,导致了只有界面处发生反应,最终表现出较长的点火延迟时间。本课题组向多种不同的高黏度HILs 中加入少量乙醇,大幅度降低了其黏度。分子动力学模拟表明乙醇的加入破坏了离子之间的作用体系,增强了离子的扩散性,从而加速了点火过程。如图1 所示,在乙醇的摩尔分数小于0.3 时,1-腈丙基-3-甲基咪唑二氰胺([CPMIM][DCA])展现了更短的点火延迟时间。然而,乙醇的添加比例较大会导致点火失败,主要是由于离子液体的量较少而乙醇的热值低导致反应的总体放热量不足[33]。
点火测试的方法与环境的不同也会造成点火燃烧过程的差异,例如氧化剂和燃料的用量、燃料或氧化剂的滴落高度、环境的温度和压力等[34]。在同一系列的研究中,往往会对这些因素进行控制,减少对点火测试结果的影响,至于这些因素到底如何影响点火燃烧过程,并没有深入的研究。

图1 添加不同量乙醇的离子液体[CPMIM][DCA]的点火测试,乙醇摩尔分数(a)-0,(b)-0.05,(c)-0.5[33]Fig.1 Ignition test of HIL[CPMIM][DCA]with different amount of ethanol,mole fraction(a)-0,(b)-0.05,(c)-0.5[33]
综上所述,虽然很多文章都涉及到点火测试,但是对点火和燃烧过程的具体现象关注较少。目前的研究主要是基于滴落点火测试和高速摄像技术,根据大部分研究观察到的现象,可以将点火过程分为接触和扩散、反应和放热、温度提升、点火火焰四个阶段。然而,并不是所有的点火测试都会清晰地观测到中间两个阶段的现象,特别是对于那些反应性特别强以至于点火延迟时间特别短的离子液体,在接触氧化剂后,温度急速飞升,液相爆沸并随即就出现火焰。而对于反应性较弱的离子液体,中间两阶段的过程就会变得漫长一些,可以清晰观测到大量气体产物从液相中挥发出来,在较长时间后出现火焰甚至有时候点火失败。对于燃烧过程的分析,目前还很缺乏理论支持和先进的测试分析技术,离子液体的燃烧不同于普通的燃料,需要更多的深入研究。
4 自燃性的预测
如果能够在实验合成之前对离子液体的自燃性进行简单的理论预测或评估,将会减少大量的错误尝试并指导设计与合成具有更强自燃性的离子液体。目前主要存在两种思路,一种是收集数据建立数学模型进行预测;另一种是基于点火反应机理,从结构和反应能量出发,提出相对应的具体判据和评价。
4.1 点火延迟时间的数学预测
预测性质普遍流行的做法是建立可信度较高的数学模型,首先收集和统计大量的已有数据,然后设计和建立数学模型将已有的数据进行关联,并采用所获得的数学模型预测未知的数据。Newsome 等[35]利用线性定量结构性质关系(QSPR)和人工神经网络(ANN)方法分析了41 种离子液体,报道了点火延迟时间与一组量子化学计算描述符之间的关系,取得了良好的关联准确性。Alamdari 等[36]建立了一种预测 31 种自燃型咪唑离子液体衍生物点火延迟时间的QSPR 模型。总数1447 个分子描述符被选择和计算,显示出良好的预测能力。但是这种方法的局限性在于当前点火测试方法并没有统一的标准,点火延迟时间的数据不确定性较高,从而降低了这种数学模型方法的预测能力。
4.2 基于结构性质关系的理论预测
Sengupta 等[37]用前线轨道理论计算了大多数阴离子与硝酸的能级差,第一次从离子液体的结构出发去解释和预测离子液体的自燃性,他们发现具有自燃性的离子液体与氧化剂的轨道能级差往往较低。其研究建议避免在结构中设计C—C 键,建议改变结构以期获得较小的能级差和较大的生成热。阳离子的重要性也是不容忽视的,Carlin 等[38]计算了阳离子的脱质子能和净质子传递能(NPT)。他们认为离子液体要发生剧烈的反应,其NPT 能量和离子性必须在一定的范围内,从而能以足够快的速度释放足够多的能量,促进自燃的发生。本课题组研究了多种咪唑二氰胺类离子液体的构效关系[39],并计算了阳离子的NPT 能量,发现点火延迟时间与离子液体的结构展现出较强的关联性。当咪唑阳离子侧链取代基为饱和直链时,其链越长则黏度越大,点火延迟时间也越长。当阳离子取代基为不饱和链时,其生成热提高,热稳定性变差,在黏度相差不大的情况下,具有不饱和链的离子液体点火延迟时间更短。整体上看,NPT 能量较大且黏度较低的离子液体往往具有较短的点火延迟时间。
本课题组[40]计算了目前已知的多种自燃阴离子以及一些普通阴离子的轨道能级差ΔE,如图2 所示。可以看出,大多数的自燃阴离子的轨道能级差都小于[NO3],[NO3]从理论上不会与 HNO3反应,所以可以将[NO3]的轨道能级差作为一种筛选的标准。阴离子[PB]包括 6 个 B—H 基团和 2 个 P—H 基团,这样的基团具有与氧化剂反应的能力,称作自燃反应性基团,其数量与点火延迟时间有较强的关联性。结合对初始点火反应能量的计算,设计HILs 的基本思路被提出:首先对结构进行理论优化以得到稳定的构型,进而计算其轨道能级差、反应自由能变和焓变,要求其轨道能级差小于[NO3],反应自由能变和焓变应为负值;最后,选择合适的另一种离子以使离子液体具备优异物理性质[40]。
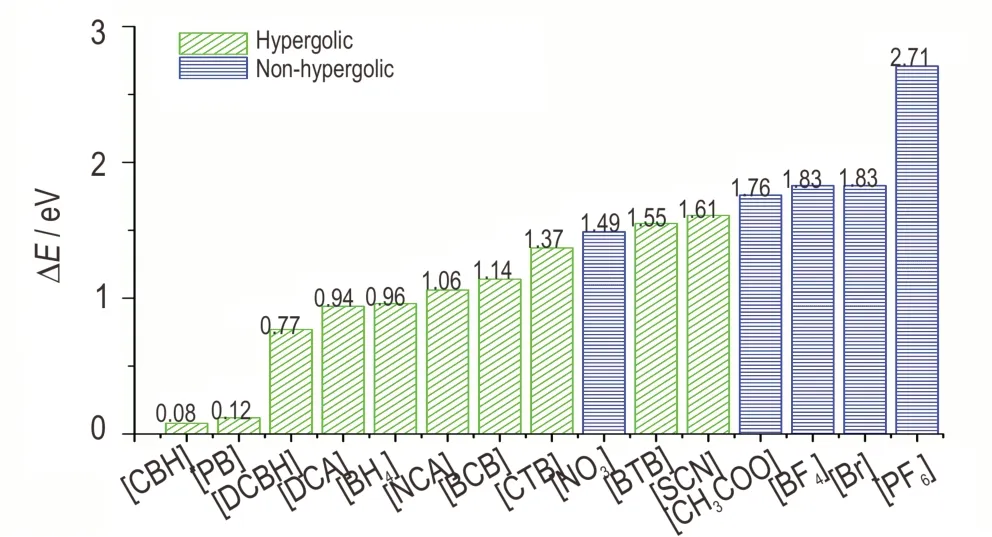
图2 几种自燃和非自燃阴离子与硝酸之间的轨道能级差[40]Fig.2 The energy gaps of hypergolic and non-hypergolic anions[40]
综上所述,由于反应动力学模型的建立比较复杂,不能直接对反应过程进行定量的计算和分析,所以对自燃性的理论预测还不够完善和准确。不同的点火测试方法对同一种HIL 可能有不同的结果,这使基于数据的数学模型法的准确性受到了很大的限制。轨道能级差是一种较为简便的判断反应性的方法,值得进一步研究与完善。
5 结论与展望
HILs 具有极低蒸汽压和结构性质可设计性,是一种优异的绿色含能材料,有望成为新一代推进剂燃料。本研究从多个方面对HILs 的点火燃烧机制进行了分析和总结:关于二氰胺阴离子与硝酸的反应机理,普遍共识认为反应由质子的传递而始,NO2的迁移大量放热,反应过程中存在CO2、N2O 和HNCO 等产物;点火过程展现出阶段化的特点,通常要经历接触和扩散、反应和放热、温度提升和点火火焰四个阶段;基于数学模型和结构性质关系能够一定程度上实现对离子液体自燃性的预测。总体上讲,这些研究尚处于初级阶段,存在研究不完善、理解不透彻等问题。未来应该有针对性地解决HILs 在点火燃烧研究中存在的不足,未来的发展方向建议包括以下几个方面:
(1)开发先进的表征测试方法。除[DCA]和WFNA 的反应与机理外,关于其他阴离子的研究尚未开展,而关于点火测试方法也没有一定的规范,发展的瓶颈是表征和测试方法的不够完善。实现对反应过程中瞬态物质的精确检测,实现点火延迟时间的强重复性,是开发先进的表征测试方法的主要目标。
(2)加强对燃烧过程与现象的深入研究。关于燃烧过程与现象的研究很少,然而对应用而言,获得燃烧方面的参数是相当重要的。未来的研究测试应该更加接近实际应用,比如研究其在推进室里的表现。
(3)研发绿色双组元推进剂。寻找与HILs 组合的绿色氧化剂将是未来有前景的发展方向。目前大部分研究所使用的氧化剂依然是发烟硝酸、四氧化二氮等强腐蚀性的有毒物质。双组元推进剂实现完全绿色化必须要发展能够与绿色氧化剂例如双氧水配合的自燃燃料。然而,现在大多数HILs 与H2O2的点火延迟时间都较长,需要从离子液体的结构、催化剂以及反应条件的设计与调控等诸多方面做更深入的研究。
