氟啶虫酰胺衍生物的设计合成与生物活性
2020-05-09杨子辉
杨子辉*,田 昊
(山东金华海生物开发有限公司,山东济南 251400)
吡啶酰胺类化合物具有杀虫、杀菌和除草等广谱生物活性,在杀菌和杀虫领域均已经有相关品种上市[1-2]。巴斯夫 2002年首次登记的琥珀酸脱氢酶抑制剂(SDHI)类杀菌剂啶酰菌胺(boscalid)即为广谱、内吸性杀菌剂,它可以防治果蔬和其他作物的由子囊菌和半知菌引起的病害,该类杀菌剂在2011年的销售额为5.81亿美元[3-5]。
氟啶虫酰胺(flonicamid)是日本石原产业在参考三氟甲基吡啶结构的杀菌剂和除草剂的基础上开发的新型吡啶酰胺类杀虫剂[6],通过阻碍害虫吮吸作用而发挥效果。害虫摄入药剂后很快停止吮吸,最后饥饿而死。氟啶虫酰胺主要用于非农作物、棉花、水果和蔬菜,对各种刺吸式口器害虫有效,具有良好的内吸和渗透作用[7],可从植物根部向茎部、叶部传导。氟啶虫酰胺2005年在美国上市用于花卉,2007年在中国、日本、意大利上市,用于水果和蔬菜,2011年在加拿大登记, 2011年全球市场销售额约为4 000万美元。2013年在中国的化合物专利到期,目前国内已有多家农化企业登记该品种原药和复配制剂[8]。
河北艾林科技有限公司 2017年设计合成的烟酰胺类化合物G1701(C)在4.0 mg/L对瓜蚜具有较好的抑制活性,达94%,优于啶虫脒,其5%乳油具有速效和与其他杀虫剂无交互抗性的特点[9]。
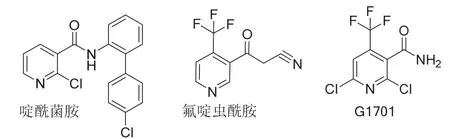
为获得具有杀虫活性的吡啶酰胺类化合物,笔者以石原产业的商品化杀虫剂氟啶虫酰胺为先导,通过变换吡啶环上羧基的位置,设计了氟啶虫酰胺衍生物。本文对其设计合成与杀虫活性进行报道。
1 材料与方法
1.1 仪器
ZF-2型三用紫外仪(上海安亭电子仪器厂);RE-52C型旋转蒸发仪、SHB-Ⅲ型循环水式多用真空泵(郑州长城科工贸有限公司);RY-1G 型熔点仪(天津天光光学仪器有限公司);核磁共振仪(BRUKER,400 MHz,CDCl3溶剂,TMS 内标);Agilent 1100 Series型高效液相色谱-质谱联用系统(EI,美国Agilent公司);薄层层析硅胶板(烟台江友硅胶开发有限公司)。
1.2 试剂
5-三氟甲基吡啶-3-羧酸(上海毕得医药科技有限公司);5-三氟甲基吡啶-2-羧酸(上海毕得医药科技有限公司);EDCI (Adamas-beta,上海泰坦科技有限公司);HObt (Adamas-beta,上海泰坦科技有限公司);三乙胺(华伦化工);其他溶剂和试剂均为市售分析纯或化学纯。
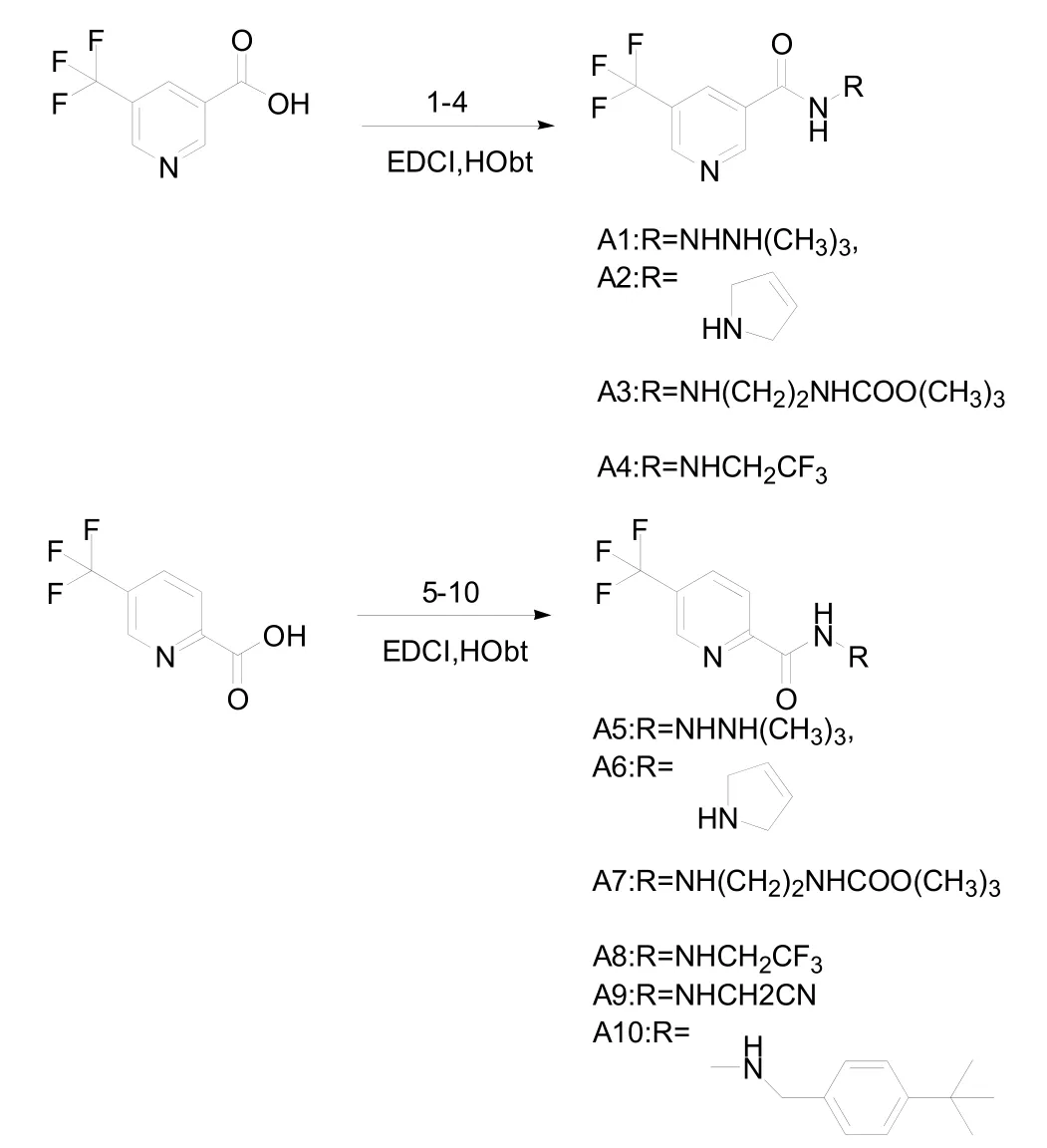
图1 目标化合物A的合成路线
1.3 化合物合成
1.3.1 目标化合物A1的合成
5-三氟甲基吡啶-3-羧酸(0.191 g, 1.0 mmmol)和叔丁基肼盐酸盐(0.124 g, 1.0 mmol)溶解于25 mL二氯甲烷中,加入Et3N (0.202 g, 2.0 mmol),随后加入1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCI,0.287 mg, 1.5 mmol)、1-羟基苯并三唑(HOBt, 0.20 g,1.5 mmol), 25oC反应3 h,TLC检测反应完全。反应液以水洗涤(20 mL×2),饱和食盐水洗涤(20 mL×1),无水硫酸钠干燥,脱溶,粗品柱层析得无色液体,收率:78%。1H NMR (500 MHz, CDCl3)δ: 8.87 (d,J=2.0 Hz, 1H, pyridine), 8.65 (s, 1H, pyridine), 8.54 (d,J=2.0 Hz,1H, pyridine), 6.80 (s, 1H, NH), 2.20 (s, 1H,pyridine), 1.25 (s, 9H, C(CH3)3)。
1.3.2 目标化合物A2的合成
参考 1.3.1的合成方法,2,5-二氢吡咯盐酸盐(0.105 g, 1.0 mmol)为后加入的物质,25 ℃反应2 h,得黄色液体,收率:76%。1H NMR (500 MHz, CDCl3)δ: 9.03 (d, J=2.0 Hz,1H, pyridine), 8.75 (s, 1H,pyridine), 8.28 (d, J=2.0 Hz,1H, pyridine), 5.80-5.75(m, 2H, CH=CH), 3.68-3.62 (m, 4H, CH3)。
1.3.3 目标化合物A3的合成
参考1.3.1的合成方法,25oC反应2 h,得白色固体,m.p.31~33 ℃,收率:70%。1H NMR (500 MHz,CDCl3) δ: 8.89 (d, J=2.0 Hz,1H, pyridine), 8.72 (s, 1H,pyrindine), 8.39 (d, J=2.0 Hz, 1H, pyridine), 3.34-3.37(m, 2H, NHCH2), 3.26-3.29(m, 2H, NHCH3), 1.49 (s,9H, OCH3)。
1.3.4 目标化合物A4的合成
参考1.3.1的合成方法,25 ℃反应1.5 h,得黄色液体,收率:82%。1H NMR (500 MHz, CDCl3) δ:9.00 (d, J=2.0 Hz, 1H, pyridine), 8.68 (s, 1H,pyrindine), 8.39 (d, J=2.0 Hz,1H, pyridine), 4.33 (s,2H, CH2)。
1.3.5 目标化合物A5的合成
5-三氟甲基吡啶-2-羧酸(0.191, 1.0 mmol)和叔丁基肼盐酸盐(0.124 g, 1.0 mmol)溶解在25 mL二氯甲烷中,加入Et3N (0.202 g, 2.0 mmol),随后加入EDCI (0.287 mg, 1.5 mmol),HOBt (0.20 g, 1.5 mmol),25 ℃反应2.5 h,TLC检测反应完全。反应液以水洗涤(20 mL×2),饱和食盐水洗涤(20 mL×1),无水硫酸钠干燥,脱溶,得到深黄色固体,m.p.22~25 ℃,收率:72%。1H NMR (500 MHz, CDCl3) δ: 8.50(d, 1H,J=1.2 Hz, pyridine), 7.80 (dd, 1H, J1=6.0 Hz, J2=1.2 Hz, pyridine), 7.50 (d, 1H, J=6.0 Hz, pyridine), 1.30 (s,9H, C(CH3)3)。
1.3.6 目标化合物A6的合成
参考 1.3.5的合成方法,2,5-二氢吡咯盐酸盐(0.105 g, 1.0 mmol)后加入反应液中,25 ℃反应2 h,得到黄色液体,收率:82%。1H NMR (500 MHz,CDCl3) δ: 8.53 (d, J=2.0 Hz,1H, pyridine), 7.83 (dd, 1H,J1=6.0 Hz, J2=1.2 Hz, pyridine), 7.56 (d, 1H, J=6.0 Hz,pyridine), 5.82-5.73 (m, 2H, CH=CH), 3.70-3.62 (m,4H, CH2)。
1.3.7 目标化合物A7的合成
参考1.3.5的合成方法,25 ℃反应1.5 h,得到黄色固体,m.p.26~28 ℃,收率:76%。1H NMR (500 MHz,CDCl3) δ: 8.63 (d, 1H, J=1.2 Hz, pyridine), 7.90 (dd, 1H,J1=6.0 Hz, J2=1.2 Hz, pyridine), 7.53 (d, 1H,J=6.0 Hz,pyridine), 3.38-3.35 (m, 2H, NHCH2), 3.25-3.28 (m,2H, NHCH2), 1.49 (s, 9H, OCH3)。
1.3.8 目标化合物A8的合成
参考1.3.5的合成方法,25 ℃反应2 h,得到棕色液体,收率:82%。1H NMR (500 MHz, CDCl3) δ:8.45 (d, 1H, J=1.2 Hz, pyridine), 7.83 (dd, 1H, J1=6.0 Hz,J2=1.2 Hz, pyridine), 7.56 (d, 1H, J=6.0 Hz, pyridine),4.30 (s, 2H, CH2)。
1.3.9 目标化合物A9的合成
参考1.3.5的合成方法,25 ℃反应2 h,得到棕色液体,收率:81%。1H NMR (500 MHz, CDCl3) δ:8.30 (d, 1H, J=1.2 Hz, pyridine), 7.89 (dd, 1H, J1=6.0 Hz, J2=1.2 Hz, pyridine), 7.58 (d, 1H, J=6.0 Hz,pyridine), 4.80 (s, 2H, CH2)。
1.3.10 目标化合物A10的合成
参考1.3.5的合成方法,25 ℃反应3 h,得到黄色液体,收率:82%。1H NMR (500 MHz, CDCl3) δ:8.68 (d, 1H, J=1.2 Hz, pyridine), 7.93 (dd, 1H, J1=6.0 Hz,J2=1.2 Hz, pyridine), 7.59 (d, 1H, J=6.0 Hz, pyridine),7.33-7.15 (m, 4H, phenyl), 4.60 (s, 2H, CH2), 1.40 (s,9H, (CH3)3).
1.4 对化合物A进行杀虫活性测试[10]
1.4.1 化合物配制
用分析天平(0.000 1 g)称取一定质量的目标化合物,用含1%吐温-80乳化剂的DMF溶解配制成1%母液,然后用蒸馏水稀释备用。
1.4.2 试验方法
喷雾法:试验对象为苜蓿蚜,分别将接种苜蓿蚜的蚕豆叶片置于 Potter喷雾塔下喷雾处理,处理后将蚕豆叶片置于20~22 ℃观察室内培养,48 h后调查结果。以毛笔触动虫体,无反应视为死虫。试验浓度500 mg/L。
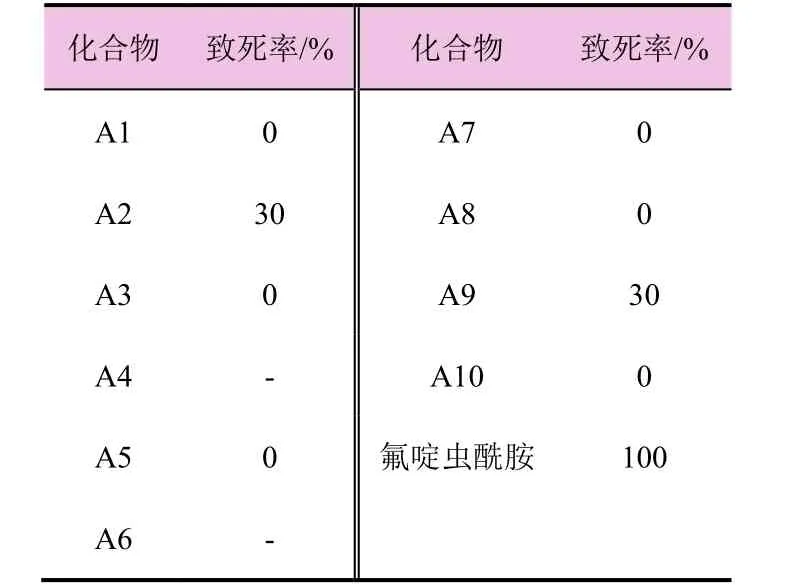
表1 化合物A对苜蓿蚜的抑制率
2 结果与讨论
2.1 合成
目标化合物由含三氟甲基的吡啶甲酸和胺缩合反应制备,以二氯甲烷作溶剂,EDCI做缩合剂,三乙胺做碱,原料反应完全,后处理以重结晶方式得目标A系列化合物。化合物合成方法简便,废水较少,收率较高,相比酰氯与胺合成酰胺的方法,是比较绿色环保的合成方法。
2.2 表征和活性
以目标化合物A10为例,氢谱中化学位移4.60示为苄基的亚甲基上的2个氢,1.40示为苄基的叔丁基的9个氢,芳香区中7.93裂分为dd峰,示为吡啶环上的氢。
A系列化合物在500 mg/L浓度下对苜蓿蚜有一定的致死活性;其中化合物A2和A9对苜蓿蚜的致死率达30%,但与氟啶虫酰胺商品药相比,仍有一定差距。该系列化合物的结构优化正在进行中。
该类化合物仍需要进一步优化,对开发氟啶虫酰胺有一定指导意义。
