喹诺酮类药物印迹仿生抗体的研制及应用进展
2020-05-08杜晓芳李兆周陈秀金王耀高红丽李道敏任国艳吕璞
杜晓芳,李兆周,陈秀金,王耀,高红丽,李道敏,任国艳,吕璞
(河南科技大学食品与生物工程学院,食品加工与安全国家级实验教学示范中心/河南省食品原料工程技术研究中心,河南洛阳471000)
喹诺酮类药物是一类重要的人工合成抗菌药物,具有抗菌谱广、活性强、组织穿透力强、价格低廉和交叉耐药性低等特点,广泛应用于抗感染治疗中[1-3]。过去的几十年,喹诺酮类药物在畜禽及水产品养殖中的不合理使用,导致其在动物性食品及环境中的残留量超标,严重威胁人类健康,常见的不良反应包括骨髓发育不全、过敏反应和肠道微生态的改变等[4-9],该类药物的残留检测已成为亟待解决的问题之一。目前常见的喹诺酮类药物残留检测方法有微生物法[10]、免疫分析法[11-13]、色谱法[14]、电化学分析法[15-16]、光谱法[17]和高效液相色谱-质谱联用法[18-19]等。但由于样品基质复杂多样,常规单一方法对于该类药物的检测存在一定的局限性,如微生物法难以定量;免疫分析法易出现假阳性且不稳定;高效液相色谱-质谱联用法检测成本昂贵等。因此,建立一种准确、快速、灵敏且高效的方法用于样品中喹诺酮类药物残留的检测迫在眉睫。
分子印迹技术是一种具有特定选择性和亲和能力的新兴聚合技术。通过分子印迹技术制备的具有类似抗体或酶专一性的仿生识别材料称为分子印迹聚合物(molecularly imprinted polymer,MIPs),也称为印迹仿生抗体[20]。分子印迹仿生抗体因具有结构预定性、实用性、稳定性好及制备简单的优点,能特异性识别靶物质,对极端环境具有很强的耐受能力,可代替生物源识别元件用于复杂基质中目标化合物的定性和定量分析[21]。目前,该仿生识别材料已广泛应用于色谱、固相萃取(solid phase extraction,SPE)[22-23]、模 拟 酶[24-25]、仿 生 传 感器[26-27]、膜分离[28-29]和临床药物分析等领域,同时也在食品、环境和生物样品的分离、纯化和富集分析中展示出广阔的应用前景。
仿生免疫分析是利用分子印迹仿生抗体的特异性识别能力而建立的一种亲和分析方法,是近几年研究的热点之一,如Chen 等[30]报道了一种以分子印迹仿生抗体作为抗体替代物的仿生酶联免疫吸附试验方法,其检测范围为5~1000μg/mL,加标牛血清样品回收率达89.00%~102.30%;Yao 等[31]报道了一种新型仿生纳米酶用于检测过氧化氢,具有10μmol/L~4mmol/L 的宽线性范围,检测限达5μmol/L。本文主要介绍喹诺酮类药物印迹仿生抗体的制备方法,总结其在食品与环境检测中的应用;结合分子印迹技术的最新研究进展,讨论了该类药物仿生抗体在制备及识别过程中面临的问题,提出了可能的解决途径与方案,为新型印迹仿生抗体的研制及应用提供理论依据和技术途径。
1 喹诺酮类药物印迹仿生抗体的制备方法
目前喹诺酮类药物印迹仿生抗体的制备方法主要有本体聚合法、分散聚合法、悬浮聚合法、原位聚合法和表面分子印迹法等。不同制备方法所得印迹仿生抗体的性能参数比较见表1。
由表1可看出,制备出的喹诺酮类药物印迹仿生抗体的形态主要有块状、球状和薄膜等几种,不同制备方法的印迹效率不同。表中本体聚合法的印迹因子较高,但其检测回收率却不如其他制备方法,可能是合成印迹仿生抗体时的研磨过程破坏了部分识别位点的空间排列;模板分子的包埋现象使模板分子洗脱不彻底,在吸附过程中仍然占据部分孔穴,致使其吸附选择性降低。因此,如何完善和创新现有制备技术来提高印迹效率和检测回收率是分子印迹领域亟待解决的问题。下面就每种制备方法的特点进行详细介绍。
1.1 本体聚合法
本体聚合法是最传统和常用的制备方法,通常是在热引发或紫外光照射的条件下,合成高度交联的块状MIPs。孙慧等[32]以氧氟沙星(ofloxacin,OFL)作为模板分子,MAA 为功能单体,PETRA为交联剂和2, 2- 偶氮二异丁腈 (2, 2-azobisisobutyronitrile,AIBN)为引发剂,在紫外光照射条件下合成MIPs,而且该MIPs 能够专一性有效 识 别OFL。 Benito-Peña 等[33]以 恩 诺 沙 星(enrofloxacin,ENR)为模板,通过热引发制备了一种新型水相容性MIPs,用于在水中选择性提取氟喹诺酮类药物(fluoroquinolone drugs,FQs)。但传统的本体聚合法需要经过研磨筛分得到所需大小的粒子,费时费力,产率一般低于50%,后处理过程易破坏识别位点结构,且形成的微粒形态不规则,多呈分散性。

表1 喹诺酮类药物印迹仿生抗体的制备方法及性能参数
1.2 悬浮聚合法
悬浮聚合法是指将溶有引发剂的功能单体以液滴状悬浮于水中进行自由基聚合的方法。此种方法的制备工艺简单,所得MIPs 的形态规则、比表面积大、吸附和识别性能较强,是制备聚合物微球最简便和最常用的方法之一。陈令涛等[34]以环丙沙星(ciprofloxacin,CIP)为模板分子,使用悬浮聚合法制备MIPs,结果表明在最优条件下饱和吸附量可达210.6mg/g,经5 次再生后吸附量仍能达到初始吸附量的92.3%。悬浮聚合法所得聚合物微球粒径较大,是亲和SPE的理想填料,但该方法易造成模板分子包埋过深,难于洗脱,以致模板分子泄漏,影响分析方法的精确性。
1.3 原位聚合法
原位聚合法是将预聚合溶液注入到色谱柱或毛细管柱等反应容器中直接聚合得到连续棒状MIPs,该方法制备简便,避免了传统制备方法中磨碎等步骤,在线洗脱后可直接应用,重复性得到显著提高。李兆敏等[35]用原位聚合法合成了CIP 分子印迹整体柱,该法简便经济,得到的MIPs直径在0.2~0.5μm之间,具有良好的均一性和连续性。
传统原位聚合方法制得的分子印迹整体柱的装样量少、选择性略差、效率不够高且易产生壁流。为改善这一缺点,可选择室温离子液体做溶剂及致孔剂应用于MIPs 的制备。室温离子液体不仅具有优异的溶剂化质量、可变的黏度范围、较低的蒸汽压和优异的化学热稳定性等特性,并可加速聚合物合成速率、提高聚合物特异性识别和结合能力。Sun等[36]在室温离子液体[BMIm]BF4中采用室温离子液体介导原位聚合技术,以诺氟沙星(norfloxacin,NFX)为模板,制备出一种新型MIPs。利用该MIPs 作为SPE 填料,建立了分子印迹固相萃取偶联高效液相色谱法(molecularly imprinted solidphase extraction coupling with high performance liquid chromatography,MISPE-HPLC),用于检测动物组织样品中痕量的FQs,回收率可达78.16%~93.50%。
通过原位聚合法也可以制备仿生传感器的识别元件,实现靶物质的特异检测。Luo 等[37]以CIP 为模板分子,采用原位光引发聚合法制备了纳米级仿生印迹膜,作为表面等离子体共振(surface plasmon resonance,SPR)传感器的识别元件,用于CIP 的检测(制备流程见图1)。在10-11~10-7mol/L浓度范围内,该传感器的线性相关系数为0.96,检测限为0.08μg/L,具有灵敏度高、检测限低、重复性和稳定性好等优点。

图1 原位光引发聚合法制备等表面等离子共振传感识别元件[37]
1.4 沉淀聚合法
沉淀聚合法是一种操作简便、成本低、产率高且印迹效果较好的方法,得到的微球颗粒较小、比表面积大且吸附性能优异。张莉等[38]采用沉淀聚合法,以四环素和NFX 为模板分子,制备仿生识别材料,作为SPE吸附剂检测蜂蜜和奶制品中的药物残留,加标回收率为82.12%~96.51%,相对标准偏差小于5.0%,检测限为0.2ng/g。Benito-Peña等[39]以ENR 为模板分子,MAA 为功能单体,2-甲基丙烯酸羟甲基酯为亲水性共聚单体,应用沉淀聚合法制备出具选择性识别能力的单分散MIPs微球,尺寸可控制在2~3μm范围内。Wu等[40]以异硫氰酸荧光素为发光材料,采用沉淀聚合法合成荧光分子印迹纳米粒子,检测水样中的CIP。结果显示,方法检测线性范围较宽,为4.04~250nmol/L,荧光特性检测限为4.04nmol/L,在一定程度上发挥了分子印迹技术的应用潜力,见图2。
1.5 溶胶-凝胶法
溶胶-凝胶技术具有可低温合成与处理、操作简单方便、产品均匀度高、纯度高等特点。杜丽丽等[41]以加替沙星为模板分子,采用溶胶-凝胶分子印迹技术,在水相中合成具有分子识别作用的新型有机-无机杂化仿生抗体材料,并以此为固相填料专一性检测牛奶中的加替沙星,回收率可达79.87%,检测限为1.12μg/L。Wang 等[42]以ENR 为模板,APTES 为功能单体,TEOS 为交联剂制备分子印迹功能化溶胶-凝胶,检测鱼肉和鸡肉中痕量的ENR,回收率可达70.00%~82.00%。通过溶胶-凝胶法制备的新型杂化仿生材料兼顾了溶胶-凝胶和分子印迹技术二者的优点,克服了传统分子印迹仿生材料的刚性与惰性较差的缺点,正逐渐成为分子印迹技术的一个重要研究方向。
1.6 表面分子印迹
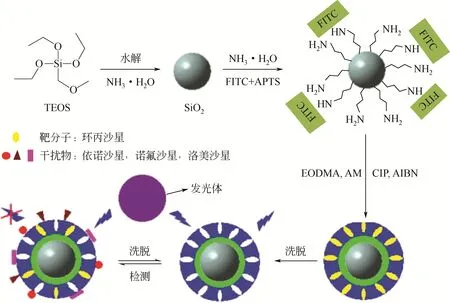
图2 荧光分子印迹纳米粒子的制备流程[40]
表面分子印迹是指在固体基底表面发生聚合反应,使印迹位点分散在MIPs或有机化合物的表面,克服了印迹位点包埋过深、模板分子难于洗脱的缺陷,加快识别位点与印迹分子的结合速率,进一步加强印迹材料吸附和分离效率。贺永桓等[45]以OFL为模板分子,Fe3O4磁性纳米颗粒为载体,采用可逆加成-断裂链转移聚合方法,制备出具有高选择性、快速识别和磁操控的核壳型分子印迹纳米材料。同样,Wang 等[43]以CIP 为模板,Fe3O4为磁性材料,羧化纤维素纳米晶体为载体,共聚合制备MIPs,选择性吸附容量可达50mg/g,具有适宜的饱和磁化强度,可同时应用于6种FQs的选择性识别。与传统的制备方法相比,磁性表面MIPs 解决了传统MIPs 模板分子包埋过深、洗脱难的问题,且结合位点在磁性载体表面,比表面积大、选择性高。但可能存在MIPs 对磁载体的包裹不完全,易发生磁泄漏问题。因此,提高仿生抗体对磁性微粒的包裹率,减少磁泄漏,是提高磁性表面MIPs 稳定性的关键。此外,表面分子印迹法也可以选择硅胶、有机聚合物载体及毛细管等材料作为基质进行聚合反应。Zdunek 等[44]以ENR 为模板在多孔氧化铝中制备纳米丝结构仿生材料,开发出一种新的光学传感器对ENR 进行特异性分析检测。该方法简便,重现性好,用于水样中ENR 的检测,检测限为0.58μmol/L。
1.7 其他合成方法
近几年研究者们也逐渐探索出一些新型的方法来合成喹诺酮类药物印迹仿生抗体。Wang 等[46]开发出一种MIPs薄膜(模式图如图3所示),将其作为仿生抗体,建立一种直接竞争仿生酶联免疫方法检测动物食品中的ENR,回收率为74.40%~86.80%,相对标准偏差在3.3%~8.0%范围内。该方法结合了分子印迹技术和酶联免疫技术的优点,经济可靠、使用简便,具有广阔的应用前景,但该方法的特异性和抗干扰能力仍待优化,MIPs 膜的理化特性,特别是识别能力、柔韧性和稳定性仍需深入研究。
2 喹诺酮类药物印迹仿生抗体在食品及环境检测中的应用进展
喹诺酮类药物印迹仿生抗体作为一种基于分子识别的高聚物,常被用作SPE填料及仿生传感器的识别元件,应用于食品及环境样品中喹诺酮类药物的残留检测。喹诺酮类药物印迹仿生抗体用于实际样品的检测见表2。
由表2可知,喹诺酮类药物印迹仿生抗体应用于实际样品的检测方法主要有MISPE-HPLC、MIMSPD-HPLC、电化学传感器和光学传感器等几种方式;检测的样品包括食品(肉、蛋及奶)和环境(土壤和水样)等领域。结果显示,上述各种分析检测方法的回收率较高,检测限最低可达8.985×10-5μg/kg。

图3 分子印迹薄膜的制备过程[46]
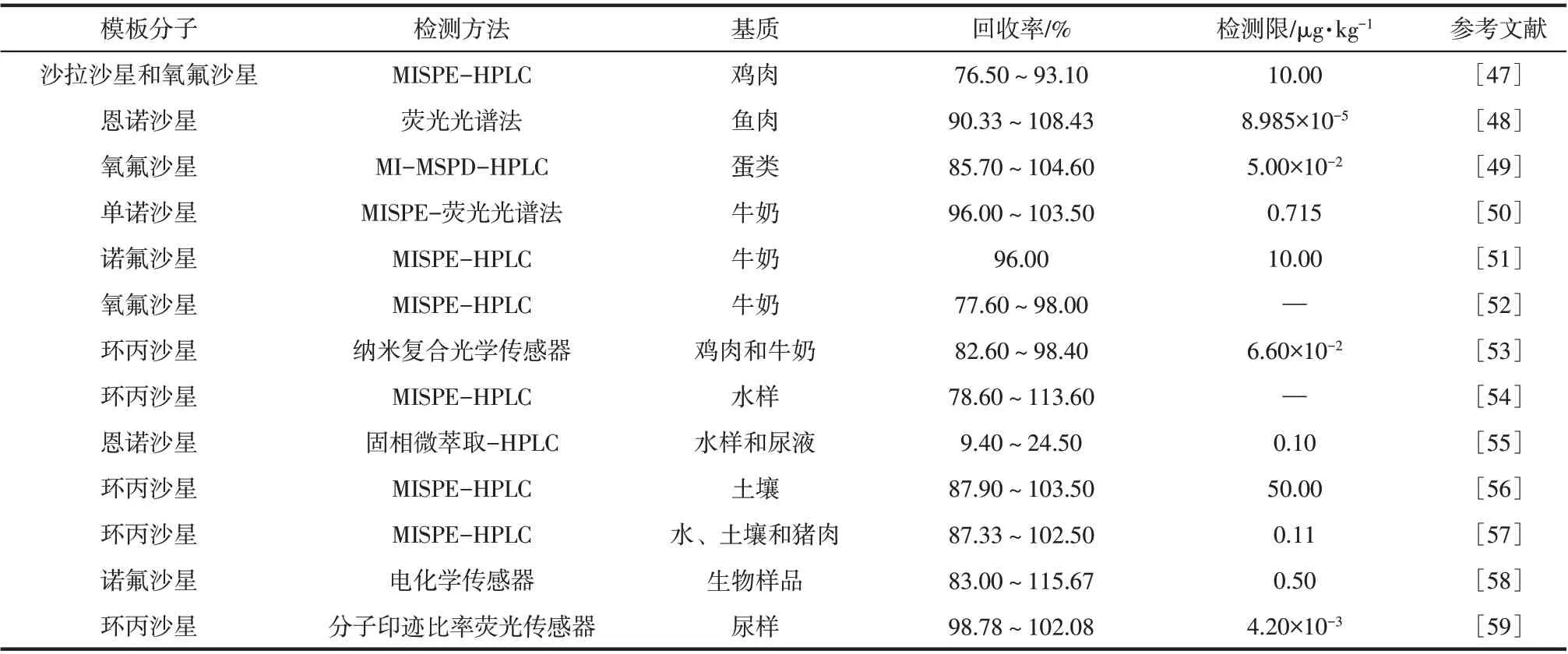
表2 喹诺酮类药物印迹仿生抗体用于实际样品的检测
2.1 肉品中喹诺酮类药物残留检测
将制备的MIPs 作为一种SPE 吸附填料,可以较好地克服样品复杂所带来的内源性干扰问题,实现对残留药物的特异性分离和富集。兰翠娟[47]以双模板MIPs制备SPE柱,结合HPLC方法检测样品中的FQs,对7 种FQs 的日间回收率为76.50%~91.80%,日内回收率为78.00%~93.10%。与单模板分子的MIPs相比,双模板MSPE-HPLC 用于FQs的残留检测更加简便和准确。
荧光标记技术也可用于MIPs 的制备。Tang等[48]应用局部光聚合法制备多功能MIPs 荧光探针,用于FQs 的检测(探针制备如图4 所示)。该荧光探针不仅具有良好的磁性和优异的选择识别能力,还具有快速和灵敏的优点,用于鱼类组织中5 种FQs的检测,回收率可达90.33%~108.43%。
2.2 蛋品中喹诺酮类药物残留检测
对禽蛋中的FQs进行分析检测比较复杂,因为药物可能与蛋类中的脂蛋白结合、萃取溶剂与蛋基质也易形成乳液和泡沫,影响检测结果的准确性。常规方法包括液-液萃取、固相(微)萃取、超临界流体萃取等样品制备方法应用于分析禽蛋中的FQs,具有相对较低的回收率、繁琐的提取程序且无法同时提取多种FQs 等缺点。基质固相分散(matrix solid-phase dispersion,MSPD)是可以同时破碎、提取和净化固体、半固体或高黏度生物样品的最有前景的技术之一,可以解决液-液或固相萃取技术检测分析复杂生物样品中的缺点。MIPs 作为选择性MSPD吸附剂可用于环境和生物样品中的痕量FQs分析,具有灵敏度高、特异型强和精密度高等优点。Yan 等[49]提出一种高选择性的分子印迹-基质固相分散(molecular imprinting and matrix solid phase dispersion,MI-MSPD)多重分析方法。首次使用制备的仿生抗体材料作为特定的MSPD吸附剂,结合HPLC方法测定和分析鸡蛋和组织样品中的5 种FQs,该方法可消除基质干扰,显著提高对药物检测的选择性和灵敏度,回收率可达85.70%~104.60%。
2.3 奶中喹诺酮类药物残留检测
分子印迹仿生抗体也可与HPLC、毛细管电泳和高效液相色谱-质谱等仪器联用,应用于乳及乳制品中药物的残留检测。Kaur等[50]建立了一种高效的MISPE-荧光光谱法,可灵敏测定牛奶中的单诺沙 星,检 测 限 达2.0×10-9mol/L。Wang 等[51]应 用MISPE-HPLC方法测定牛奶中FQs残留,基于NFX的MIPs 固相萃取柱对4 种药物(CIP、NFX、ENR和洛美沙星)显示出较高的吸附容量(≥4520ng)和回收率(≥96.00%)。此外,该SPE柱与市售SPE柱相比具有更好的净化效果和重复性,可以重复使用50次以上。多模板制备的MIPs 同时测定乳及乳制品中多种残留药物,更加灵敏、快速。Zhang等[52]以OFL和17β-雌二醇为模板,改性单分散聚珠为载体,合成一种多模板表面MIPs,作为SPE 吸附剂同时测定牛奶样品中的痕量喹诺酮类和雌激素类物质,回收率达77.60%~98.00%。
Yuphintharakun 等[53]以CIP 为模板分子,通过溶胶-凝胶法合成仿生抗体。然后将羧酸功能化的多壁碳纳米管和嵌入仿生抗体内的CdTe 量子点组成纳米复合光传感器(构建原理图如图5 所示),用于鸡肉和牛奶中CIP的检测,具有高灵敏度、特异选择性和高亲和力等特点,检测限为0.066μg/L,回收率可达82.60%~98.40%。

图4 多功能分子印迹荧光探针的制备流程[48]
2.4 环境中喹诺酮类药物蓄积检测
土壤及水体中抗生素的残留和蓄积已成为一个新出现的环境问题,对土壤、水体安全以及全球公共卫生构成的威胁越来越大,亟需建立新方法进行检测。
MISPE已用于环境样品中残留药物的样品前处理,实现环境样品(水体、土壤和尿液等)中靶物质的选择性萃取。Qu等[54]分别以CIP和ITA为模板分子和功能单体,在金属离子介导下合成一种新型MIPs,用作SPE 吸附剂检测水样中4 种FQs 和2 种四环素药物,回收率可达78.60%~113.60%。与传统MIPs相比,该MIPs可显著增强印迹效应并具有更强的特异性吸附能力。Barahona 等[55]提出在聚丙烯中空纤维(polypropylene hollow fibers,HFs)孔中填充MIPs(制备方案如图6 所示),研制固相微萃取装置,结合HPLC-串联质谱方法检测水样和尿液中的FQs,检测限可达0.1~10g/L,相对标准偏差小于20%。
Turiel 等[56]以CIP 为模板,通过沉淀聚合制备MIPs,作为选择性吸附剂检测分析土壤样品中的FQs。在最优条件下,成功检测土壤样品中的5 种FQs,回收率可达87.90%~103.50%。Zhu 等[57]以CIP为模板分子,使用离子液体功能单体,在水中合成了一种新型的仿生材料(合成路线如图7 所示),已成功应用于水、土壤和猪肉样品中痕量CIP的分离和富集,回收率为87.33%~102.50%。
仿生传感器具有灵敏度高、线性范围宽和检测限低的优点,常用于环境中药物的残留检测。Liu等[58]采用沉淀聚合法,以NFX为模板分子,合成印迹仿生抗体,进一步功能化修饰,制备出快速和超灵敏检测NFX的电化学传感器(构建方法如图8所示),可用于制剂和生物样品中靶物质的快速检测。在最优条件下,该传感器的线性检测范围为0.003~3.125μmol/L,检 测 限 为1.58nmol/L。Liu等[59]利用高荧光碳点与CdTe 量子点结合,构建了一种多功能分子印迹比率荧光传感器,已成功应用于人尿样中CIP 的检测,线性范围为0~60nmol/L,检测限为0.0127nmol/L。

图5 环丙沙星纳米复合光传感器的构建原理[53]
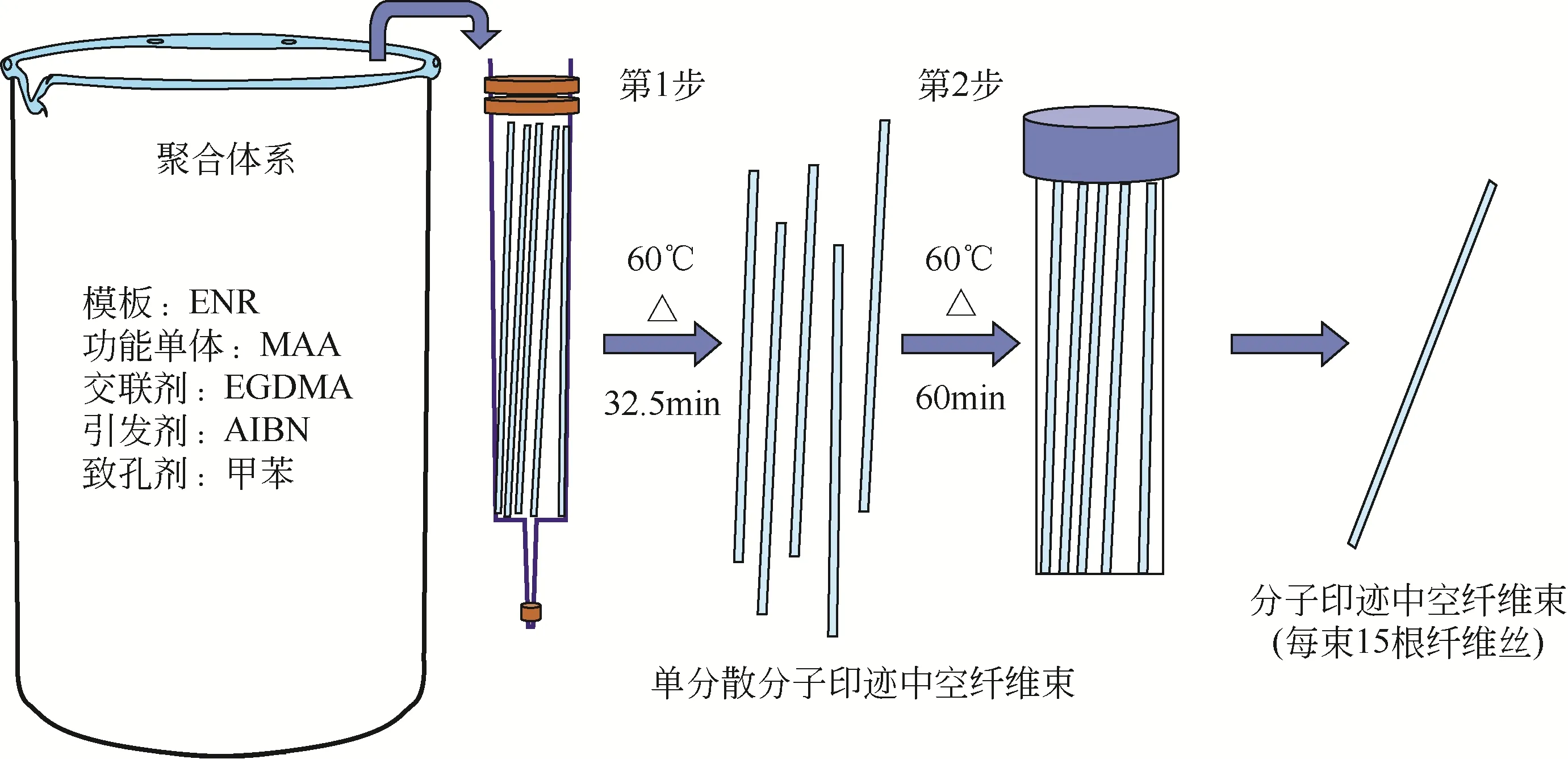
图6 制备分子印迹中空纤维束的两步聚合工艺方案[55]

图7 环丙沙星仿生识别材料合成示意图[57]
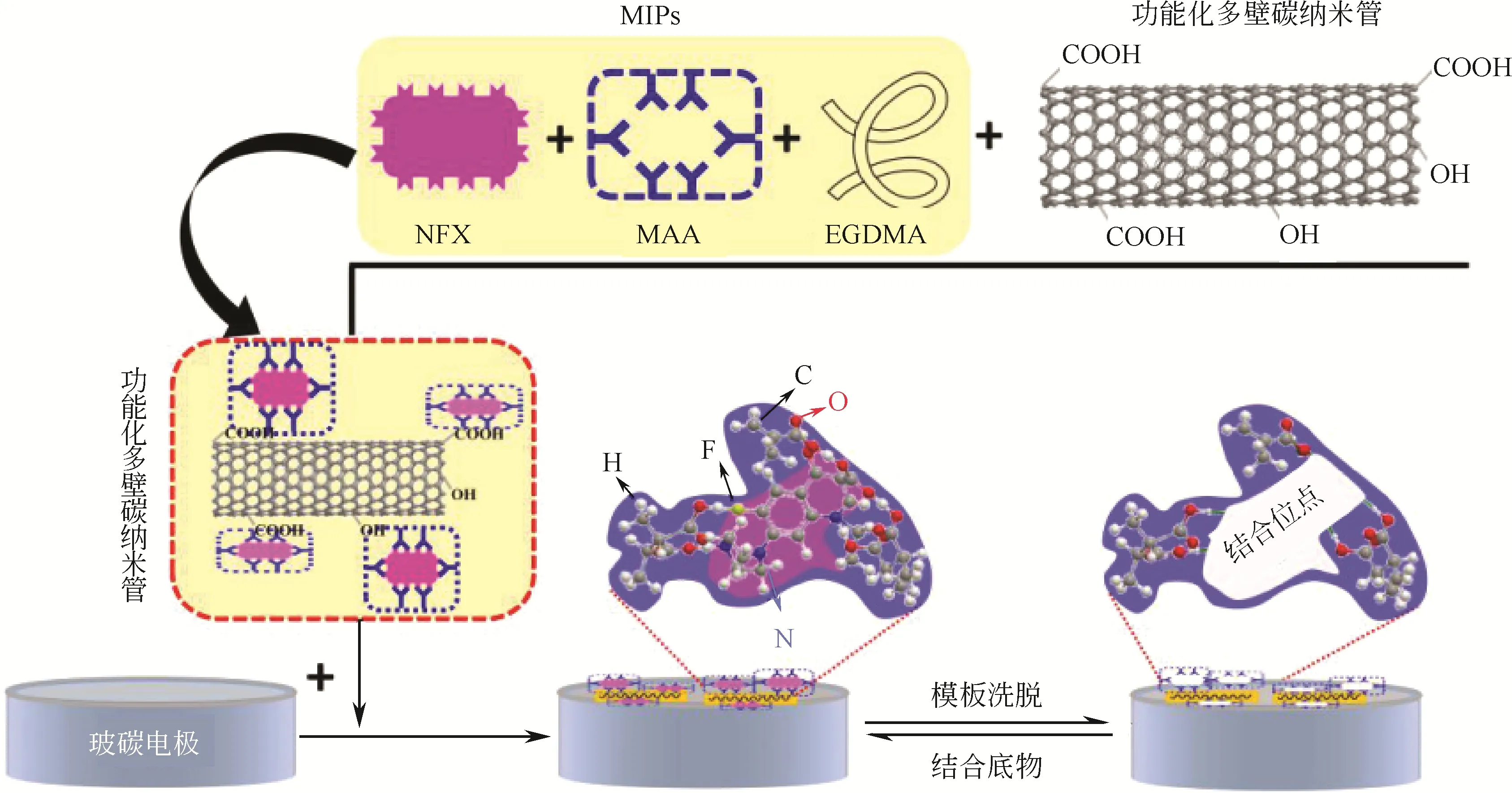
图8 分子印迹电化学传感器的构建[58]
3 结语与展望
分子印迹仿生抗体显示出良好的选择性、灵敏度和稳定性,已广泛应用于食品和环境安全领域。然而,目前喹诺酮类药物印迹仿生抗体在实际应用中仍面临一些挑战,尚难以完全替代传统检测方法。首先,合成的印迹仿生抗体过程中模板分子与聚合物的作用力较弱(主要靠氢键、静电、疏水及范德华力等),导致印迹容量和效应较低,严重限制了其向商业化规模发展;其次,对分子印迹过程及识别过程的机理、结合位点的作用机理、仿生抗体的结构和传质机理等方面的研究仍不透彻;此外,大多数分子印迹的合成和识别基本上都限制在有机相中,研究如何能够用特殊的分子间作用力在水溶液或极性溶剂中进行分子印迹和识别仍是目前难以解决的问题。
为解决以上问题,今后喹诺酮类药物印迹仿生抗体的研究应主要集中在以下几方面:寻找一些能够形成更强作用键的功能单体,或者将几种作用力偶合起来,增强印迹过程中的键合作用力;从分子水平上更好地理解和研究分子识别过程,制备出性质与天然抗体相类似的均质性结合位点的新型分子印迹仿生抗体;通过优化分子印迹仿生抗体的合成条件,实现从有机相到水相的转变,使分子印迹仿生抗体能够代替生物抗体,构建和开发高性能识别模式,建立高保真仿生分析方法。
总之,从成本、生态和环境保护的角度来看,合成或寻找更适宜的功能单体和溶剂,开发更便捷的合成方法及构建高性能仿生识别模式,是新型喹诺酮类药物印迹仿生抗体研制及应用的重要发展方向。
