基于中智相似积分算法心肌超声造影系统自动定量分析缺血再灌注大鼠存活心肌
2020-05-03孙智超张运帷于海源沈文茜郭延辉田家玮杜国庆
孙智超,王 飞,张运帷,王 爽,于海源,沈文茜,陈 双,吴 言,郭延辉,田家玮,杜国庆*
(1.哈尔滨医科大学附属第二医院超声科,黑龙江 哈尔滨 150001;2.哈尔滨医科大学心肌缺血机理与诊疗技术省部共建教育部重点实验室,黑龙江 哈尔滨 150001;3.美国伊利诺伊大学斯普林菲尔德分校计算机系,美国 伊利诺伊 62703)
急性心肌梗死(acute myocardium infarction, AMI)后及时恢复心肌供血可减少心肌细胞损伤,保护心脏功能,但大量研究[1-2]表明血管开通常会造成心肌缺血再灌注(ischemia-reperfusion,I/R)损伤。不同缺血时间再灌注会导致心肌发生不同结局,且恢复血流灌注后,缺血心肌仍有部分虽然运动异常,但细胞依然存活,称为存活心肌[3]。研究[4]显示如果冠状动脉微循环受损严重,致存活心肌较少或缺失,即使开通阻塞的冠状动脉血管,心肌微循环仍无法恢复正常,预后无法改善。梗死心肌已无可挽救,但如存在存活心肌,则快速重建血运非常有价值,而如何准确识别存活心肌是临床亟待解决的难题。心肌超声造影(myocardium contrast echocardiography, MCE)可评估危险心肌微循环灌注情况及其局部收缩功能,进而较准确识别存活心肌。目前依赖操作者主观判断分析MCE图像,可重复性差。本研究采用本课题组研制的基于中智相似积分(neutrosophic similarity score, NSS)算法MCE分析系统识别大鼠存活心肌。
1 资料与方法
1.1 动物分组及模型制备 健康雄性SD大鼠12只(哈尔滨医科大学附属第二医院动物中心提供),体质量280~300 g,腹腔注射10%水合氯醛(0.3 ml/kg体质量)麻醉后保定在固定板上,肢端连接心电仪,气管插管连接小动物呼吸机,无菌条件下开胸,充分暴露心脏,剥开心包,于肺动脉圆锥和左心耳下方2~3 mm前室间沟处结扎冠脉左前降支时,用自制软管置于结扎环内,建立缺血再灌注模型,体表连接同步心电图,见ST段显著抬高、结扎部位下部心肌变白、左心室前壁运动减弱为阻断成功。阻断30 min(I/R-30组,n=6)或45 min(I/R-45组,n=6)后松开结扎线,抽去软管,结扎部位下心肌由发白变成紫红色,为心肌I/R模型建模成功。
1.2 仪器与方法 采用GE Vivid7彩色多普勒超声诊断仪,10S探头,频率8~11 MHz,分别于术前、阻断即刻及再灌注后7、14及28天行MCE检查。调节仪器至最佳显示状态并保持整个实验中设置不变。造影剂使用SonoVue(Bracco,Italy),经鼠尾静脉以 0.05 ml/s推注稀释造影剂,获得左心室短轴切面(乳头肌水平)造影视频图像,并将之存入光盘中用于图像脱机分析。图像纳入标准:①无明显声衰减;②左心室短轴心肌呈圆形;③左心室腔造影剂微泡充盈均匀、饱满;④左心室心肌灌注包括开始灌注-充盈-平台期。12只大鼠行超声造影共获得MCE视频60个,每组30个,所获左心室短轴乳头肌水平切面声像图图像均符合纳入标准。
采用基于NSS算法的MCE-NSS系统[5]从以下3个方面进行分析。
1.2.1 自动识别心、外内膜边界 ①计算机自动计算中智图像的相似度;②运用中智相似度完成图像转换;③均值聚类初始化超声图像区域;④利用水平集来迭代寻找心肌内外边界,自动识别心肌区域(图1)。
1.2.2 自动合理分区 系统自动从心腔圆心均匀发射射线,将心肌和心腔分为18个区(图2),自动计算乳头肌水平切面18个节段室壁增厚率(wall thickening, WT)及标化造影剂灌注强度值(contrast intensity, CI),WT=(左心室壁收缩末期厚度-左心室壁舒张末期厚度)/左心室壁收缩末期厚度。WT<0.3节段存在室壁运动减弱,标化CI<-54Pix的区域为灌注缺损区[6]。
1.2.3 危险各区域评估 阻断即刻将室壁收缩运动减弱或消失节段(WT<0.3)定义为危险节段;再灌注后危险节段划分为3个区域:①WT<0.3且CI<-54 Pix为危险中央区;②WT<0.3且CI>-54Pix为危险周边区;③WT>0.3且CI>-54Pix为危险恢复区。计算危险中央区、周边区和恢复区各占左心室短轴乳头肌水平切面整体节段的百分比,观察阻断即刻及术后7、14、28天时危险中央区、周边区和恢复区面积变化情况。
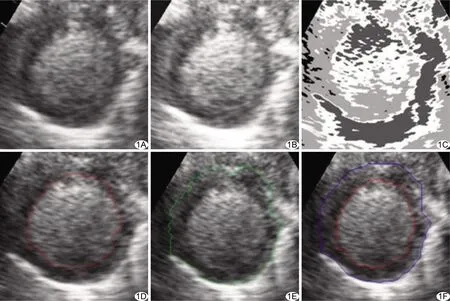
图1 NSS算法图像处理流程 A.原始MCE图像; B.中智相似度转换图像; C.中智活动轮廓模型结果; D.寻找心内膜边界; E.寻找心外膜边界; F.心肌最终分割结果

图2 MCE-NSS系统分析流程 A.原始MCE图像(阻断后); B.NSS算法分割后图像; C.系统自动将心肌和心腔分为18个区,并计算每个区心肌的WT和CI
1.3 病理学检查 术后28天麻醉大鼠后行心脏灌流术,于心尖注射10%氯化钾2~3 ml使心脏停止跳动于舒张期,取出心脏。以甲醛溶液固定24 h后,沿左心室短轴将心肌均匀切分为5等分(厚约2~3 mm)。对所获环状心肌组织行Masson染色,计算梗死心肌面积;行免疫组织化学染色,在200倍光学显微镜下观察并统计毛细血管数量,每张切片随机取4个视野取平均数,计算微血管密度(microvessel density, MVD)。
1.4 统计学分析 采用SPSS 21.0统计分析软件。连续性变量使用K-S正态性检验,采用±s表示符合正态分布的资料,组间比较采用独立样本t检验;组内比较采用单因素方差分析;以Pearson相关分析评价危险中央区面积与梗死面积及CI与MVD间的相关性,|r|≥0.8为相关性良好。P<0.05为差异有统计学意义。
2 结果
12只大鼠均建模成功。
2.1 MCE-NSS系统评估危险节段各区面积变化情况 术后7、14和28天,危险中央区百分比与阻断即刻相比无明显变化(P均>0.05),而危险周边区面积逐渐缩小(P均<0.01),危险恢复区面积逐渐增加(P均<0.01)。I/R-45组危险中央区面积术后各时间点均大于I/R-30组(P均<0.01),而2组危险周边区和恢复区面积差异均无统计学意义(P均>0.05),见图3。
2.2 MCE-NSS结果与病理结果的相关性 Masson染色显示I/R-30组梗死面积为12.66%,小于I/R-45组的24.72%(t=3.24,P<0.01),MCE-NSS危险中央区面积百分比和Masson染色测得梗死面积百分比呈正相关(r=0.81,P<0.01);危险周边区与恢复区均未见心肌坏死,证实为存活心肌,其中危险周边区即为顿抑心肌。见图4。免疫组织化学染色显示I/R-45组梗死周边区MVD为20.88%,较I/R-30组22.94%明显减少(t=2.26,P<0.05),危险周边区CI值与MVD呈正相关(r=0.86,P<0.01),见图5。
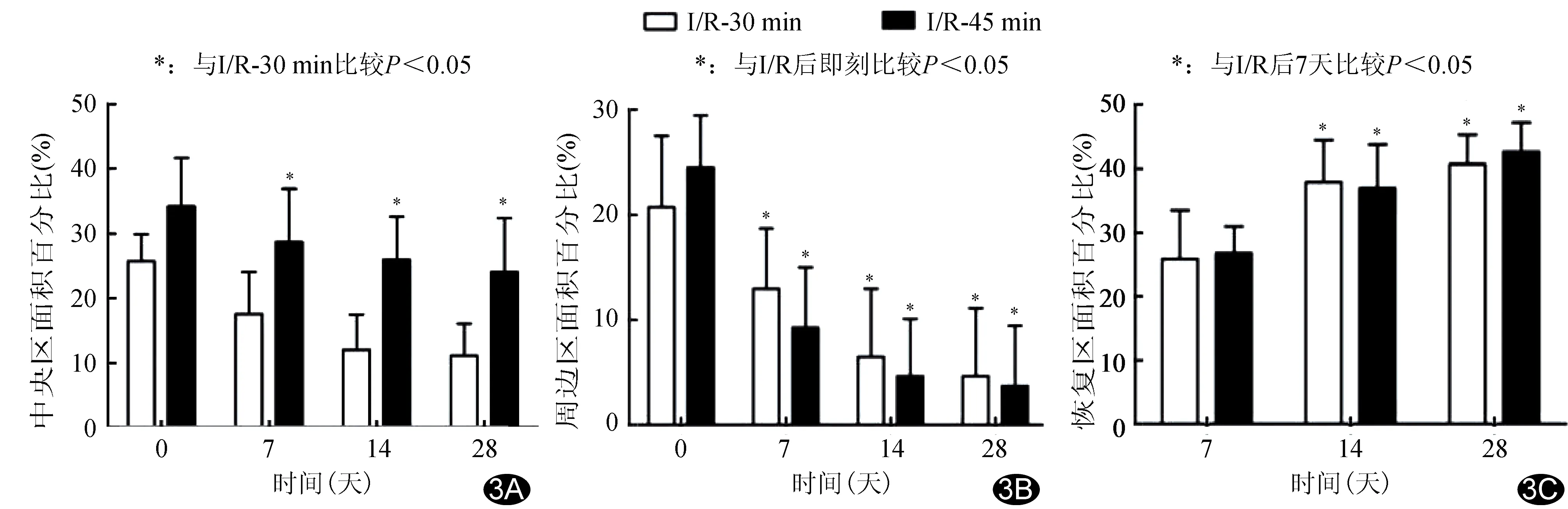
图3 术后不同时间点危险节段各区面积百分比比较 A.术后危险中央区面积百分比比较; B.术后危险周边区面积百分比比较; C.术后危险恢复区面积百分比比较
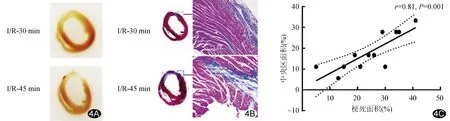
图4 Masson染色与MCE-NSS结果的相关性 A.心肌石蜡包埋; B.Masson染色(×200); C.Masson染色计算心肌梗死面积和MCE-NSS危险中央区面积的相关性散点图,二者呈正相关

图5 免疫组织化学染色和MCE-NSS结果的相关性 A.I/R-30组免疫组织化学染色(×200); B.I/R-45组免疫组织化学染色(×200); C.免疫组织化学染色计算MVD与MCE-NSS计算的危险周边区灌注强度的相关性散点图,二者呈良好正相关
3 讨论
计算机辅助诊断基于计算机对医学图像进行处理分析,以辅助影像医师诊断,提高诊断准确率。现有MCE分析主要依赖操作者主观判断,可重复性差,而计算机辅助诊断可弥补其缺陷。MCE-NSS系统可实现同时描记心内膜及心外膜边界,自动计算WT及CI,进而评估室壁运动及微循环情况[7]。
研究[8]表明,尽管及时开通阻塞血管,AMI患者仍会出现“低灌注”或“无复流”现象。MCE可定量评估心肌微循环灌注[9]。本研究应用MCE-NSS系统观察大鼠I/R模型危险中央区、周边区及恢复区各时间点变化情况,发现危险周边区和恢复区CI值于术后7天时最低,术后14、28天逐渐升高,原因可能在于缺血区域及周边心肌组织发生水肿、炎性改变等,影响了微循环血流灌注,心肌炎性反应及水肿消退后,心肌血流灌注得到改善。I/R-30组缺血时间较短,危险周边区和恢复区CI值在术后14、28天基本恢复正常,与术前比较差异无统计学意义;而I/R-45组危险中央区CI值至术后28天仍低于术前,且始终低于I/R-30组,原因可能在于较长缺血时间对心肌微循环结构造成更为严重的损伤,如果危险区域心肌微循环结构受到不可逆破坏,会出现持续灌注缺损[10]。术后28天危险周边区CI与MVD呈正相关,提示MCE-NSS软件能够定量评估缺血后局部微循环灌注情况。
存活心肌是指因梗死或缺血而导致收缩功能异常,血流恢复后收缩功能逐渐恢复的心肌[11],分为冬眠心肌和顿抑心肌[12],主要表现为代谢、收缩功能及微循环灌注减弱。核素心肌灌注显像是判断存活心肌的金标准[4],通过放射性核素标记对心肌灌注或代谢示踪而评估心肌存活性,但仅为半定量分析,且价格昂贵,临床应用并不广泛。负荷试验通过增加心脏负荷判断心肌的收缩储备功能,进而判断心肌存活,是判断存活心肌较为常用的方法[10,12-13],但多为半定量分析,且对AMI患者存在一定风险。MCE能评价心肌微循环情况,成本低、安全性高,是识别存活心肌较为理想的方法。应用计算机软件定量综合评估CI和WT,可反映心肌微循环灌注情况和局部收缩功能。本研究I/R模型大鼠危险中央区微循环灌注和局部收缩功能直至术后28天仍有明显降低,且均无法恢复,故判定该区域为梗死区域,且其面积与Masson染色测得梗死面积呈正相关,提示其所识别的危险中央区面积可代表梗死心肌范围。另外,术后随时间逐渐延长,危险周边区面积不断减小,由于周边区界定标准是微循环灌注恢复而局部收缩功能仍然减低,故此区域为“顿抑心肌”[12],即本系统通过识别危险周边区而实现了对顿抑心肌的判断,而危险恢复区作为解除冠状动脉阻断后迅速恢复微循环灌注和收缩功能的区域,可直接判断为存活心肌区域。当然危险恢复区与正常心肌在细胞水平有所区别,如存在心肌细胞凋亡等;而正常心肌区域原本微灌注和室壁收缩运动均属正常,判断标准也是WT>0.3且CI>-54Pix,但超声难以区别。
综上所述,新型MCE-NSS系统可实现评估大鼠心肌I/R后左心室局部收缩功能及微循环情况,并能识别存活心肌。
