肿瘤相关成纤维细胞在肿瘤免疫抑制中的作用及其应用研究进展
2020-04-29梁陆鑫侯宗柳邱婉芳王文举杨芳
梁陆鑫,侯宗柳,邱婉芳,王文举,杨芳
昆明医科大学,昆明650500
尽管以肿瘤细胞为主要靶点的治疗模式显著改善了恶性肿瘤患者的预后,但肿瘤复发、致死性转移和顽固性肿瘤微环境(TME)仍是尚未完全解决的三个重要问题[1,2]。肿瘤“种子与土壤”学说是肿瘤生物学最富有影响力的理论之一,该理论认为肿瘤的发生发展不仅是肿瘤细胞自身遗传学和表观遗传学的改变,还有TME作为恶性肿瘤生长的“肥沃土壤”,它们彼此相互影响,共同促进肿瘤的发生与发展[3,4]。近年来,靶向表面标志物治疗使得患者的抗肿瘤免疫功能在一定程度上有所增强,但长期的临床疗效欠佳。目前,研究者认为TME中存在导致机体免疫应答低下或不应答的因素,故肿瘤处于免疫抑制状态[5]。肿瘤相关成纤维细胞(CAFs)是TME的优势细胞,可作为免疫抑制TME的生物标志物[6],其具有活化特性,表型和功能也表现为多样性。CAFs确切的起源仍没有完全阐明,关于CAFs的功能报道结论也不一致,推测可能是由于CAFs的高度异质性所致。因此,CAFs在TME靶向治疗中受到特别的关注。现就CAFs在肿瘤免疫抑制中的作用及以CAFs靶点靶向治疗的临床应用研究进展进行综述。
1 CAFs在肿瘤免疫抑制中的作用
1.1 CAFs在肿瘤免疫调控中发挥作用 CAFs是TME中的重要组成部分,是一群存在于几乎所有实体瘤中的成纤维细胞,在某些肿瘤间质组织中的比例高达90%[7,8]。CAFs不同于正常的成纤维细胞,它在TME中具有活化的特性,并表达特定的标志物如成纤维细胞激活蛋白(FAP)、波形蛋白、α-平滑肌肌动蛋白(α-SMA)、成纤维细胞特异性蛋白、血小板源生长因子受体、富含半胱氨酸的分泌型酸性蛋白、结蛋白、硫酸软骨素蛋白多糖等,这些标志物在不同细胞中的表达存在差异,说明CAFs具有表型异质性[9]。CAFs是一组不同的细胞亚群,在TME中对不同刺激做出反应,表现出独特的分泌表型,并具有特定的生物学功能。
有学者[10]首次在体内实验中证实,前列腺癌上皮细胞单独或与正常成纤维细胞共培养时均不具有致瘤性,但当与CAFs共培养时则能形成巨大的实体瘤,揭示了在CAFs的参与下TME对肿瘤发生发展的促进作用。研究者[11]发现,CAFs通过上调血小板衍生生长因子的表达,抵消抗VEGF疗法对血管形成的抑制作用,介导肿瘤细胞对抗VEGF治疗的耐受性。有学者[12,13]发现,靶向清除转基因小鼠原位移植瘤的FAP+CAFs可以反过来增强小鼠抗肿瘤免疫效应[4]。整个实体瘤组织中,CAFs多位于组织的边缘或浸润在肿瘤组织中,在肿瘤免疫调控方面具有重要作用(见图1)。如CAFs产生的TGF-β和VEGF可以抑制树突状细胞(DC)成熟,促进调节性DC形成,同时能够促进CD4+T细胞向调节性T细胞的分化;CAFs分泌的IL-6促进单核前体细胞向髓源性抑制细胞的分化;CAFs分泌基质细胞衍生因子1(SDF-1)能够促进血管生成,促进免疫细胞在TME中的浸润;CAFs也可以通过分泌大量的胞外基质抑制免疫细胞的活性[11,14]。
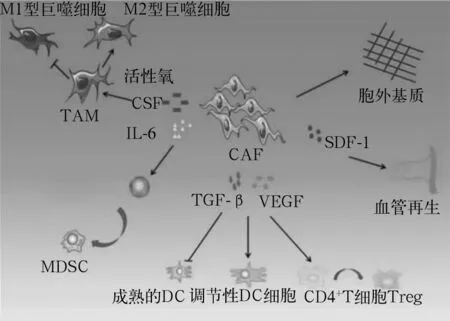
图1 CAFs对TME中免疫细胞的调控作用
1.2 CAFs通过转化生长因子β(TGF-β)介导免疫抑制的发生 正常的成纤维细胞处于静止状态,当它们受到生长因子、细胞因子和氧化应激的刺激后,分化成CAFs[15]。TGF-β能够提供CAFs与TME之间进行交流作用,CAFs又可释放胶原蛋白和纤连蛋白等细胞外基质成分,激活TGF-β。CAFs介导免疫抑制是通过TGF-β的刺激作用于TME中的大部分细胞,包括抑制抗肿瘤细胞增殖作用和增加肿瘤细胞的活性两方面[16]。CAFs自身也具有免疫抑制特性,通过COX-2依赖机制上调细胞内的组蛋白去乙酰化酶表达而产生作用。转移性膀胱癌相关研究进一步揭示,CAFs在有TGF-β作用的情况下通过阻断CD8+T细胞的获得从而减弱抗肿瘤免疫[17]。活化的胰腺星状细胞(相当于胰腺当中的CAFs)分泌SDF1等趋化因子募集和隔离CD8+T细胞,从而阻断其接近肿瘤细胞[18]。当更多的CD8+T细胞被募集到肿瘤基质中,消除FAP+CAFs会重新激活抗肿瘤免疫反应。具有靶向性的α-SMA+CAFs的肿瘤侵袭性更强,可增加调节性T细胞的浸润,进而达到抑制免疫监视的作用。
一般来说,大多数CAFs亚群通过影响抗肿瘤免疫细胞的活性和生存来介导TME的免疫抑制[1]。CAFs通过与TME内的其他细胞相互作用,促进肿瘤发生发展。CAFs的数量与侵袭性呈正相关,且随着肿瘤分期的增高,CAFs对靶向治疗的反应被阻滞。CAFs在肿瘤发生发展过程中发挥的功能使其成为肿瘤治疗的理想靶点。
2 CAFs在肿瘤治疗中的应用
2.1 靶向FAP的临床应用 随着对CAFs病理基础分子机制的不断研究,许多靶向关键调控因子的药物正在进行临床和(或)临床前评估。FAP是CAFs特异性的标志物,目前抗CAFs治疗主要集中于FAP方向[19]。在转基因小鼠中使用FAP启动子驱动的白喉毒素受体来消耗FAP阳性基质细胞已被证实会减缓胰腺导管腺癌的增长。FAP5-DM1是一种新型抗FAP单克隆抗体偶联美登木素生物碱,对肿瘤生长有长期的抑制作用,甚至可使肿瘤完全消失,在富含基质细胞的肺癌、胰腺癌和头颈癌的异种移植瘤模型中未见明显的毒性作用。有研究表明,在小鼠肺癌模型中清除表达FAP的CAFs可使肿瘤细胞和基质细胞在肿瘤免疫过程中快速缺氧坏死,这个过程涉及IFN-γ和TNF-α,已被证明参与了CD8+T细胞依赖性杀伤过程[12]。目前可采用Sibrotuzumab单克隆抗体进行靶向治疗[20,21],针对结直肠癌的治疗正在进行临床试验。嵌合抗原受体CAR-T细胞靶向FAP方案被证实在小鼠模型[22]和恶性胸膜间皮瘤患者来源的异种移植模型[23]中具有良好的效果。鉴于CAFs的基因表达比肿瘤细胞更稳定,针对CAFs携带的FAP抗原进行免疫接种可能是靶向FAP免疫治疗的最佳策略。
2.2 靶向特定蛋白/分泌因子的临床应用 基于特定蛋白质(如FAP)和参与CAFs激活的信号通路分子(如TGF-β、PDGF、FGF)或CAFs特定分泌因子的靶向治疗正在研究中[24]。目前有研究表明,在胰腺癌中,靶向FAP治疗与靶向CXCL12和AMD3100联合应用,可与抗PD-L1产生协同作用[25]。CAFs在表型和功能上的固有异质性可能源于其多样的细胞来源,CD10和GPR77作为特异性CAFs表面标志物,将有助于不同CAFs亚群的分类,并有助于制定针对致瘤CAFs亚群的精准靶向策略[26]。CAFs分泌的其他特定蛋白(如TGF-β、IL-6等)也可作为靶点以提高效应细胞的免疫功能[24]。在活性类赖氨酸氧化酶2存在的情况下,3-羟苯基化合物被确定为TGF-β1的有效阻断剂,能强力阻滞体内病理性胶原蛋白的积累而提高效应T细胞的杀伤能力[27]。在靶向CAFs特定蛋白/分泌因子的治疗中,重要细胞因子或调节因子作为联合靶点的应用可能更广泛。
2.3 其他CAFs靶向基因抑制剂的临床应用 CAFs相关治疗靶点已进入临床试验阶段,如JAK2被认为是CAFs的潜在靶点,参与STAT3的激活;JAK2抑制剂如SAR302503[28]和帕克替尼[29]被用于CAFs的失活和消耗基质,导致胶原蛋白结构减少。SHH基因是圆滑蛋白基因(SMO)激活的配体,在CAFs中过表达,活化的STAT3也能上调其表达。在临床试验中,一些SMO抑制剂(伊曲康唑和vismodegib)可抑制肿瘤的生长。因此,SHH抑制剂被认为是一种很好的抑制CAFs的治疗策略[30]。此外,有几种VEGF抑制剂正在进行临床试验研究,它们会消耗CAFs来源之一的内皮细胞,从而减少CAFs的数量[31]。在TME中,CAFs的存活影响着免疫抑制的发生,奠定了靶向基因抑制剂临床开发及应用的基础。
总的来说,上述抗CAFs治疗方案的设计都是以CAFs促肿瘤发展为前提。CAFs在表型和功能上的内在异质性可能源于其细胞来源的多样性,因此,在设计以CAFs为靶点的肿瘤免疫方案时需要多方面考虑。CAFs靶向治疗正在迅速探索和发展,随着单细胞测序和新型生物材料细胞的出现,选择性消除CAFs亚群或减弱其促肿瘤作用,可能成为一种有效的治疗方式。
综上所述,靶向CAFs的治疗方案受到特别关注,但仍面临一些障碍和挑战,主要包括:①CAFs的来源不确定;②靶向CAFs具有异质性,表现为表型、分泌谱和亚群功能不同,给诊断和靶向治疗带来困难[26];③CAFs诱导信号具有功能多样性,一种CAFs可以激活发挥致瘤和反致瘤作用的信号[32];④CAFs的功能因肿瘤类型而异[33];⑤细胞特异性标志物的识别和追踪限制将阻碍靶向CAFs方案的有效治疗。另外,靶向某些CAFs亚群还可能会在TME中引发难以预测且因人而异的基质反应。深入的基因组测序可分析CAFs分子结构,加快了CAFs特异性诊断、预后评估及CAFs靶向治疗的发展速度[34]。因此,还需要对CAFs的不同亚型进行更深入的研究,确定肿瘤进展中具有优势的亚型,重点研究其靶向治疗方案[35]。
