加速康复外科在3D腹腔镜辅助胃癌根治术中的应用研究
2020-04-22杨吉荣张珂诚崔建新卢灿荣
杨吉荣,张珂诚,崔建新,卢灿荣,卫 勃,唐 云,陈 凛
(1.濮阳市安阳地区医院普外一科,河南 濮阳,455000;2.解放军总医院普通外科)
手术应激是患者术后发生并发症的高危因素[1]。加速康复外科(enhanced recovery after surgery,ERAS)整合一系列具有循证医学依据的围术期管理策略,以减少患者手术应激,优化生理状态,促进快速康复[1-3]。不同手术的ERAS路径有所差异[4-5],其临床实施也需要外科医师与麻醉医师等多学科协作。笔者单位较早在胃癌手术中应用ERAS,并参与制定ERAS路径指南,成立加速康复外科学院以促进ERAS临床应用的实施[3,5-6]。随着技术的发展及设备的研发,微创外科逐渐成为胃手术中重要的手术方式。近年,笔者中心三维(three dimension,3D)腹腔镜辅助胃癌手术的应用与日俱增。本文总结我中心ERAS应用经验,探究ERAS路径在3D腹腔镜胃癌根治术中应用的可行性。
1 资料与方法
1.1 临床资料 纳入2018年1月至6月同一手术组采用ERAS路径行3D腹腔镜辅助胃癌根治术的患者。收集患者临床病理资料,包括性别、年龄、合并症、营养风险评分、手术时间、术中出血量及术后病理分期等。术后并发症根据Clavien-Dindo分级[7],记录术后30 d内死亡率。以下8项措施用来计算ERAS路径的依从性:术后无胃管放置,术后1~2 d拔除尿管,无腹腔置管引流,术后第1天下床活动,术后第1天进食清流营养液,术后3~5 d进食流食,术后镇痛并防止恶心呕吐。
1.2 ERAS路径 ERAS路径施行患者围术期管理[5]。住院前,患者在门诊接受术前宣教与咨询,进行腹部CT、胸片、胃镜、心电图、血常规及肺功能等检查,以明确诊断与术前评估。鼓励患者至少戒烟2周。虚弱患者行预康复训练,以改善生理、代谢、营养及精神状态,增加功能储备。住院当天,再次以书面形式进行宣教。告知患者可能的住院时间、术前禁食时间、手术方式、疼痛控制及引流管拔除等内容。采用营养风险筛查2002表评估患者营养状态。术前不进行常规机械性肠道准备,术前禁食6 h。采用丙泊酚、短效阿片类药物进行麻醉诱导,使用短效非去极化肌松药,以利气管插管与通气,短效麻醉药以维持麻醉,短效肌松药以利术野暴露。终末潮气(0.7~1.3)或脑电双频指数(40~60)监测麻醉深度,对于老年患者避免麻醉过深(脑电双频指数小于45)。麻醉后插入胃管、尿管。切皮前1 h应用抗生素,手术时间超过3 h追加剂量。调节手术室温度在25℃~28℃。视情况使用加热装置维持患者体温。术中采取目标导向液体治疗与保护性通气措施。切口局部注射0.5%布比卡因以缓解术后疼痛,并使用患者自控疼痛装置。应用昂丹司琼,以减少术后恶心呕吐。手术完成时拔除鼻胃管,不常规放置引流管。术后第1天,鼓励患者下床活动,口服水及清流营养液,并拔除尿管。术后3~5 d,如果患者耐受,则进食流食。术后5~7 d,如耐受可进混合软食。检验指标正常、无不适症状后鼓励出院。
1.3 手术方法 根据术前检查、术中探查结果,患者行3D腹腔镜辅助全胃或部分胃切除术[8-10]。主要操作步骤:5孔法建立气腹(图1),压力维持在12~15 mmHg。探查腹腔,悬吊肝脏左外叶(图2)。超声刀打开胃结肠系膜,向脾区游离,清扫4组淋巴结,离断胃网膜左血管(图3)。向肝曲游离,分离胃结肠融合筋膜间隙,清扫幽门下6组淋巴结,离断胃网膜右血管(图4)。清扫5组及12组淋巴结,裸化十二指肠,腔镜下直线切割闭合器离断十二指肠(图5)。清扫7、8、9、11组及小弯侧1、3组淋巴结,并离断胃右血管(图6)及胃左血管(图7)。腔镜下切割闭合器离断远端胃组织(图8),上腹部小切口行消化道重建(图9)。根据术中所见行胃十二指肠、胃空肠、Roux-en-Y或食管胃吻合。
1.4 统计学处理 采用SPSS软件进行数据分析。连续性变量以均数±标准差或中位数和四分位间距(interquartile range,IQR)表示。连续性变量采用Mann-Whitney检验或独立样本t检验比较,分类变量用卡方检验。单因素与多因素回归分析探究延迟出院(术后住院时间超过7 d)的影响因素。Pearson相关分析ERAS依从性与术后住院时间的关系。双侧P<0.05为差异有统计学意义。
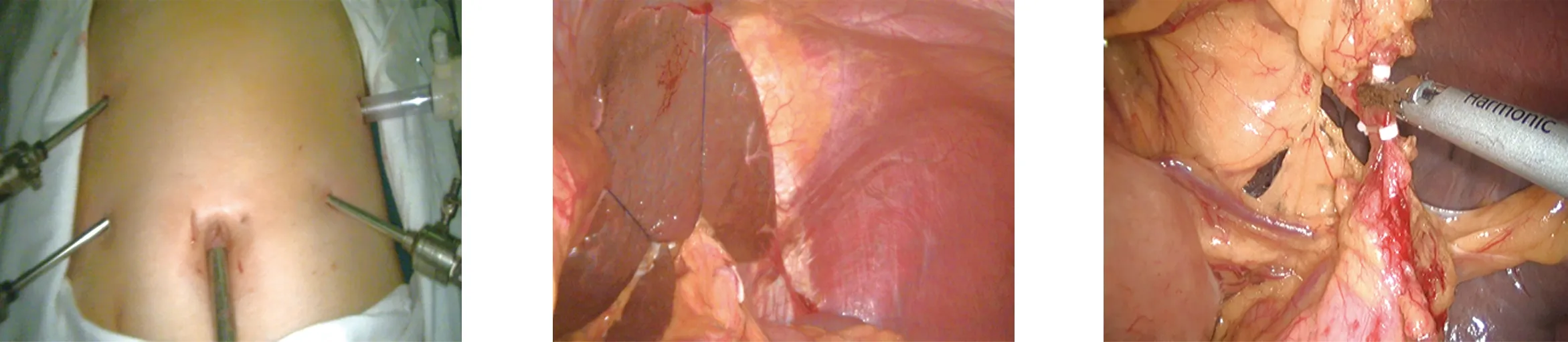
图1 穿刺孔位置 图2 肝脏左外叶悬吊 图3 离断胃网膜左血管

图4 离断胃网膜右血管 图5 离断十二指肠 图6 离断胃右血管
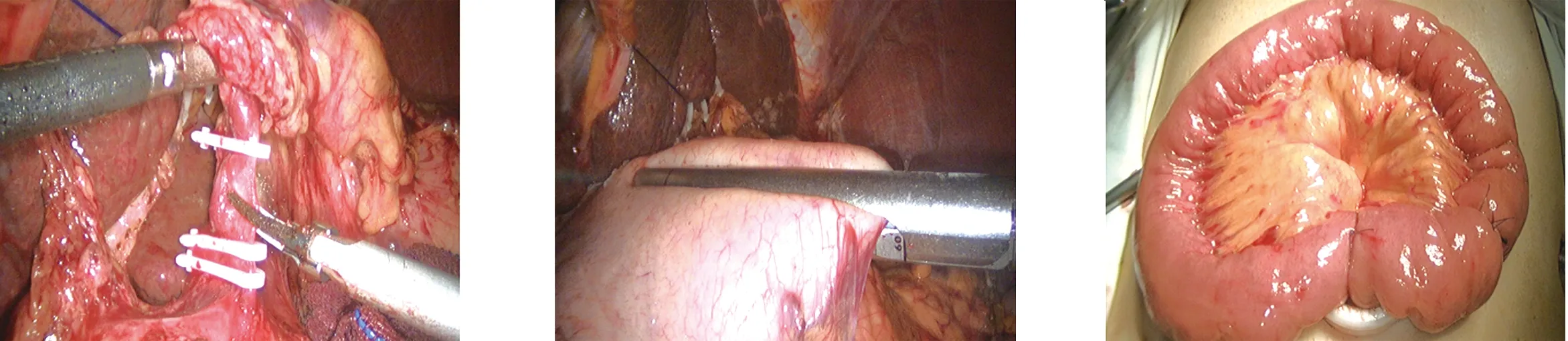
图7 离断胃左血管 图8 离断远端胃组织 图9 辅助小切口消化道重建
2 结 果
2.1 基线资料 84例采用ERAS路径行3D腹腔镜辅助胃癌根治术,纳入最后分析,患者63.5岁(IQR:53.0-66.0),体质指数24.0 kg/m2(IQR:21.0-26.0)。男68例,女16例。A型血23例,AB型血10例,B型血23例,O型血28例。营养风险筛查2002表筛查营养风险评分为:49例0分,20例1分,6例2分,5例3分,4例4分。17例患者合并1种合并症,3例合并2种,1例合并3种。合并症类型依次为:糖尿病(6例),肝胆疾病(6例),心脏疾病(5例),贫血(3例),高血压(3例),反流性食管炎(1例),胰腺囊肿(1例),十二指肠息肉(1例)。
2.2 围术期结果 ASA评分Ⅰ级、Ⅱ级、Ⅲ级分别为1例、73例、10例。中位手术时间230 min(IQR:200-250),中位出血量为100 mL(IQR:100-100)。38例患者行全胃切除术,42例行部分胃切除术(包括36例远端胃切除术、6例近端胃切除术)。此外,4例患者行联合脏器切除术(2例行远端胃切除联合胆囊切除术,1例行远端胃切除联合部分肝脏切除术,1例行远端胃切除联合横结肠切除术)。4例中转开腹,其中2例因联合脏器切除,2例因严重腹腔粘连。83例(98.8%)行D2根治术。3例需术中输血。83例行D2手术,1例行D1+术。重建方式为Billroth Ⅰ式16例,Billroth Ⅱ式5例,Roux-en-Y式57例,食管胃吻合6例。
肿瘤大小3.5 cm(IQR:2.5-4.9)。肿瘤分化程度为:高-中分化1例,中分化13例,中-低分化35例,低分化33例,印戒细胞2例。病理学分期Ⅰ、Ⅱ、Ⅲ期分别为31例、19例、34例。中位淋巴结清扫数量为30.5枚(IQR:24-41.7)。8例患者发生了术后并发症,包括4例贫血需要输血治疗(Ⅱ级),1例腹腔积液需要引流(Ⅲ级),1例吻合口漏需要再次手术(Ⅲ级),2例转入ICU治疗(Ⅳ级)。无术后病死率。中位术后住院时间7 d(IQR:5-8),中位住院费用为79 434元(IQR:69 705-91 305)。
2.3 ERAS依从性 中位总体依从率为0.69(IQR:0.50-0.88)。术后镇痛与防止恶心呕吐依从性均为100%,82.1%的患者于术后1~2 d拔除尿管,64.3%无术后胃管,56%无术后引流,56%术后3~5 d进流食,45.1%于术后第1天进食清流营养液,术后第1天下床依从性仅为34.5%。单因素分析表明,手术时间(OR:1.02,P<0.001)、出血量(OR:1.01,P<0.011)与延迟出院正相关,而ERAS依从性与延迟出院负相关(OR:0.04,P<0.001)。见表1。多因素分析结果表明,仅ERAS依从性与延迟出院显著负相关(OR:0.65,P=0.001)。见表2。相关性分析表明,术后住院时间与ERAS依从性显著负相关(Spearmanr=-0.7,P<0.001,图10)。以中位总体依从性0.69为界值,84例患者分为ERAS高依从性与ERAS低依从性两组。ERAS高依从性组住院费用更低[76 365元(IQR:67 259-84 705) vs. 86 967元(67 259-103 654),P=0.031]。
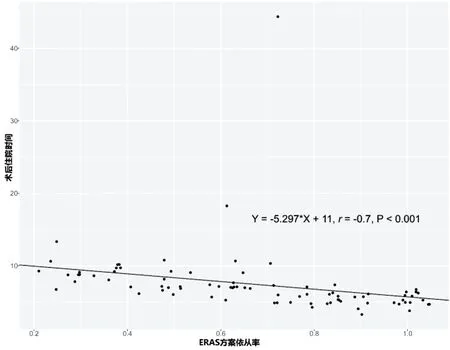
图10 术后住院时间与ERAS方案依从率相关性
3 讨 论
ERAS理念于2007年引入中国[11]。笔者中心率先研究了ERAS在胃切除术及老年胃癌患者中的应用价值,并证实了其促进患者康复的优势[3,6]。目前尚无文献报道ERAS联合3D腹腔镜手术用于胃癌患者围术期管理的安全性、有效性。本研究结果表明,ERAS可安全地应用于3D腹腔镜胃手术中。
表1 延迟性出院的单因素分析结果
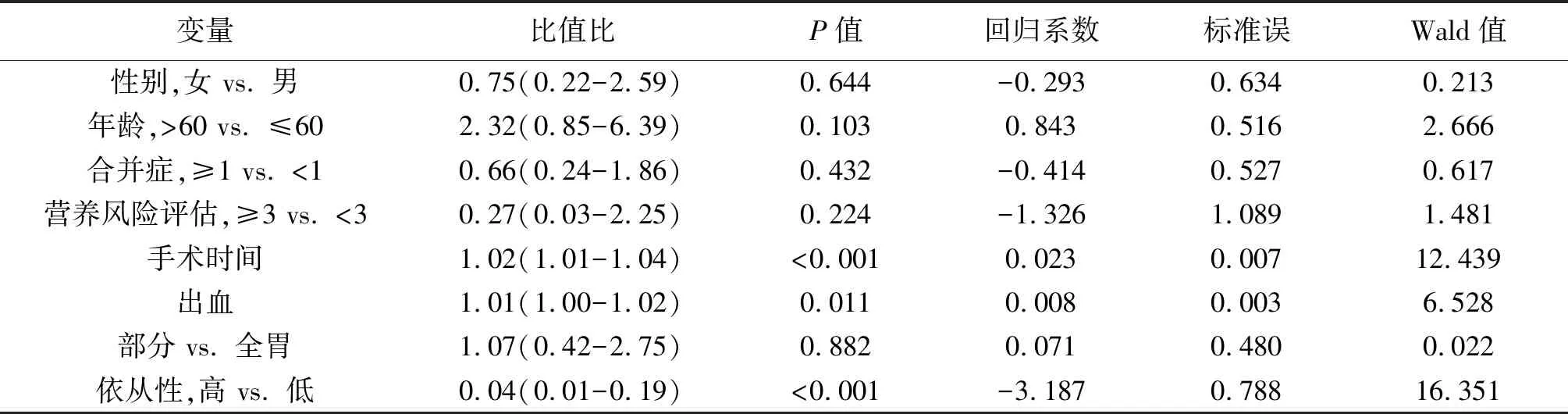
变量比值比P值回归系数标准误Wald值性别,女 vs. 男0.75(0.22-2.59)0.644-0.2930.6340.213年龄,>60 vs. ≤602.32(0.85-6.39)0.1030.8430.5162.666合并症,≥1 vs. <10.66(0.24-1.86)0.432-0.4140.5270.617营养风险评估,≥3 vs. <30.27(0.03-2.25)0.224-1.3261.0891.481手术时间1.02(1.01-1.04)<0.0010.0230.00712.439出血1.01(1.00-1.02)0.0110.0080.0036.528部分 vs. 全胃1.07(0.42-2.75)0.8820.0710.4800.022依从性,高 vs. 低0.04(0.01-0.19)<0.001-3.1870.78816.351
表2 延迟性出院的多因素分析结果
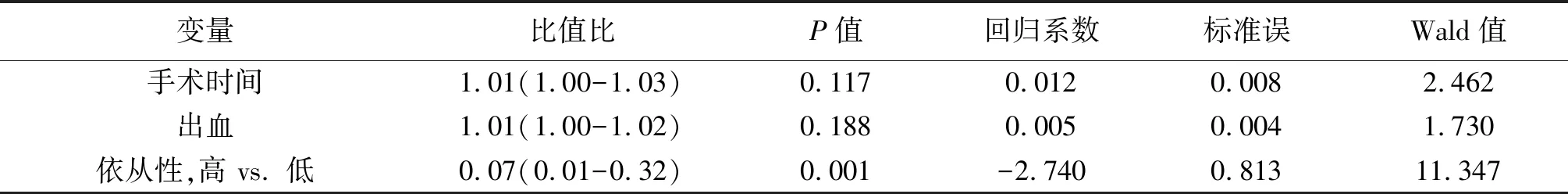
变量比值比P值回归系数标准误Wald值手术时间1.01(1.00-1.03)0.1170.0120.0082.462出血1.01(1.00-1.02)0.1880.0050.0041.730依从性,高 vs. 低0.07(0.01-0.32)0.001-2.7400.81311.347
既往研究中,多数ERAS方案仅聚焦于外科相关措施,如无腹腔引流、早期拔除尿管、早期运动等。但ERAS强调整合多学科力量共同促进患者康复,因此有必要重视麻醉相关措施,如多模式镇痛方案、保护性通气策略等。与既往文献报道不一样的是,本研究中ERAS策略整合了外科与麻醉相关措施,以提供患者最优围术期康复路径。本研究中,我们采用脑电双频指数指导的麻醉策略,维持麻醉于合适深度,同时避免麻醉药物过量使用,以促进患者术后快速康复、苏醒。术中我们应用保护性通气策略,以利减少肺部并发症、缩短住院时间[12]。目标导向的液体治疗来维持内环境稳定、防止液体负荷过多。术后疼痛影响患者康复,因此我们采用多模式镇痛方案,包括罗哌卡因、氟比洛芬酯,以促进患者早期下床与进食。
提高ERAS的依从执行率是确保疗效的关键。本研究证实高依从性患者住院时间更短,医疗费用更低,术后康复更快。一项国际登记研究结果表明,ERAS依从性与住院时间及并发症显著负相关[13]。为提高ERAS依从执行率,有必要分析ERAS执行过程中的有利与不利因素。McLeod采用“理论至实践”循环方法,建立了适合医院执行的ERAS方案,而Pearsall采用半结构化访问量表以发现执行ERAS过程中有利与不利因素[14-15]。根据我们的经验,有三方面因素影响了ERAS方案的实施:行政相关,医务人员相关及患者相关。为克服行政方面的不利因素,整合多学科团队合作力量,笔者中心建立了胃肠外科ERAS学院,整合外科医师、麻醉医师、护理人员及营养医师的力量。笔者中心同时建立ERAS绿色通道,以确保患者住院的行政支持。医务人员相关不利因素在于不愿改变其沿袭传承的诊疗常规,而ERAS继续教育活动利于解决此问题。患者不合理期望同样是ERAS执行的不利因素,我们通过视频展示、书面教育与口头告知进行患者宣教,以建立患者合理期望,取得患者配合。
通过建立ERAS方案及提高ERAS执行依从性,本研究中3D腹腔镜胃切除术患者的术后中位住院时间为7 d,术后并发症发生率为9.5%。既往胃手术相关ERAS研究中,Liu等[16]报道行2D腹腔镜胃手术患者术后中位住院时间、术后并发症分别为6 d与8.1%;日本学者报道[17],术后中位住院时间、并发症发生率分别为8 d与10.7%;意大利学者报道分别为8 d与11.1%[18]。据此,本研究结果与既往研究一致。与已有研究不一样的是,本研究整合3D腹腔镜手术于ERAS路径中。与2D传统腹腔镜手术相比,3D腹腔镜可提升术者专业熟练度,3D视野有助于术者在镜下较难的操作,如腹腔干附近淋巴结的清扫等[19-20]。与已有3D腹腔镜胃手术文献报道数据相比[21],患者肿瘤学安全性指标相当,但本研究中患者术后住院时间更短,并发症更少,证实了患者可从ERAS方案中获益。
本研究具有以下潜在局限性。首先,本研究为单臂队列研究,我们正进行前瞻性队列研究以进一步证实本研究结果。其次,需对患者进行随访,以获得长期疗效的数据。再者,ERAS方案对于基础条件较差、高营养风险患者是否安全适用,仍需数据支持。
总之,本研究结果表明,ERAS路径可促进3D腹腔镜胃癌患者的快速康复。提高ERAS方案依从执行率可缩短住院时间、降低医疗费用。
