前列地尔联合马来酸桂哌齐特对2型糖尿病并发周围神经病变患者的临床疗效及对神经传导速度、氧化应激指标、胱抑素C水平的影响
2020-04-16山永仪李舜君李冬萍邹冬梅田立曹宏杨叔禹
山永仪 李舜君 李冬萍 邹冬梅 田立 曹宏 杨叔禹
(1西宁市第一人民医院内分泌科,青海 西宁 810000;2南通大学第三附属医院内分泌科;3厦门大学附属第一医院内分泌科)
糖尿病周围神经病变(DPN)是2型糖尿病患者常见慢性并发症之一,主要以肢体麻木、疼痛等感觉和运动障碍为主要症状,常引起患者焦虑、抑郁、失眠等;当病情持续进展时,可引起下肢坏疽,严重者可能截肢,严重影响患者的身心健康〔1〕。目前临床对于DPN的发病机制尚不十分明确,主要考虑与局部血流微循环障碍、氧自由基损伤、血脂代谢异常等因素有关〔2〕。临床治疗DPN较棘手,主要以控制血糖,营养神经等对症支持治疗。马来酸桂哌齐特是治疗DPN的常用药物,有效改善神经功能。前列地尔是一种血管活性药物,具有改善微循环,营养神经等〔3,4〕。目前临床较少对糖尿病患者神经传导速度、血流动力学指标、视觉模拟评分(VAS)等相关评分、氧化应激指标、胱抑素(Cys)C水平影响进行研究。本研究对DPN患者采用前列地尔联合马来酸桂哌齐特治疗,对其临床疗效、传导速度、血流动力学指标、VAS等相关评分、氧化应激指标、CysC水平进行全面研究,取得较好疗效。
1 资料与方法
1.1一般资料 2016年4月至2019年4月于西宁市第一人民医院内分泌科住院的2型糖尿病并发周围神经病变患者130例。纳入标准:①符合2017年版中国2型糖尿病防治指南〔5〕;②符合《实用糖尿病学》中关于DPN的诊断依据〔6〕。排除标准:①排除其他神经病变及其他对神经传导产生影响的疾病;②严重的心脑血管和肝肾等疾病;③对所用药物或其成分过敏者;④拒绝参与本研究的患者。随机分为对照组和病例组各65例;对照组男39例,女26例;年龄(66.28±12.34)岁;糖尿病病程(11.73±3.67)年;DPN病程(1.46±0.42)年。病例组男34例,女31例;年龄(68.51±13.72)岁;糖尿病病程(12.35±3.84)年;DPN病程(1.58±0.47)年。两组基数资料差异无统计学意义(P>0.05)。本研究经过医院伦理委员会批准,患者均签订知情同意书。
1.2治疗方法 患者均给予控制饮食、运动、控制血糖等对症支持治疗;对照组给予马来酸桂哌齐特(北京四环制药有限公司,国药准字号:H20020125,2 ml/支)8 ml+0.9%NaCl 500 ml,静脉滴注,1次/d。病例组在对照组基础上给予注射用前列地尔干乳剂(优帝尔,重庆药友制药有限责任公司生产,国药准字号:H20100047,5 μg)10 μg+0.9%NaCl 100 ml,静脉滴注,1次/d。治疗时间为2 w。
1.3观察指标
1.3.1运动和感觉神经传导速度 测定运动和感觉神经(腓总神经、尺神经、胫神经、正中神经)传导速度。
1.3.2血流动力学指标 全血黏度、血浆黏度、血细胞比容、血流流速。
1.3.3氧化应激和胱抑素C水平 检测超氧化物歧化酶(SOD)水平、丙二醛(MDA)水平、总抗氧化能力(TAOC)和CysC水平。
1.3.4视觉模拟法评分(VAS)、多伦多临床评分系统(TCSS)评分、匹茨堡睡眠质量指数量表(PSQI)评分 1)VAS评分:疼痛强度的变化采用VAS。0分表示没有痛,10分表示剧烈疼痛。2)TCSS评分:临床神经病变评分表采用TCSS进行评分,分数越高,神经病变越严重。3)PSQI评分:睡眠质量的变化采用PSQI评分。0分表示睡眠良好,21分表示存在严重睡眠障碍。
1.4临床疗效〔7〕依据临床症状和神经传导速度等进行评判;(1)显效:症状消失,神经传导速度增加>5 m/s;(2)有效:症状明显改善,神经传导速度增加2~5 m/s;(3)无效:症状无改善,神经传导速度无明显变化。总有效率=(显效+有效)/总数×100%。
1.5统计学方法 采用SPSS19.0软件进行t、χ2检验。
2 结 果
2.1两组临床疗效比较 病例组总有效率显著高于对照组(P<0.05),见表1。
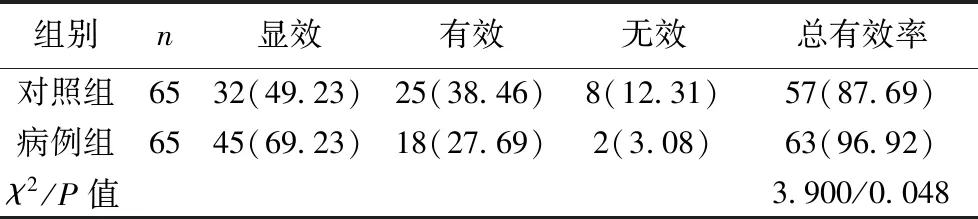
表1 两组临床疗效比较〔n(%),n=65〕
2.2两组运动和感觉神经传导速度比较 治疗前,两组运动、感觉神经(腓总神经、尺神经、胫神经、正中神经)传导速度比较,差异无统计学意义(P>0.05);治疗后,两组运动、感觉神经(腓总神经、尺神经、胫神经、正中神经)传导速度显著高于治疗前,且病例组运动和感觉神经传导速度显著高于对照组(P<0.05),见表2。
2.3两组血流动力学指标比较 治疗前,两组全血黏度、血浆黏度、血细胞比容、血流流速比较,差异无统计学意义(P>0.05);治疗后,两组全血黏度、血浆黏度、血细胞比容显著低于治疗前,血流流速显著高于治疗前,且病例组血流动力学指标改善情况显著优于对照组(P<0.05),见表3。
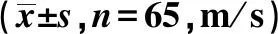
表2 两组运动、感觉神经传导速度比较
与治疗前比较:1)P<0.05;与对照组比较:2)P<0.05,下表同

表3 两组动脉血流动力学指标比较
2.4两组氧化应激和CysC水平比较 治疗前,两组SOD、MDA、TAOC、CysC水平比较,差异无统计学意义(P>0.05);治疗后,两组SOD、TAOC水平明显高于治疗前,MDA、CysC水平明显低于治疗前;且病例组氧化应激和CysC水平改善情况显著优于对照组(P<0.05),见表4。

表4 两组氧化应激和CysC水平比较
2.5两组VAS、TCSS评分、PSQI评分比较 治疗前,两组VAS、TCSS评分、PSQI评分比较,差异无统计学意义(P>0.05);治疗后,两组VAS、TCSS评分、PSQI评分明显低于治疗前;且病例组VAS、TCSS评分、PSQI评分显著低于对照组(P<0.05),见表5。
2.6两组不良反应比较 病例组不良反应发生率低于对照组,但差异无统计学意义(P>0.05),见表6。不良反应在停药后均自行缓解,未出现肝肾功能异常等其他严重不良反应。

表5 两组VAS、TCSS评分、PSQI评分比较分)
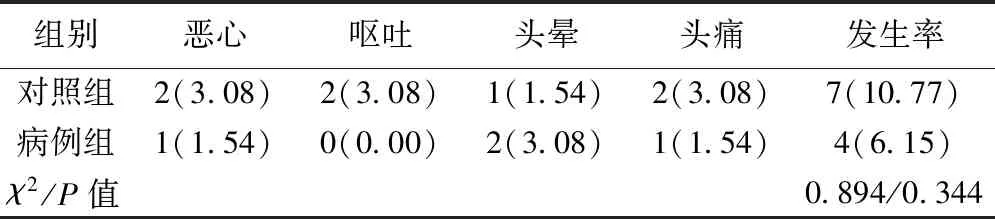
表6 两组不良反应比较〔n(%),n=65〕
3 讨 论
DPN的发生率占糖尿病患者的60%~90%,依据国际糖尿病联盟统计分析,在未来的20年内,全世界糖尿病患者人数将达到5.92亿,故DPN发生情况不容乐观〔8〕。在DPN病情进展中,高血糖诱发的微血管病变、神经营养因子合成分泌下降、神经营养代谢障碍具有重要作用〔9〕。
马来酸桂哌齐特是临床治疗DPN最常用的药物,是一种钙离子通道拮抗剂,通过离子交换阻止钙离子进入血管平滑肌,从而扩张血管,降低血管阻力,有效缓解血管痉挛〔10〕。此外,马来酸桂哌齐特还可以通过提高腺苷浓度,促进腺苷和环磷酸腺苷(cAMP)结合,阻碍多元醇通路的形成,使得山梨醇和果糖的堆积减少,提高细胞内Na+-K+-ATP酶的活性,降低氧耗〔11〕。再者,马来酸桂哌齐特可以提高红细胞的可塑性,增加细胞内一氧化氮(NO)含量,提高血管内血液流速,降低阻力,进而改善神经变性、水肿,提高神经传导速度来达到治疗DPN的功效〔12〕。研究显示,马来酸桂哌齐特可以改善DNP患者的临床症状〔13〕。
前列地尔可以抑制血小板凝集及免疫复合物合成,降低血栓素A2和血液黏稠,抑制氧自由基,可以明显改善血液的高凝状态和微循环〔14〕。一方面,前列地尔能够促纤溶和溶栓,活化脂蛋白酶,促进三酰甘油的分解,降低血液黏稠度,减少并阻止动脉粥样硬化斑块形成〔15〕。另一方面,前列地尔与血小板抗体结合后,可以激活腺苷酸环化酶,增加红细胞CAMP和神经细胞肌醇含量,改善肌醇代谢,增加血管内膜的血流,提高运动神经传导速度〔16〕。再者,可以分布于损伤的血管部位,靶向定位受损血管,扩张血管;能够抑制去甲肾上腺素的释放,促进血管平滑肌舒张,改善微循环,增加神经营养〔17〕。研究表明,前列地尔联合马来酸桂哌齐特可以显著提高周围神经传导速度,改善患者预后〔18〕。
研究表明,糖尿病患者在高血糖或者血糖波动较大状态下,容易发生氧化应激,导致细胞内线粒体脱氧核糖核酸(DNA)损伤,引起周围神经和血管内皮细胞功能下降〔19〕。TAOC、SOD和MDA是临床反映抗氧化应激能力常用的指标,与DPN患者病变严重程度呈正相关〔20〕。CysC是通过损伤神经组织、微血管来加快DPN病情进展,其水平升高是反映患者预后不良的独立危险因素〔21〕。
综上,前列地尔联合马来酸桂哌齐特对2型糖尿病并发周围神经病变患者临床疗效显著,可明显改善患者神经传导速度和血流动力学指标,调节氧化应激水平,安全性好。
