膈下肝癌经肝动脉化疗栓塞联合射频消融的临床疗效分析
2020-04-13刘家成刘一鸣宋松林郑传胜
石 钦,周 晨,刘家成,钱 坤,刘一鸣,宋松林,郑传胜,熊 斌
膈下肝癌因毗邻膈肌、肺、心脏等重要脏器,是局部治疗的难点之一。RFA作为原发性和继发性肝脏恶性肿瘤的局部有效治疗方法,具有微创、耗时短、费用低等特点,联合B超和CT影像引导可有效避免严重并发症的发生,提高靶向穿刺精准性[1]。尽管如此,治疗不完全和局部肿瘤进展仍然是其主要限制[2]。TACE是中晚期肝癌患者的首选治疗方案,不仅可促进肿瘤坏死而显著缩小病灶范围,而且可因碘油沉积而使肝癌在CT图像上显示更佳,从而提高RFA的疗效,弥补其不足[3-4]。本研究旨在评估经TACE联合RFA治疗膈下肝癌的安全性与有效性。
1 材料与方法
1.1 材料
2回顾性分析2014年3月至2018年11月在我科进行治疗的55例膈下肝癌患者61处病灶,患者基线特征如表1所示。
1.1.1 纳入标准 ①符合病理或临床诊断标准诊断为肝癌患者,无论是否接受过手术切除或介入治疗;② Child-Pugh分级A级或B级;③未合并门脉癌栓或肝外转移;④肾功能、心脏功能基本正常;⑤影像学诊断至少有1枚肿瘤结节靠近膈肌且距离≤5mm;⑥所有患者术前签署知情同意书。
1.1.2 排除标准 ①影像学上未发现靠近膈肌的肿瘤结节;②肝肾心功能差;③凝血功能异常无法纠正;④ECOG评分≥2;⑤合并其他严重疾病,无法配合治疗。
1.1.3 仪器设备 数字减影血管造影系统(DSA):采用德国SIEMENS AG公司生产的Artis zee ceiling型数字减影血管造影X线机。射频消融系统:采用美国Rita公司生产的射频消融系统,射频电极针规格为14 G Rita多极或16 G Rita单极。CT设备使用Siemens somaton sensation 16排螺旋CT。超声仪器采用Siemens Acuson X300超声。
1.2 方法
1.2.1 治疗经过 纳入的55例61处膈下肝癌患者均先进行TACE治疗,经过1~4周后行RFA治疗,在进行本次TACE联合RFA治疗期间未接受其他介入和手术治疗。所有患者术前查血生化、肝肾功能、凝血功能、肿瘤标志物、CT或MRI增强,并签署了知情同意书。
1.2.2 TACE治疗方法 消毒铺巾,局麻下采用Seldinger技术穿刺右侧股动脉,引入5 F Yashiro及微导管至腹腔干、肝左右动脉、肠系膜上动脉,注入造影剂行动脉造影,DSA摄影。明确病灶位置和大小后,经同轴微导管超选择置于膈下肝癌病灶主要供血动脉进行栓塞治疗,栓塞材料均选择碘化油和化疗药物(如表阿霉素)混悬液,联合适量粒径300~500μm或500~700μm明胶海绵进行栓塞。术毕造影显示肿瘤病灶栓塞效果满意。
1.2.3 RFA治疗方法 术前给予患者静脉滴注氟比洛芬酯或地佐辛,用1%利多卡因从皮肤至肝被膜进行充分局麻,经多普勒超声进行定位引导,确定穿刺部位,将14 G Rita多极或16 G Rita单极RFA针穿刺入膈下肝肿瘤病灶;达肿瘤部位后,经CT引导下调整消融针在肿瘤内的确切部位,以便纠正因超声单切面引导而造成的偏移,同时设定消融范围和消融时间,开始进行消融治疗;在CT引导下多次调整消融部位以覆盖肿瘤并进行安全范围内的整体消融。术毕复查CT增强或超声造影见消融效果满意,拔针行针道消融,包扎伤口。术中患者出现的疼痛,通过加入适量利多卡因与0.9%NaCl溶液1:1稀释液经进水孔对肿瘤病灶进行灌注,必要时给予吗啡肌内注射,以缓解患者疼痛。
1.2.4 术后处理及随访复查 术后观察3~7 d,进行水化、抗感染及护肝治疗。术后1个月内复查血生化及肝肾凝功能,并在1~3个月内复查肿瘤标志物以及CT或MRI增强,以后每3个月复查1次。疗效评价标准视CT或MRI增强来判断病变范围变化、是否出现新的肿瘤病灶以及原有病灶是否出现强化作为依据,并根据改良实体瘤疗效评价标准(mRECIST)来综合判断疗效[5]。
1.3 统计学方法
数据分析采用IBM SPSS Statistics 24统计软件,计量资料以均数±标准差(x±s)表示。治疗前后血生化及肝功能、AFP变化采用配对t检验;采用Kaplan-Meier生存曲线分析患者生存时间;P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效及并发症
55例肝癌患者共61处膈下病灶术后临床症状均得到缓解,肝区不适有所好转。其中术后17例出现腹痛腹胀不适,9例出现恶心呕吐反应,给予对症治疗后均消失。4例在1年后出现门脉癌栓,给予D-TACE联合门脉125I粒子植入治疗后有所好转,2例在1年后出现骨转移,1例在1年后出现腹腔多发转移,余未发现其他远处转移。
2.2 血液指标变化
比较发现,治疗后1个月内的肝功能及血生化指标与治疗前比较,差异无统计学意义(P>0.05),说明TACE联合RFA治疗策略对患者的肝功能并无影响,但治疗前后AFP明显下降,差异具有统计学意义(t=3.277, P<0.05)。见表2。

表2 患者治疗前后血生化及肝功能比较
2.3 术后肿瘤反应
55例肝癌患者61处膈下病灶在RFA术后2~3个月均经CT或MRI增强来评估病灶治疗情况,根据mRECIST评价标准进行评价,其中30处病灶(49.2%)完全缓解(CR),24处病灶(39.3%)部分缓解(PR),7处病灶(11.5%)疾病稳定(SD),无病灶疾病进展(PD)。客观反应率(ORR)为88.5%,疾病控制率(DCR)为100%,所有患者均获益。图1示膈下肝癌经TACE联合RFA治疗前后表现。
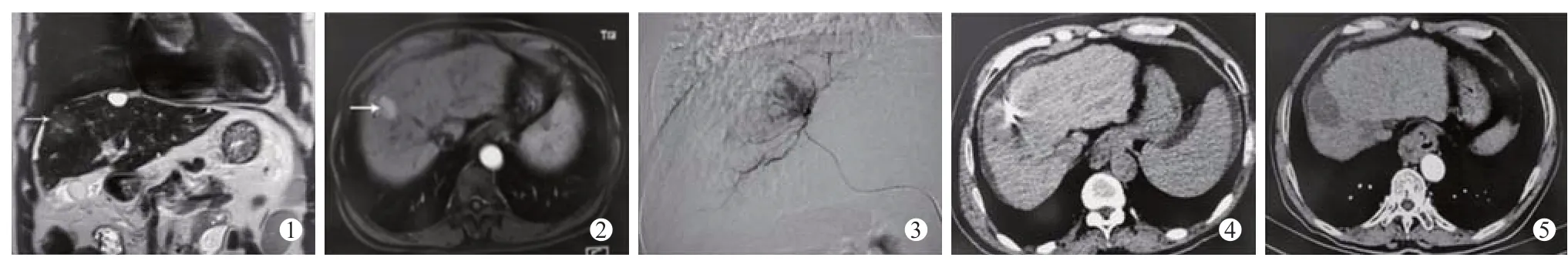
图1 膈下肝癌治疗前后表现
2.4 生存率
术后6个月随访中1例患者死于消化道出血,其余患者均存活,术后6个月死亡1例生存率为98.2%(54/55);术后1年随访中另有4例患者死亡,3例死于肿瘤进展,1例因腹腔多发转移死亡,术后1年生存率为90.9%(50/55);术后随访2年、3年患者生存率分别为80.0%(44/55)、72.7%(40/55),如图2所示。

图2 膈下肝癌患者生存曲线
3 讨论
已有多篇文献报道[6-8],TACE联合RFA治疗肝癌在控制肿瘤进展和改善患者生存方面优于单一的TACE或RFA治疗。膈下病灶≤5 cm肝癌的RFA有一定难度,因距离膈肌、心肺等重要脏器较近,且病灶小,定位穿刺较为困难,B超联合CT双导向射频消融可以克服这一难题,CT引导可以弥补B超因肺和肋骨引起的声窗限制,B超可以直接指引穿刺针的走向,从而显著提高穿刺精准性。本次研究中45处膈下病灶≤5 cm肝癌患者均采用B超和CT双导向进行RFA,穿刺过程中均准确进入病灶,术中未出现严重并发症。
单一RFA治疗容易出现消融不彻底、局部肿瘤进展反应或并发症的发生[2,9]。Morimoto等[10]和Peng等[11]指出,对于不能手术切除的单发或多发肝癌,联合TACE治疗效果更好。其优势主要在于:①TACE是肝癌非手术治疗的主要方式,通过对肿瘤病灶进行化疗药物灌注,并对肿瘤供血动脉进行栓塞,抑制肿瘤生长进展,从而引起肿瘤坏死而缩小病灶范围;②因TACE治疗方式仍以碘油为主,故膈下病灶碘油沉积可为CT引导下RFA作图像引导,提高穿刺精准性;③由于碘油在病灶的沉积,可增强RFA的热传导效应,从而提高疗效;④TACE联合RFA治疗膈下肝癌,可减小因RFA热效应对周围重要脏器的损伤,避免严重并发症的发生。
随访期间,61处病灶中49.2%达到CR,39.3%达到PR,11.5%处于SD,无PD出现,ORR为88.5%,DCR为100%,所有患者均获益。经TACE联合RFA治疗后6个月生存率98.2%,治疗后1年、2年、3年患者生存率分别为90.9%、80.0%、72.7%。在随访过程中发现肿瘤复发及进展的患者均采取治疗措施。其中,治疗后6例患者因肿瘤复发而再次进行TACE联合RFA的,经治疗后病灶控制较好,且无严重并发症出现。4例在1年后出现门脉癌栓,采用D-TACE联合门脉125I粒子植入治疗后有所好转,术中无严重并发症出现。
以往有文献报道RFA术中患者出现疼痛[12],术中疼痛会影响患者屏气时射频针的刺入,从而导致穿刺偏移而损伤周围脏器,引起严重并发症,因此镇痛也是RFA治疗的一大关键。Yokoyama等[13]报道了瑞芬太尼连续静脉给药对于RFA术中疼痛的缓解效果。为了有效缓解患者在消融治疗过程中的疼痛,我们在术前预先给予患者静脉滴注氟比洛芬酯或地佐辛,用1%利多卡因从皮肤至肝被膜进行局麻,术中将利多卡因和0.9%NaCl溶液进行1:1稀释,将适量利多卡因稀释液通过射频针的进水孔对肿瘤病灶缓慢灌注,若患者疼痛仍未缓解,则给予吗啡肌内注射。这种镇痛方式镇痛效果显著,患者在术中均未诉肝区有明显疼痛反应。
目前对于不可切除的膈下肝癌治疗尚无统一的安全有效方法。有文献报道,只要具备娴熟的操作技能和丰富经验,膈下肝癌RFA的治疗结果与其他部位肝癌并无显著差异[14-15]。以往有报道125I放射性粒子联合TACE序贯RFA治疗包膜下肝癌[16],但其对于膈下肝癌的治疗效果还有待大样本数据的验证。本次研究中仍有一些不足,如没有比较有无肝硬化背景的膈下肝癌患者治疗获益情况。目前还有新的治疗方法有待进一步研究,比如出现多种新型栓塞材料如载药微球,可显著提高肝癌患者生存率[17],是否可以通过提高TACE疗效,继而联合RFA治疗膈下肝癌患者使其获益更大还有待研究;膈下肝癌患者在进行RFA过程中,由于病灶与周围脏器距离较近,射频针不能距离膈肌过近以免损伤脏器,因而容易出现治疗不完全,若对肿瘤病灶的安全消融部分进行热消融来杀伤肿瘤细胞,剩余部分能否通过碘油的热传导效应达到周围未消融区域肿瘤坏死,还有待进一步研究来证明。
总之,TACE联合RFA治疗膈下肝癌是安全、有效的,两者可以互相弥补不足,能显著控制肿瘤发展,延长患者生存率,避免术后严重并发症的发生,是临床上疗效显著的治疗方法。
