含分子内配位作用的环状铋(III)化合物抑制人乳腺癌MCF-7细胞增殖的初步研究
2020-04-13欧颖璨刘永平
欧颖璨,刘永平,陈 懿
(湖南中医药大学医学院,中国 长沙 410208)
乳腺导管上皮细胞在各种内外致癌因素的作用下异常增生,超过自我修复的限度而发生的癌变,即乳腺癌,是全世界女性最常见的癌症死亡原因[1-4]。据国家癌症中心2019年公布的2015年乳腺癌发病数据显示,乳腺癌发病率位居女性恶性肿瘤的第1位,全国大概有30.4万的女性罹患乳腺癌[5]。上世纪60年代美国科学家Rosenborg首次发现顺铂(cisplatin)对肿瘤细胞生长具有良好的抑制作用,以顺铂为代表的铂系抗肿瘤药物在癌症治疗中发挥了巨大的作用[6]。然而,长期的临床实践中,人们发现顺铂及其衍生物对乳腺癌的治疗效果不尽如人意[7,8]。因此,研发高效、低毒的新型金属类抗乳腺癌药物仍然是当前化学和药学的研究热点之一。
铋(bismuth)是自然界中唯一的“绿色”重金属,兼具价格低廉、毒性低、放射性弱等性质,故铋系化合物作为生物医药应用具有“得天独厚”的优势。1786年,Odier等[9]报导了首例用于治疗消化不良的铋系药物,由此揭开了铋系化合物在生物医药领域研究的序幕。在此后两个多世纪,大量结构新颖和理化性质特异的铋化合物被相继报道并广泛地用于治疗炎症、溃疡、痔疮、梅毒以及SARS病毒感染等疾病[10-12]。此外,铋系药物在抗肿瘤领域的研究得到了国内外科研工作者的广泛关注[13-25]。例如,212Bi和213Bi可以作为治疗小型肿瘤的化疗药剂[19,20],联用硝酸铋和柠檬酸铋能够减轻铂系药物在癌症治疗过程中造成的毒副作用[21]。近年来,随着有机金属化学的飞速发展,一些含有铋-碳共价键的非放射性有机铋化合物对恶性肿瘤细胞的生长抑制作用也被相继报道[22-25]。然而,目前人们对铋系抗肿瘤药物的研究普遍集中于治疗血液肿瘤的探究,如白血病、骨髓瘤以及恶性淋巴瘤等,有关铋剂在治疗乳腺癌等实体肿瘤的研究却鲜有报道。
尹双凤等[26,27]曾报道了10余种杂铋(III)环化合物,抗肿瘤活性实验结果表明,与常规的抗肿瘤药物顺铂相比,该类型有机铋(III)配合物对多种肿瘤细胞(人肺癌细胞A549,人肝癌细胞SMCC7721,人胃癌细胞MGC-803和SGC-7901,人结肠癌细胞SW480)具有更优的抗增殖活性,证实了杂铋(III)环化合物在抗肿瘤研究领域的研究价值和开发潜力。笔者针对环状结构的优势考察了5种含分子内E→Bi配位作用的有机铋(III)配合物对MCF-7人乳腺癌细胞生长抑制率的影响,遴选出药效最优的配合物,为进一步设计高效、低毒的铋系抗乳腺癌药物提供理论指导和技术支撑。
1 实验部分
1.1 仪器与试剂
仪器:SW-CJ型净化工作台(苏州净化),XDS型倒置显微镜(上海蔡康光学仪器),HF90型CO2培养箱(上海力康),SZ-95双纯水蒸馏器(上海雅荣),YTD100E消毒柜(广东樱雪),16045型酶标仪(美国伯乐)。
试剂:氯化铋(安耐吉化学)、正丁基锂(百灵威试剂公司)、硫酸钠(国药试剂公司),所用试剂均为AR,无水溶剂使用前均按标准程序干燥;配体[2,2′-(氧二(亚甲基))二(溴苯)、N,N-双(2-溴苄基)苯胺、双(2-溴苄基)环己胺、1-溴-2-(((2-溴苄基)氧基)甲基)萘、(2-溴苄基)((1-溴萘-2-基)甲基)硫烷]参照文献[27]所报道的方法获得;CCK-8试剂盒(同仁)。
1.2 铋化合物的合成
参照文献[27]所报道的方法制备了5种含三齿配体的环状铋(III)化合物,具体合成步骤如下:氮气氛围下,于350 mL的Schlenk反应管中,依次加入相应的配体和150 mL超干的乙醚,待固体充分溶解,将反应管移置-60 ℃乙醇浴中,逐滴加入2.5 mol·L-1正丁基锂20.4 mL,逐步升至室温,反应4 h。在-78 ℃乙醇浴中,搅拌下逐滴加入8.03 g(25.5 mmol)氯化铋的乙醚(60 mL)溶液,逐步升至室温,直至反应完毕。减压脱去乙醚,用二氯甲烷溶解残留物,过滤沉淀,去离子水洗涤有机层,无水Na2SO4干燥。减压脱去二氯甲烷,重结晶(CH2Cl2/hexane)获得目标化合物晶体,配合物的收率依次为:82%1,94%2,86%3,78%4,62%5。

1.3 铋化合物的表征数据
化合物1: 无色固体;熔点205~207 ℃;1H NMR (CDCl3, 400 MHz, TMS)δ8.62 (2H, d,J= 7.2 Hz), 7.58 (2H, t,J= 7.6 Hz), 7.44 (2H, d,J= 7.6 Hz), 7.32 (2H, t,J= 7.6 Hz), 5.25 (2H, d,J= 13.6 Hz), 4.85 (2H, d,J= 13.6 Hz);13C NMR (CDCl3, 100 MHz, TMS)δ173.4, 144.7, 139.7, 137.7, 132.3, 132.0, 128.0, 127.0, 126.9, 77.8.
化合物2: 无色固体;熔点257~259 ℃;1H NMR (CDCl3, 400 MHz, TMS)δ8.60 (2H, d,J= 7.2 Hz), 7.51 (4H, t,J= 8.0 Hz), 7.44 (2H, d,J= 7.2 Hz), 7.31 (1H, t,J= 7.2 Hz), 6.65 (2H, t,J= 7.2 Hz), 6.47 (2H, d,J= 7.6 Hz), 4.76 (2H, d,J= 14.8 Hz), 4.52 (2H, d,J= 14.8 Hz);13C NMR (CDCl3, 100 MHz, TMS)δ172.66, 147.47, 146.98, 137.43, 130.66, 128.79, 127.33, 127.13, 124.06, 118.06, 62.27.
化合物3: 无色固体;熔点266~269 ℃;1H NMR (CDCl3, 400 MHz, TMS)δ8.62 (2H, d,J= 7.6 Hz), 7.39-7.48 (4H, m), 7.31 (2H, t,J= 7.6 Hz), 4.36 (2H, d,J= 15.2 Hz), 4.15 (2H, d,J= 15.2 Hz), 2.92 (1H, t,J= 11.6 Hz), 1.99 (2H, d,J= 11.6 Hz), 1.84 (2H, d,J= 12.8 Hz), 1.63 (1H, d,J= 12.8 Hz), 1.23~1.42 (4H, m), 1.12 (1H, t,J= 12.8 Hz);13C NMR (CDCl3, 100 MHz, TMS)δ170.85, 149.69, 138.15, 130.799, 128.05, 127.63, 64.81, 60.67, 30.69, 25.65, 25.48。
化合物4: 黄色固体;熔点230~231 ℃;1H NMR (CDCl3, 400 MHz, TMS)δ9.05 (2H, m), 7.93 (1H, d,J= 8.4 Hz), 7.81 (1H, d,J= 8.4 Hz), 7.69 (1H, t,J= 7.2 Hz), 7.61 (1H, d,J= 8.4 Hz), 7.57 (1H, d,J= 7.6 Hz),7.45~7.50 (2H, m), 7.42 (1H, t,J= 7.6 Hz), 5.28 (2H, d,J= 16.0 Hz), 5.04 (1H, d,J= 13.2 Hz), 4.96 (1H, d,J= 14.0 Hz);13C NMR (CDCl3, 100 MHz, TMS)δ145.8, 143.8, 141.5, 141.1, 139.0, 136.0, 133.0, 131.4, 129.0, 128.7, 128.3, 127.8, 126.3, 126.1, 124.8, 78.2, 76.1。
化合物5: 绿色固体;熔点247~249 ℃;1H NMR (CDCl3, 400 MHz, TMS)δ9.25 (1H, d,J= 7.6 Hz), 9.02 (1H, d,J= 8.8 Hz), 7.91 (1H, t,J= 8.0 Hz), 7.85 (1H, d,J= 8.4 Hz), 7.67 (1H, d,J= 7.6 Hz),7.55~7.65 (3H, m), 7.48 (2H, t,J= 7.6 Hz), 4.99 (1H, d,J= 14.0 Hz), 4.67 (1H, d,J= 15.6 Hz),4.27 (1H, d,J= 16.4 Hz), 4.22 (1H, d,J= 14.0 Hz);13C NMR (CDCl3, 100 MHz, TMS)δ150.8, 144.6, 141.1, 140.5, 134.6, 132.4, 131.8, 131.4, 129.0, 128.5, 128.3, 127.8, 126.7, 126.2, 41.7, 40.2。
1.4 MCF-7细胞生长抑制率的测试
采用CCK-8法测定5种铋(III)化合物对MCF-7细胞的生长抑制率。具体步骤如下:选取处于对数期的细胞在温度37 ℃、潮湿的二氧化碳与空气(体积比1∶19)混合气中连续孵育12 h;传代,配制指定浓度的悬浮液,于96孔培养板上按0.1 mL/孔接种,并在标准条件下继续孵育24 h;孵育结束后,弃去上清液,分别加入含指定浓度配合物(溶于二甲基亚砜中)的培养液,并以仅包含二甲基亚砜的培养液作为空白对照,在37 ℃条件下连续孵育一定时间;而后弃去上清液,洗涤,加入10 μL指定浓度的CCK-8试剂,在标准条件下孵育约2 h;最后,利用酶标仪测定细胞中生成的甲臜含量,生长抑制率百分比的计算公式见式1。实验过程中,每组数据至少独立重复3次,使用Graphpad prism程序通过非线性回归分析确定各铋(III)化合物的半抑制浓度(IC50值)。

(1)
2 结果与讨论
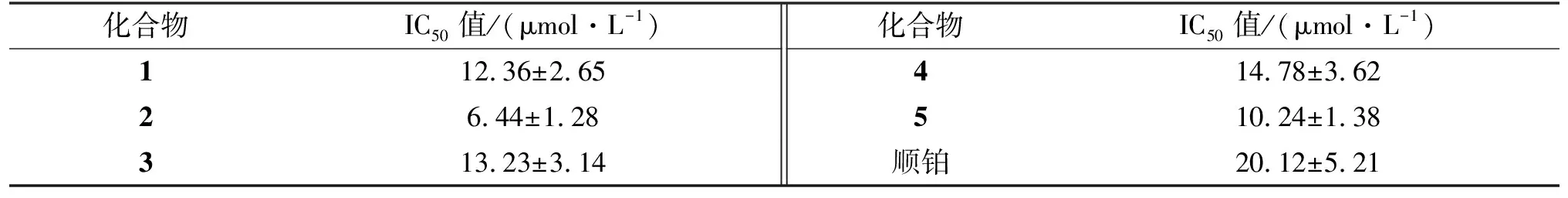
由表1可知,铋(III)化合物1~5对人乳腺癌细胞MCF-7具有不同程度的抗增殖作用,且该系列化合物对肿瘤细胞的生长抑制作用明显优于顺铂(20.12 μmol·L-1)。其中,Bi(III)化合物2的抗增殖作用尤为显著,其半抑制浓度(IC50值)可低至6.44 ± 1.28 μmol·L-1,表明了该化合物在癌症治疗领域中潜在的药用前景。进一步分析Bi(III)化合物1~3对MCF-7细胞的生长抑制率,发现配位原子的电子云密度越小,相应化合物对肿瘤细胞的生长抑制作用越强(IC50值:1, 12.36 μmol·L-1,vs2, 6.44 μmol·L-1,vs3, 13.23 μmol·L-1)。由此推测,Bi(III)化合物1~3对MCF-7细胞的抗增殖活性可能与Bi中心和配位原子之间的配位能力有关。此外,环状结构的位阻效应也能够影响Bi(III)化合物的抗癌药效。例如,化合物4与1的O→Bi配位能力无显著差异(O→Bi配位键键长:1, 0.254 3 nmvs4, 0.254 8 nm)[27],但化合物4对MCF-7细胞的增殖抑制作用要明显差于化合物1(IC50值:1, 12.36 μmol·L-1,vs4, 14.78 μmol·L-1),原因可能是化合物4具有空间位阻更大的配体骨架。(C,S,C)型三齿螯合铋(III)化合物5对MCF-7细胞的抗增殖活性明显优于(C,O,C)型衍生物4(IC50值:4, 14.78 μmol·L-1vs5, 10.24 μmol·L-1)。为了揭示铋化合物的构-效关系,笔者在今后的研究工作中拟利用多种表征技术深入探究铋化合物对肿瘤细胞的作用机制。综上所述,该系列含分子内配位作用的有机铋(III)化合物具有潜在的临床应用前景,通过改变配位原子的电子效应及配体骨架的空间位阻可以实现对其抗肿瘤活性的调控,这为进一步设计研发高效、低毒的铋类抗癌药物提供了有益的参考依据。
表1铋(III)化合物1~5及顺铂作用MCF-7细胞的IC50值
Tab.1IC50values of heterocyclic organobismuth(1~5) complexes and cisplatin on MCF-7 cells
化合物IC50值/(μmol·L-1)化合物IC50值/(μmol·L-1)112.36±2.65414.78±3.6226.44±1.28510.24±1.38313.23±3.14顺铂20.12±5.21
3 结论
使用CCK-8法考察了5种含三齿配体的Bi(III)化合物对MCF-7细胞的抗增殖作用。研究结果表明,该类型有机铋(III)化合物1~5对MCF-7细胞均有一定程度的抗增殖作用。其中PhN(C6H4CH2)2BiCl(2)作为活性最优的配合物半抑制浓度可低至6.44 μmol·L-1,远优于常用的抗肿瘤药物顺铂,说明有机铋化合物在癌症治疗领域中具有良好的药用前景。Bi(III)化合物的构-效关系研究结果也表明,通过改变配位原子的类型及配体骨架的空间位阻能够实现对该类型含分子内配位作用的Bi(III)化合物抗肿瘤活性的调控。
