miR-155-5p对急性髓系白血病细胞凋亡的影响及可能机制
2020-04-11邓之奎朱伟
邓之奎, 朱伟
(1. 江苏大学医学院, 江苏 镇江 212013; 2. 淮安市第一人民医院血液科实验室, 江苏 淮安 223300)
近年来,随着化疗、造血干细胞移植、免疫治疗、分子靶向治疗等技术的进步,急性髓系白血病(acute myeloid leukemia,AML)患者大多能获得完全缓解,标准的一线诱导化疗方案能够使60%~80%的年轻患者以及40%~60%的老年患者获得缓解,然而,仍有60%的患者缓解后面临复发的风险[1]。耐药是AML患者治疗失败、生存率低的关键因素[2],然而AML耐药的确切机制尚不完全明确。近年来,AML耐药机制的研究主要集中在耐药相关蛋白及酶异常、基因突变、miRNAs的改变以及耐药相关信号通路的异常活化[3]。本研究以AML患者骨髓单个核细胞(BMMNC)以及AML细胞系为研究对象,探讨miR-155-5p对AML细胞凋亡的影响及可能机制,为临床克服AML患者化疗耐药、提高疗效提供实验依据。
1 材料和方法
1.1 BMMNC采集
收集本院2016年1月至2018年12月43例AML患者,诊断标准参照WHO急性白血病临床分型(2016),所有患者均经细胞形态学、免疫分型、细胞遗传学和分子学(MICM)确诊。患者的中位年龄36(18~75)岁,男24例,女19例。采用Ficoll密度梯度离心法分离出BMMNC,分装至1.5 mL EP管内(每管细胞数约1×106),保存于-80 ℃低温冰箱。对照组为21例缺铁性贫血患者。标本采集经淮安市第一人民医院医学伦理委员会批准,并获得患者本人知情同意。
1.2 细胞系及培养
HL-60、THP-1细胞系购于美国ATCC细胞库(美国Virginia公司),用含有10%胎牛血清、100 mg/mL链霉素和100 U/mL青霉素的RPMI-1640培养基(美国Invitrogen公司)于37℃、5% CO2的饱和湿度培养箱中培养,每隔48~72 h换培养液1次,取对数生长期细胞用于后续实验。
1.3 试剂
Bcl-2抗体(美国Proteintech公司);NF-κB(p65)抗体、β-肌动蛋白抗体、羊抗鼠IgG-HRP抗体、羊抗兔IgG-HRP抗体(美国Cell signaling Technology公司);ECL检测发光试剂盒(美国Bioworld Technology公司);细胞凋亡试剂盒(德国MiltenyiBiotec公司);总蛋白提取试剂盒(南京诺唯赞公司);qRT-PCR相关的逆转录及扩增试剂盒(中国Vazyme公司);PVDF膜(中国凯基生物科技有限公司);CCK-8试剂盒(日本同仁生物科技有限公司);miR-155-5p转染试剂盒(上海生工生物科技有限公司)。
1.4 qRT-PCR检测BMMNC中miR-155-5p和Bcl-2 mRNA的表达
Trizol法提取BMMNC的总RNA,通过逆转录试剂盒,Oligo引物及逆转录酶将总RNA逆转录为cDNA。miR-155-5p特异引物为5′-TTAATGCTAATCGTGATAGGGGT-3′;Bcl-2上游引物为5′-CCCCACAGTCTACTGTAAG-3′,下游引物为5′-GCATTGCCGATGGTACTGATT-3′;β-肌动蛋白上游引物为5′-GGCATCGTGATGGACTCCG-3′,下游引物为5′-GCTGGAAGGTGGACAGCGA-3′。定量PCR(美国应用生物系统公司7300扩增仪)反应程序为95℃ 3 min,95℃ 30 s,40个循环,62℃ 40 s。扩增结果以β-肌动蛋白作为内参基因,采用ΔΔCt法计算相对定量。
1.5 细胞转染
miR-155-5p类似物:5′-GAUAGUUCGGUGUGCACA-3′,miR-155-5p类似物对照:5′-AUGGUCGUUAAGCCAGUG-3′;miR-155-5p抑制剂:5′-CGGAUAUGUGCAGUGCUA-3′,miR-155-5p 抑制剂对照:5′-AGGCAGUGUCGUCAAUUG-3′。依据转染试剂盒说明书,取对数生长期的HL-60、THP-1细胞分别接种于6孔板,次日细胞汇合度达30%~50%时,加入混匀后的脂质体2000和miR-155-5p类似物或抑制剂,室温孵育30 min,置于37℃、5%CO2的孵育箱中转染6 h后换液,继续培养48 h。qRT-PCR验证转染效率,方法同步骤“1.4”。
1.6 CCK-8法检测HL-60和THP-1转染细胞的活性
取转染后处于对数生长期的HL-60、THP-1细胞,以4×104/mL的密度接种于96孔培养板中,每孔体积为100 μL。加入不同浓度的化疗药物阿糖胞苷(终浓度为0、0.01、0.02、0.04、0.08、0.16、0.32、0.64和1.28 μg/mL),置于37℃、5% CO2的培养箱中孵育48 h,弃去上清液,每孔中加入100 μL PBS和10 μL的WST-8试剂,避光37℃温箱孵育2 h后用酶标仪检测光密度(D)值,检测波长为480 nm。每个浓度设置3个复孔。
1.7 流式细胞术检测HL-60和THP-1转染细胞的凋亡率
将转染后的HL-60、THP-1细胞以每孔1×105个的密度接种于6孔板中,各设3个复孔,待细胞贴壁后,加入阿糖胞苷(0.16 μg/mL)处理48 h后,用酶消化法收集细胞于1.5 mL EP管中,1 000 r/min离心10 min,PBS洗涤1次,每管加入200 μL结合液、5 μL Annexin V试剂和10 μL PI试剂,避光室温孵育10 min后置于冰上。流式细胞仪检测细胞凋亡率。
1.8 qRT-PCR法检测转染miR-155-5p抑制剂后HL-60和THP-1细胞NF-κB、Bcl-2的mRNA表达
Trizol法提取转染miR-155-5p抑制剂后HL-60和THP-1细胞的总RNA,通过逆转录试剂盒,Oligo引物及逆转录酶将总RNA逆转录为cDNA。NF-κB上游引物为5′-CCTATGTGGAGATCATTGAGCA-3′,下游引物为5′-CAAAGATGGGATGAGAAAGGAC-3′;Bcl-2上游引物为5′-CCCCACAGTCTACTGTAAG-3′,下游引物为5′-GCATTGCCGATGGTACTGATT-3′;β-肌动蛋白上游引物为5′-GGCATCGTGATGGACTCCG-3′,下游引物为5′-GCTGGAAGGTGGACA GCGA-3′。定量PCR(美国应用生物系统公司7300扩增仪)反应体系:上下游引物各1 μL、Taq DNA聚合酶12.5 μL、模板cDNA 2 μL、去离子水8.5 μL,总反应体系25 μL。扩增条件:95℃预变性3 min,94℃ 30 s,66℃ 30 s,72℃ 1 min,共35个循环,72℃ 5 min。扩增结果以β-肌动蛋白作为内参基因,采用ΔΔCt法计算相对定量。
1.9 蛋白质印迹法检测转染miR-155-5p抑制剂后HL-60和THP-1细胞NF-κB、Bcl-2的蛋白表达
6孔板每孔用1 mL PBS洗涤1次,置于冰上,每孔加入70 μL含蛋白酶抑制剂的细胞裂解液,细胞刮刀顺同一方向将转染miR-155-5p抑制剂后的AML细胞轻轻刮下,吸取每孔中的蛋白裂解液至1.5 mL EP管中,振荡器振荡混匀1 min,置于冰上10 min后继续振荡1 min,重复3次,4℃、12 000×g离心15 min后吸取上清液至新EP管中,按照4 ∶1的比例加入5×上样缓冲液,水浴煮沸8 min,-20℃短期保存。取50 μg蛋白质为上样量,先经80 V恒压电泳,当蛋白进入积层胶时将电压调至100 V恒压电泳,待蛋白跑至胶底部后以350 mA恒流电转2 h,将PVDF膜浸于5%脱脂牛奶中封闭1 h,分别加入一抗(NF-κB、Bcl-2、β-肌动蛋白,稀释比例1 ∶1 000),4℃孵育过夜。次日以TBST洗涤3次,每次10 min,加入HRP标记的羊抗兔IgG二抗(稀释比例1 ∶2 000),37 ℃温育1 h,最后,加入Millipore的曝光液(A液和B液按1 ∶1的比例混合),采用化学发光凝胶成像系统进行检测。
1.10 统计学处理

2 结果
2.1 miR-155-5p、Bcl-2在AML患者BMMNC中高表达
qRT-PCR结果显示AML患者较缺铁性贫血患者BMMNC的miR-155-5p和Bcl-2 mRNA表达明显升高(图1)。
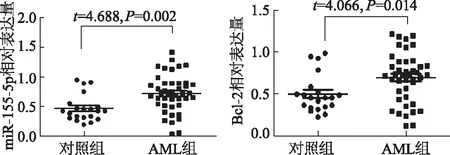
图1 miR-155-5p、Bcl-2在AML患者BMMNC中高表达
2.2 miR-155-5p对阿糖胞苷处理的HL-60和THP-1细胞活性和凋亡的影响
HL-60细胞转染miR-155-5p类似物或抑制剂后,qRT-PCR检测转染效率,miR-155-5p表达较对照组有明显差异(F=124.7,P<0.01),见图2A。CCK-8及流式检测结果显示转染miR-155-5p类似物的HL-60细胞经阿糖胞苷处理后细胞活性较对照组增加,细胞凋亡率明显减少(t=6.806,P<0.01);而转染miR-155-5p抑制剂组细胞活性降低,凋亡率明显增加(t=3.790,P<0.01),见图2B、C。qRT-PCR检测THP-1细胞转染miR-155-5p类似物或抑制剂转染效率,miR-155-5p表达较对照组有明显差异(F=295.3,P<0.01),见图3A。阿糖胞苷处理后转染miR-155-5p类似物的THP-1细胞活性增强,凋亡率减少(t=4.487,P<0.01);转染miR-155-5p抑制剂的THP-1细胞活性降低,凋亡率增加(t=16.01,P<0.01),见图3B、3C。

图2 miR-155-5p对阿糖胞苷处理的HL-60细胞活性和凋亡的影响
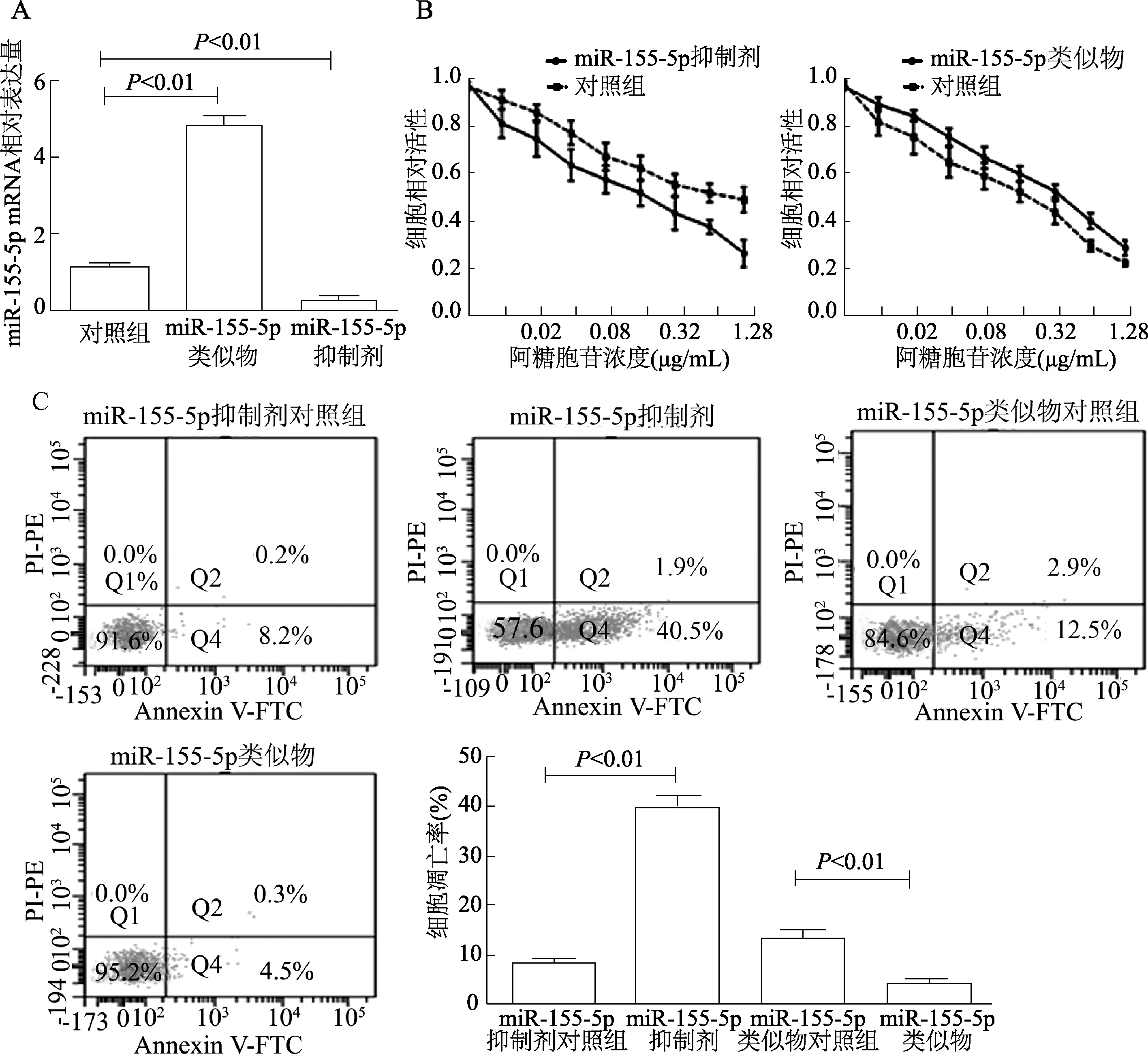
图3 miR-155-5p对阿糖胞苷处理的THP-1细胞活性和凋亡的影响
2.3 抑制miR-155-5p后HL-60和THP-1细胞NF-κB、Bcl-2表达减少
qRT-PCR和蛋白质印迹结果显示,HL-60细胞转染miR-155-5p抑制剂后,NF-κB、Bcl-2在mRNA水平与蛋白水平的表达均下降(P均<0.05),见图4A、4B。用THP-1细胞重复上述实验进行验证也发现同样的结果(P均<0.05),见图4C、4D。表明miR-155-5p可能通过上调NF-κB、Bcl-2抑制AML细胞凋亡。
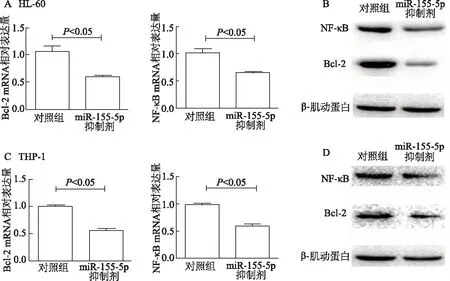
图4 抑制miR-155-5p对HL-60、THP-1细胞NF-κB、Bcl-2表达的影响
3 讨论
研究发现miRNAs主要通过调控DNA损伤、细胞周期以及细胞凋亡等介导肿瘤耐药[4-6]。研究表明,miR-155在多种肿瘤组织中表达异常,并与临床病理标志物、肿瘤分型和较低的存活率相关,能够介导多种信号通路,包括NF-κB信号通路,NF-κB可直接结合miR-155的启动子调控miR-155的表达。miR-155参与多种生理学过程,包括造血细胞分化、免疫反应、炎症以及肿瘤治疗耐药[7-8]。miR-155在多种实体肿瘤的发病机制中起着至关重要的作用,Bayraktar等[7]通过对乳腺癌、结肠癌、肺癌、胰腺癌、前列腺癌和胃癌6个实体肿瘤的540个样本的miRNA表达谱进行分析,发现miR-155的表达在乳腺癌、肺癌和结肠癌样本中上调,并可促进包括乳腺癌和肺癌在内的几种癌症的肿瘤细胞生长、细胞迁移、侵袭以及上皮间质转化。
miR-155除了在实体瘤的发生及耐药中发挥重要作用外,也参与多种血液肿瘤的发病及耐药。miR-155是血液系统肿瘤最具有特征性的致癌miRNA,包括弥漫大B细胞淋巴瘤、滤泡淋巴瘤、慢性淋巴细胞白血病、霍奇金淋巴瘤、合并FLT3-ITD基因突变的AML[9-12]。高表达的miR-155可以显著增强肿瘤细胞活性,同时降低白血病细胞对化疗药物的敏感性[7]。研究证实miR-155在成人与儿童AML中高表达,特别是FLT3-ITD突变的AML,且高表达miR-155的AML患者预后较差[13]。本研究通过分析AML患者临床样本发现miR-155-5p、Bcl-2在AML患者BMMNC中表达明显增高。
为了进一步验证miR-155-5p在AML细胞生长及凋亡中的作用,在AML细胞系中,分别转染miR-155-5p类似物与miR-155-5p抑制剂,发现转染miR-155-5p类似物组细胞活性增加、凋亡减少,而转染miR-155-5p抑制剂组细胞活性降低、凋亡增加,提示miR-155-5p可以提高AML细胞活性、抑制其凋亡。同时,在转染miR-155-5p抑制剂的AML细胞中,NF-κB、Bcl-2的mRNA和蛋白水平表达均降低,提示miR-155-5p促进抗凋亡蛋白Bcl-2表达,并抑制AML细胞凋亡。
综上,本研究结果显示miR-155-5p、Bcl-2在AML患者BMMNC中高表达,在AML细胞中miR-155-5p可以促进AML细胞对阿糖胞苷的抗性、抑制其凋亡,miR-155-5p可能通过促进NF-κB、Bcl-2的表达抑制AML细胞凋亡。因此,miR-155-5p或可作为提高AML治疗效果的分子靶标。
