紫杉醇脂质体联合铂类治疗晚期食管癌疗效与安全性系统评价*
2020-04-11王亚露江洁美许杜娟
王亚露,江洁美,方 玲,许杜娟,△
(1.安徽医科大学药学院,安徽 合肥230032;2.安徽医科大学第一附属医院药剂科,安徽 合肥230022)
食管癌患者预后通常较差,确诊时多数已为局部不可切除或有远处转移,故多采用姑息性化学治疗(简称化疗)[1]。紫杉醇为抗微管药物,可破坏微管和微管蛋白二聚体间存在的动态平衡,诱导和促进微管蛋白装配微管,防止解聚,抑制细胞有丝分裂,使细胞阻滞于M期,从而发挥抗肿瘤作用[2]。以紫杉醇为基础的联合化疗方案治疗食管癌已被多项临床试验证实具有一定疗效[3-7],且在2019年食管癌和食管胃交界癌美国国立综合癌症网络(NCCN)临床实践指南和2018年版国家卫生健康委员会食管癌诊疗规范中均推荐紫杉醇和铂类的联合方案作为食管癌辅助化疗、同步放化疗及晚期化疗的主要治疗方案。由于紫杉醇几乎不溶于水,故加入聚氧乙烯蓖麻油提高紫杉醇的溶解度,但聚氧乙烯蓖麻油在体内降解时会引起严重过敏反应、肾毒性、神经毒性等不良反应。紫杉醇脂质体作为一种紫杉醇药物的新剂型,通过药物与脂质体在膜双层内的结合,提高了紫杉醇疏水分子的溶解度和体内的稳定性,避免了聚氧乙烯蓖麻油的毒副作用[8]。目前,已有文献在卵巢癌、乳腺癌、非小细胞肺癌及胃癌的治疗中将紫杉醇脂质体与普通紫杉醇进行疗效和安全性对比的Meta分析[9-16],但在治疗食管癌方面仅有随机对照试验(RCT)或单臂临床试验,有效性和安全性尚不确切。本研究中系统检索了相关文献,对紫杉醇脂质体治疗食管癌疗效与安全性的单臂试验及RCT进行了系统评价,为临床治疗提供参考。现报道如下。
1 资料与方法
1.1 文献纳入标准与排除标准
纳入标准:经临床内窥镜,细胞学、影像学等检查确诊为晚期食管癌;研究类型为采用紫杉醇脂质体联合铂类方案治疗晚期食管癌的临床试验,包含与普通紫杉醇对比的RCT;RCT中研究组干预措施为紫杉醇联合铂类化疗方案(包括顺铂、奈达铂、奥沙利铂),对照组干预措施为普通紫杉醇联合铂类化疗方案,两组患者的其他基础治疗相同;单臂试验与RCT研究组化疗方案相同;化疗时间为2个周期以上,21~28d为1个周期。
排除标准:缺失疗效和不良反应评价指标数据;重复发表;个案、综述、摘要及会议报告等;回顾性观察。
1.2 结局指标
本研究的疗效评价指标为客观缓解率(ORR),按世界卫生组织(WHO)或实体瘤的疗效评价标准(RECIST)制订的标准,ORR为完全缓解(CR)和部分缓解(PR)的病例数占总病例数的百分比。安全性评价指标为不良反应发生率,按常见不良事件评价标准(CTCAE 5.0版),不良事件的严重程度分为0~Ⅳ级,不良反应发生率=[(Ⅰ+Ⅱ+Ⅲ+Ⅳ)/总病例数]×100%。
1.3 文献检索策略
利用计算机检索数据库PubMed,Embase,Cochrane Library,WebofScience以及中国期刊全文数据库(CNKI)、中文科技期刊数据库(VIP)、万方数据库(WanFang Data),并辅以手工检索原文中的相关参考文献。检索时间为自建库至2019年7月。中文检索关键词:“紫杉醇”“泰素”“奥素”“普通紫杉醇”“紫杉醇脂质体”“力扑素”“注射用紫杉醇脂质体”“食管癌”“食管肿瘤”;英文检索关键词:paclitaxel OR taxol OR traditional paclitaxel and liposomal paclitaxel OR paclitaxel liposome OR lipusu and esophageal neoplasms OR esophageal cancer OR esophageal carcinoma。不限制发表语言、发表时间等。
1.4 文献筛选及资料提取
依据纳入与排除标准,由2位研究员独立完成文献筛选、数据提取,且进行交叉核对,若产生分歧则由第三位研究员进行裁定。提取资料的数据内容包括第一作者,发表时期,发表类型,患者特征(人数、年龄、疾病分期等),干预措施与化疗方法,化疗疗程,结局指标数据。
1.5 文献质量评价
2位研究员根据Cochrane系统评价手册5.1.0版[17],对最终纳入的RCT独立进行质量评价,若产生分歧则由第三位研究员进行裁定。根据偏倚类型包括选择偏倚:随机序列的产生、分配隐藏;实施偏倚:实施者与参与者双盲;测量偏倚:结局评估盲法;失访偏倚:结局数据不全;发表偏倚:选择性报告;其他来源偏倚。按照“低风险”“不清楚”“高风险”进行选择回答。
1.6 统计学处理
纳入的RCT采用Cochrane协作网提供的RevMan 5.3软件进行Meta分析,其中分类资料使用比值比(OR)或风险比(RR)和95%可信区间(CI)进行分析。各纳入研究结果间的异质性采用I2检验进行分析。若P>0.1,I2<50%,说明各研究间有统计学同质性,即采用固定效应模型进行Meta分析;若P<0.1,I2>50%,说明各研究间存在异质性,随即分析异质性来源,采用随机效应模型进行Meta分析,若异质性过大,则进行描述性分析。单臂试验研究中的分类变量由StataSE 11.0软件进行效应量合并。
2 结果
2.1 文献检索结果及纳入文献基本特征
首次检索文献172篇,经去重,最终共纳入13篇研究,文献纳入及排除过程见图1。其中单臂试验研究7篇[18-24],RCT研究6篇[25-30],包括713例患者。所有研究均报道了疗效与安全性,均在治疗2周期后进行疗效评价。纳入的单臂试验中紫杉醇脂质体应用剂量均为135 mg/m2。详见表1。
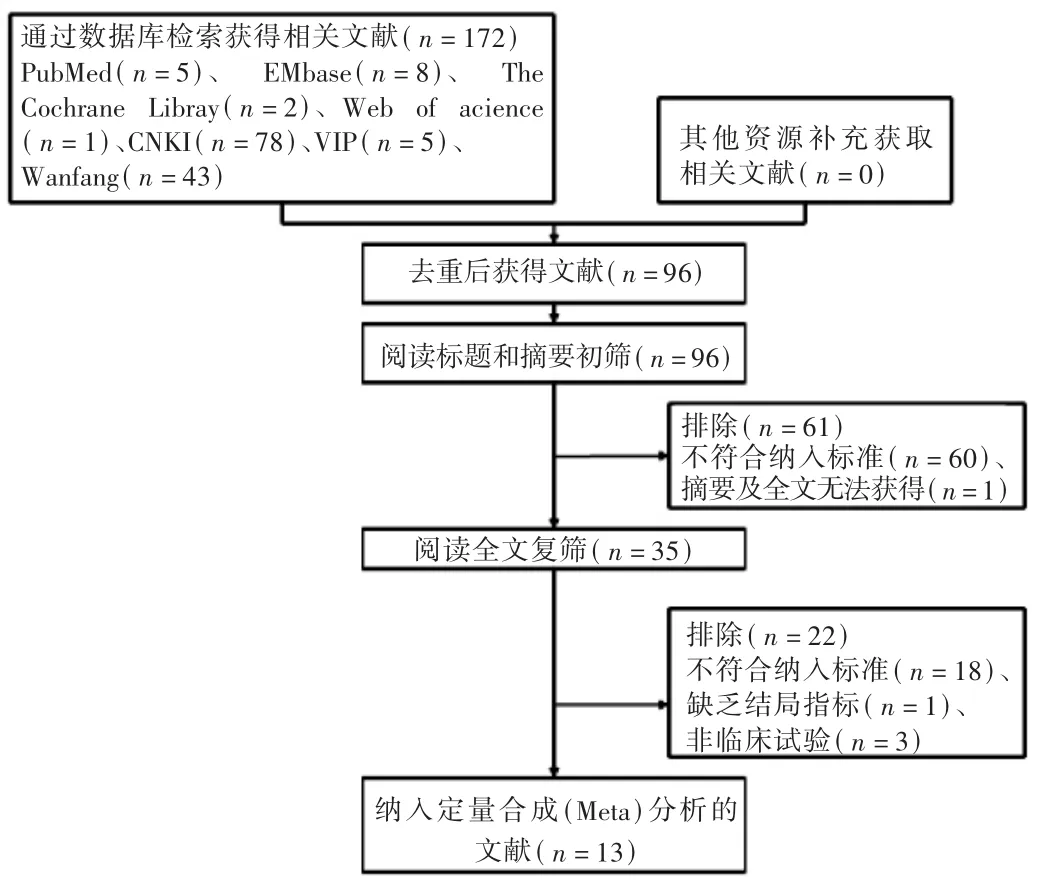
图1 文献筛选流程及结果
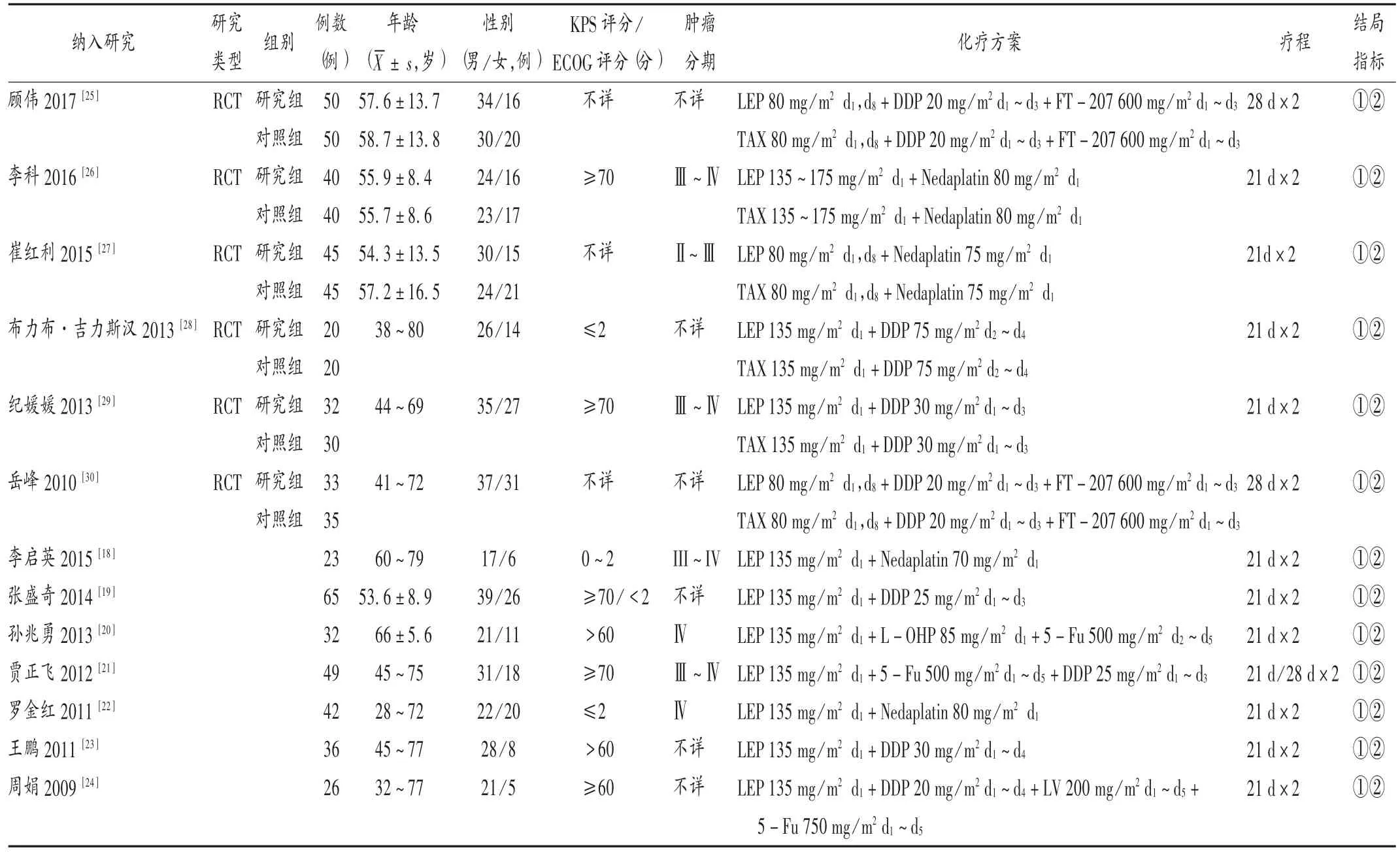
表1 纳入研究的基本特征
2.2 纳入文献的质量评价
对纳入的6篇RCT进行质量评价。6篇RCT均描述为随机分组,1个研究[26]运用“分层随机分组法”,评价为“低风险”,2个研究[27,30]按“入院先后分组”,评价为“高风险”,其余3个研究[25,28-29]未描述具体的随机方法,评价为“不清楚”。所有研究均未描述分配隐藏,盲法,评价为“不清楚”。所有研究报告的数据均完整且没有选择性报告的结果,评价为“低风险”。详见图2。
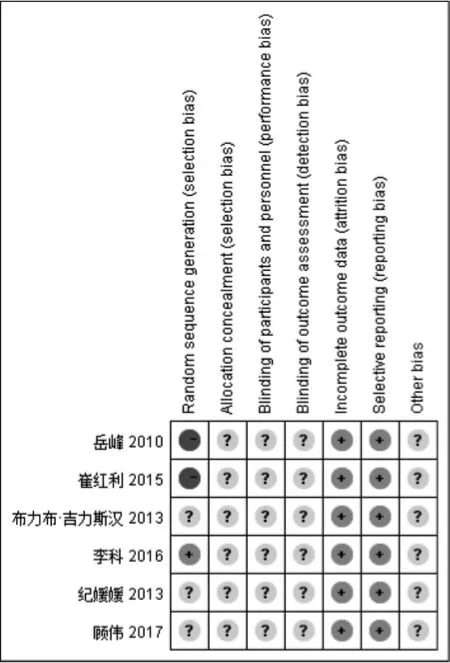
图2 纳入文献的偏倚风险图
2.3Meta分析结果
单臂试验的合并ORR:纳入了7篇紫杉醇脂质体的单臂试验研究[18-24],共273例患者,均报道了ORR,应用StataSE 11.0软件进行ORR的合并,计算合并ORR并绘制森林图,见图3。结果显示,ORR为46%,95%CI(0.40,0.52)。
RCT的ORR:纳入了6篇紫杉醇脂质体联合铂类与紫杉醇联合铂类治疗晚期食管癌的的RCT[27-32],均报道了ORR,患者440例。通过异质性检验,各研究同质性较好(P=0.81,I2=0%),故采用固定效应模型分析。结果显示,两组ORR比较,差异无统计学意义[RR=1.08,95%CI(0.87,1.35),P=0.50]。详见图4。
不良反应发生率:比较6个RCT中的不良反应发生率,出现的不良反应包括骨髓抑制、白细胞减少、血小板下降、血红蛋白减少、疲乏、呼吸困难、肌肉痛、皮肤潮红、消化道症状、脱发、恶心呕吐、心电图变化、肝功能损伤、肾功能损伤、周围神经炎、皮疹、腹泻及口腔黏膜炎。将至少2篇以上均报道的不良反应进行Meta分析,详见表2,由于各组同质性较好,均采用固定效应模型分析。其中紫杉醇脂质体呼吸困难、肌肉痛、恶心呕吐、皮肤潮红的发生率均低于紫杉醇组,差异有统计学意义(P<0.05)。详见图5。
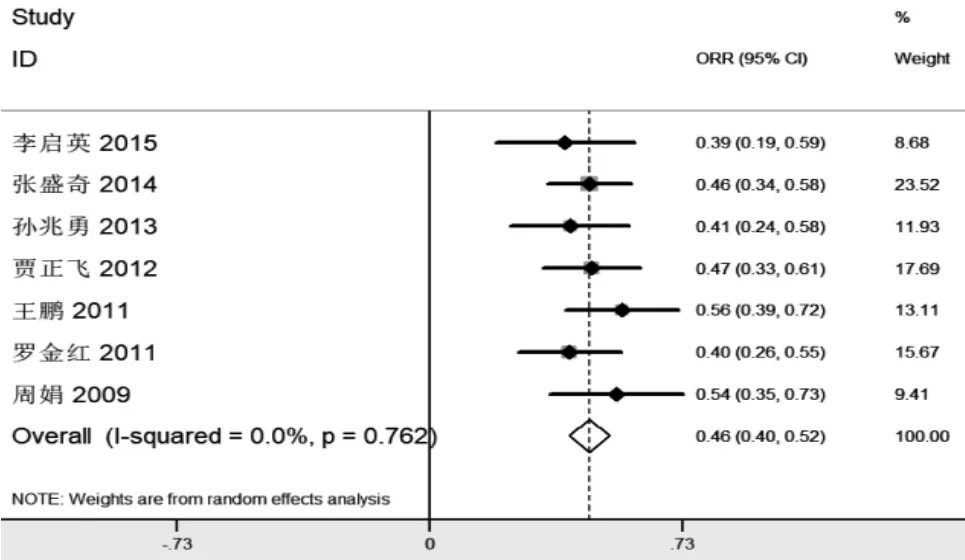
图3 单臂试验的合并客观缓解率Meta分析森林图
2.4 发表偏倚分析
基于客观缓解率的结果采用倒漏斗图进行发表偏倚分析。结果6个研究全部位于95%CI内,且基本呈对称分布,表明纳入的研究间不存在明显的发表偏倚。详见图6。
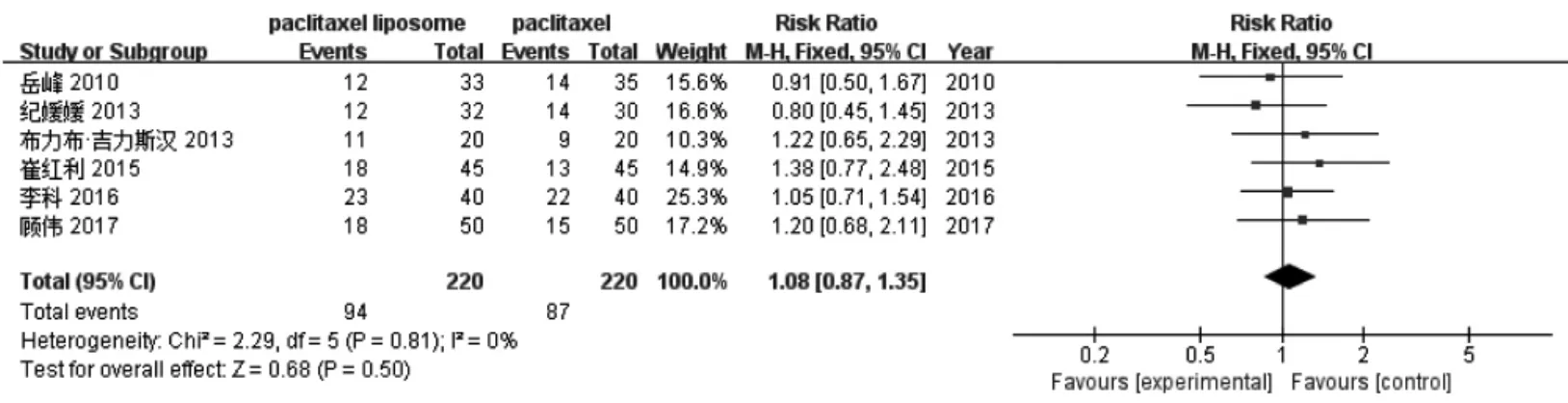
图4 两组ORR比较Meta分析森林图
3 讨论
本研究中纳入了紫杉醇脂质体治疗晚期食管癌的单臂试验,并通过合并客观有效率,结果显示,紫杉醇脂质体联合铂类治疗晚期食管癌有效率可达46%。与CAO等[31]报道的紫杉醇联合奈达铂在食管癌的一线治疗中所得的ORR=41.7%,95%CI(27.8,55.7%),与GONG等[32]报道的ORR=43.6%相近。故紫杉醇脂质体联合铂类治疗晚期食管癌疗效较好。
同时,将纳入的RCT进行Meta分析,在疗效方面通过ORR评价,结果显示,两组的ORR无显著差异(P=0.50),即紫杉醇脂质体联合铂类与紫杉醇联合铂类治疗晚期食管癌的疗效相当。紫杉醇脂质体和紫杉醇治疗卵巢癌、乳腺癌、晚期非小细胞肺癌的有效性比较无显著差异[9-10,12],疗效相当。但唐慕菲等[11]报道,在治疗卵巢癌的有效性上,两组有统计学差异(P=0.02),紫杉醇脂质体的疗效优于紫杉醇。以上分析结果不同的原因还需进一步临床试验去探讨。
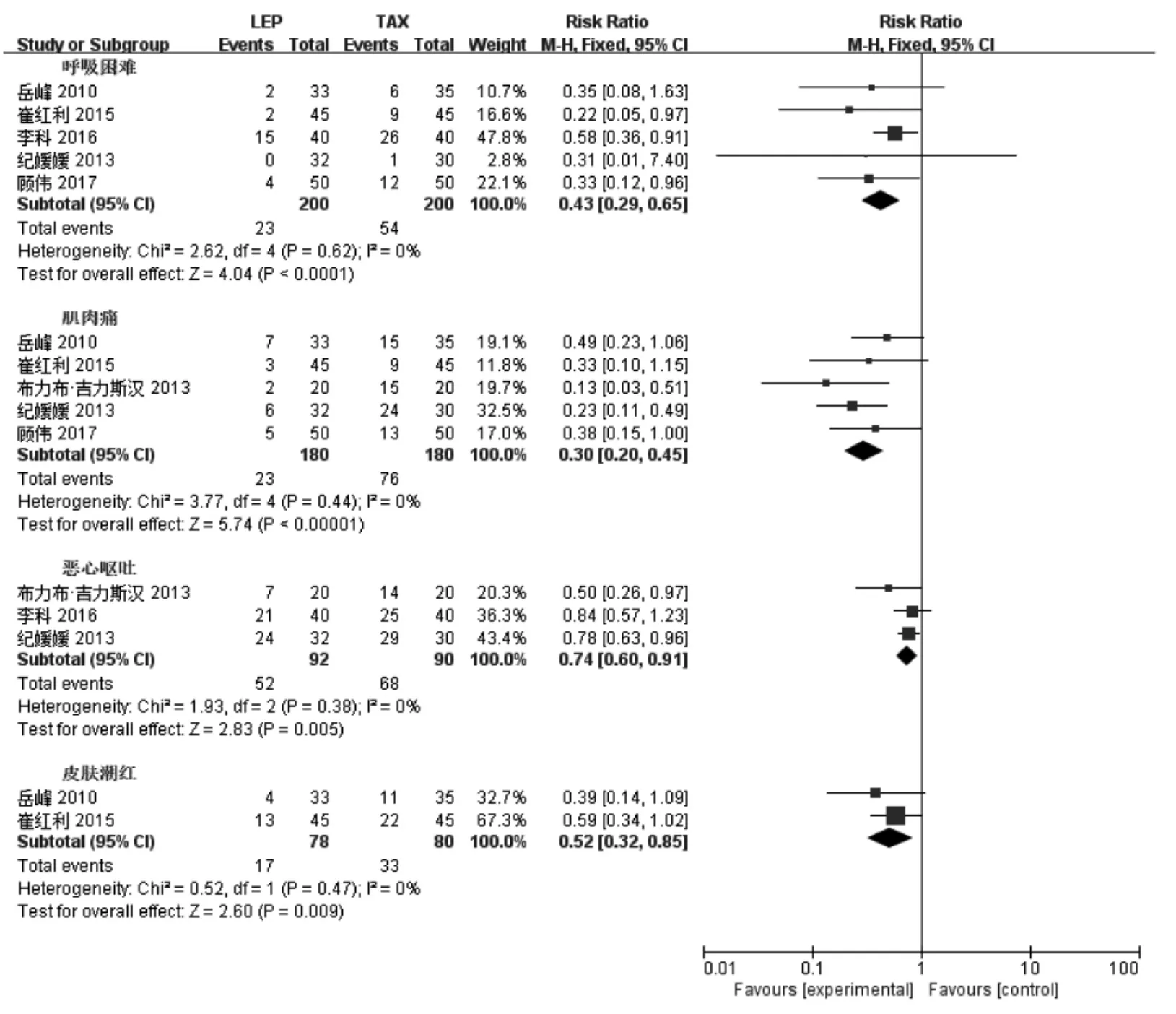
图5 两组不良反应发生率比较Meta分析森林图

表2 两组不良反应发生率Meta分析结果

图6 客观缓解率倒漏斗图
在安全性方面,通过对两组不良反应发生率进行Meta分析,其中紫杉醇脂质体联合铂类较紫杉醇联合铂类在呼吸困难、肌肉痛、恶心呕吐、皮肤潮红的发生率低(P<0.05)。过敏反应是紫杉醇注射液的主要不良反应,通常是由于紫杉醇注射液中的聚氧乙烯蓖麻油所引起,主要表现为局部或全身性潮红、呼吸困难、胸背部疼痛及常伴有恶心呕吐等消化道症状[33]。本研究结果显示,这几种不良反应,紫杉醇脂质体的发生率均低于紫杉醇,表明紫杉醇脂质体在一定程度上可降低过敏反应的发生率。过敏反应的出现,往往限制了继续用药,间接影响疗效。故通过剂型的改变,一定程度上可增加紫杉醇的用药机会和安全性,提高治疗效果,改善预后。
综上所述,紫杉醇脂质体联合铂类治疗晚期食管癌临床有一定获益率,且部分不良反应发生率明显较普通紫杉醇低。本研究局限性在于,检索出的文献均为中文文献,可能由于紫杉醇脂质体为我国自主研发药物,在国外的应用受限。自紫杉醇脂质体上市以来,临床应用日渐广泛,在国内药品市场的占有率有逐渐上升趋势[34]。由于紫杉醇脂质体的价格远高于普通紫杉醇,国内仍会进行一些RCT,探索两者的疗效和安全性差异,寻得更新的证据,但较少的样本量限制了效应量的检出,故仍需更高质量、更严谨、更大样本的RCT去验证。
