炎症性肠病合并血栓的临床特点及危险因素
2020-04-11尹明明樊周沛李颖霞温洪涛
尹明明,樊周沛,李颖霞,温洪涛
(郑州大学第一附属医院 消化内科,河南 郑州 450000)
炎症性肠病(imflammatory bowel disease,IBD)是一种慢性非特异性疾病,主要包括溃疡性结肠炎(ulcerative colitis,UC)和克罗恩病(crohn disease,CD)。IBD及其并发症严重影响患者的生活质量,其中血栓栓塞是可能危及生命的肠外并发症之一[1]。IBD患者发生血栓的机制尚不明确。机体可能通过多种机制影响血栓形成前状态,其中最重要的是获得性内皮细胞功能障碍、血小板异常、凝血系统激活及纤溶系统受损[2]。近年来研究发现,IBD血栓形成与疾病活动程度和应用糖皮质激素有关[2]。本研究探讨IBD合并血栓的临床特点及相关危险因素,旨在为该病的预防、筛查、诊断和治疗提供借鉴。
1 资料与方法
1.1 一般资料选取2010年1月至2019年4月郑州大学第一附属医院确诊的42例IBD合并血栓患者,将其纳入观察组。按照1∶2的比例纳入同期住院的性别、年龄相匹配的84例未出现血栓的IBD患者为对照组。纳入标准:(1)确诊为IBD,IBD诊断符合中华医学会消化病学分会炎症性肠病学组制定的《炎症性肠病诊断与治疗的共识意见》[3];(2)IBD发病期间合并急性血栓栓塞,符合《中国血栓疾病防治指南》中有关血栓的诊断标准[4]。排除标准:存在高血压、糖尿病、高脂血症、肿瘤等血栓形成的常见危险因素的患者。
1.2 收集指标性别、年龄、临床表现、实验室指标、肠镜及病理结果、血栓部位、治疗方法及预后。实验室指标包括血常规[白细胞计数(white blood cell,WBC)、血红蛋白(hemoglobin,Hb)、血小板(platelet,PLT)],凝血功能[凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partial thromboplastin time,APTT)、纤维蛋白原(fibrinogen,FIB)、D-二聚体],炎症指标[血沉(erythrocyte sedimentation rate,ESR)、C反应蛋白(C-reactive protein,CRP)]。
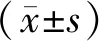
2 结果
2.1 一般资料根据选例标准,最终纳入42例IBD合并血栓患者(观察组),按1∶2比例纳入84例IBD未出现血栓的患者(对照组)。对照组男51例,女33例。观察组男26例,女16例。两组性别比较,差异无统计学意义(χ2=0.017,P=0.897>0.05)。两组年龄、PT、APTT、FIB、WBC、Hb、ESR比较,差异无统计学意义(均P>0.05)。观察组D-二聚体、PLT及CRP水平均高于对照组,差异有统计学意义(均P<0.05)。见表1。

表1 两组临床资料比较
注:PT—凝血酶原时间;APTT—活化部分凝血活酶时间;FIB—纤维蛋白原;WBC—白细胞计数;Hb—血红蛋白;PLT—血小板;ESR—血沉;CRP—C反应蛋白。
2.2 IBD合并血栓的危险因素通过单因素筛选出3个有差异的指标进入回归模型,结果表示,D-二聚体、PLT与CRP水平升高是IBD合并血栓的独立危险因素(均P<0.05)。见表2。
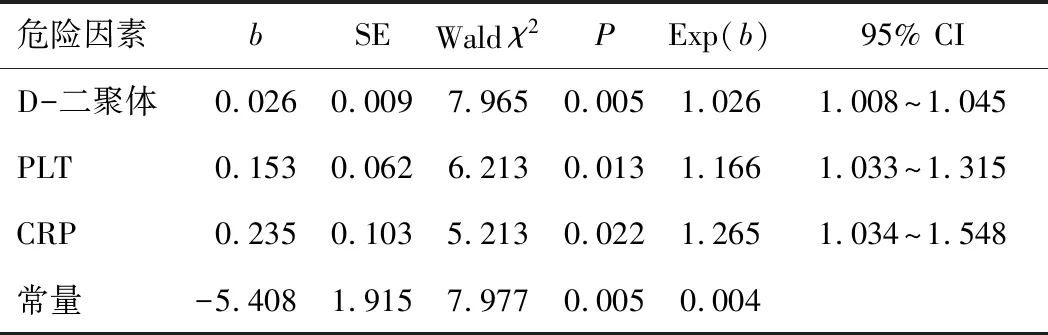
表2 IBD合并血栓的危险因素的logistic回归分析
注:PLT—血小板;CRP—C反应蛋白。
2.3 IBD合并血栓患者的临床特点
2.3.1临床表现 在42例IBD合并血栓患者中,IBD常表现为腹泻(37例,88.0%)、血便(30例,71.4%)和腹痛(28例,66.7%),其他症状如腹胀、发热、肠梗阻、肠穿孔共9例(21.4%)。合并血栓后,根据血栓部位不同,表现为胸闷2例(4.8%),单侧下肢疼痛、肿胀10例(23.8%),肢体麻木、嗜睡、乏力4例(9.5%),肝酶升高、腹水1例(2.4%),心慌、心前区不适3例(7.1%),休克2例(4.8%)。有20例(47.6%)患者无明显血栓栓塞表现,因临床症状突然加重,经血管彩超、CTA等检查发现血栓。
2.3.2检查及治疗 通过增强CT及内镜检查发现肠穿孔2例,肠壁增厚28例,肠腔狭窄15例,直肠病变27例,假息肉8例。在3例CD患者中,2例病变部位为A3L3B2,1例为A3L3B1。在39例UC患者中,4例E1,10例E2,27例E3。应用美沙拉嗪治疗32例(76.2%),糖皮质激素15例(35.7%),硫嘌呤类2例(4.8%),手术7例(16.7%)。
2.3.3血栓部位及血栓的治疗 在42例IBD合并血栓患者中,静脉血栓18例(42.9%),动脉血栓20例(47.6%),肺栓塞合并深静脉血栓1例(2.4%),脑梗死合并深静脉血栓1例(2.4%),弥散性血管内凝血(disseminated intravascular coagulation,DIC)2例(4.8%)。静脉血栓包括下肢深静脉血栓16例(38.1%),门静脉血栓1例(2.4%),肺栓塞1例(2.4%)。动脉血栓包括脑梗死16例(38.1%),心肌梗死3例(7.1%),肠系膜上动脉1例(2.4%)。抗凝治疗(低分子肝素、华法林、利伐沙班)12例(28.6%)。采取紧急手术复通治疗5例(11.9%),包括因脑梗死溶栓治疗2例,因下肢深静脉血栓行下腔静脉血栓滤网植入1例,因门脉血栓行下腔静脉造瘘并门体分流道成形术1例,因心肌梗死行冠状动脉旁路移植术1例。保守治疗25例(59.5%)。
2.4 转归42例IBD合并血栓的患者:死亡2例,其中1例患者因手术后出现感染性休克合并DIC而死亡,另1例内科治疗无效死于休克合并DIC;病情加重3例;好转37例。
3 讨论
早在1936年,Bargen等[5]首次报道了IBD与静脉血栓可能存在一定的联系。2008年美国胸科医师学会明确提出IBD是静脉血栓栓塞症(venous thromboembolism,VTE)的危险因素[6]。有研究表明,IBD患者发生VTE的风险升高3倍[7]。
IBD患者发生血栓的机制目前尚不明确。CRP在产生中可减少内皮细胞产生一氧化氮,导致内皮异常[8]。IBD活动期往往伴随PLT数量上升,PLT活性增强,刺激血小板-白细胞聚集物的生成,使患者易发生血栓[9]。激素通过促进多种凝血因子(凝血因子Ⅶ、Ⅷ和Ⅺ)和纤溶酶原激活物抑制剂-1(PAI-1)的合成和分泌,直接激活凝血系统并抑制纤溶系统,增加了IBD患者发生血栓的风险[10]。多项研究表明D-二聚体和PLT升高可被作为IBD活动的标志[10-11]。本研究结果显示,D-二聚体、PLT与CRP水平升高是IBD合并血栓的独立危险因素。
IBD患者合并VTE的常见部位以下肢深静脉为主,其次为肺动脉、内脏静脉等。下肢深静脉血栓及肺栓塞的临床表现较明显。内脏静脉血栓的症状隐匿,有时仅表现为腹痛、肝酶升高、腹水、肾区叩痛、上肢水肿等,易被忽略。在本研究中,下肢深静脉血栓占静脉血栓的88.9%,动脉血栓20例(47.6%)。与既往研究结果[12]相比,动脉血栓的发病率偏高,可能与近些年心脑血管相关疾病增多有关。14例脑梗塞患者仅表现为乏力、嗜睡等,1例肠系膜上动脉血栓患者表现为腹痛、血便加重,1例门脉血栓表现为肝酶升高、腹胀、少量腹水,这些临床症状易被忽略,增加了临床诊断的难度。IBD合并血栓的治疗难度大。对无严重出血的中重度IBD住院患者,建议预防性使用肝素类抗凝药物[3]。
总之,D-二聚体、PLT与CRP水平升高是IBD合并血栓的独立危险因素。当IBD患者出现腹痛加重、肝酶升高、下肢疼痛肿胀或血便加重等情况,且合并PLT、CRP或D-二聚体升高,需筛查血栓栓塞,以便及时发现血栓,早期进行治疗。
