硼掺杂多孔碳球吸附Cd(Ⅱ)的热力学和动力学
2020-04-10郭世浩邓弘勇张继伟马路路刘帅霞
陈 锋, 郭世浩, 刘 佩, 邓弘勇, 张继伟, 马路路, 马 培, 刘帅霞
(河南工程学院资源与环境学院, 郑州 451191)
镉(Cd)是一种在自然界中以化合物状态存在且对环境有极大污染的重金属,可通过食物链进入人体,引起慢性中毒,甚至导致死亡。因此,在金属Cd(Ⅱ)被释放到环境中之前,有必要对其进行去除。目前,金属Cd(Ⅱ)的处理方法主要有化学沉淀法、离子交换法、吸附法等。其中,吸附法因具有运行费用低、处理效果好、易解吸等优点,倍受中外科学家的青睐,在重金属废水处理方面发挥着不可或缺的作用[1]。
吸附法的关键在于吸附剂的选择,而吸附剂种类繁多。其中多孔碳球可分为微孔碳球、介孔碳球和分级孔碳球等,具有表面官能团丰富、比表面积大、孔径结构可调、热稳定性好及密度低等优点,可作为吸附分离过程的吸附剂和催化过程的载体。例如,周璇[1]利用葡萄糖一步水热法制备出碳微球,再经铁盐改性后得到磁性碳微球,用于废水中Cd(Ⅱ)的吸附,吸附效果较好。此外,有研究表明杂原子掺杂可进一步提升多孔碳材料各方面的性能。例如,焦玉春[2]分别以尿素和有机胺为氮源制备出氮掺杂多孔碳球,并对CO2进行吸附,结果表明氮掺杂不仅为CO2提供了更多的吸附位点,还具有一定的扩孔作用,进一步提升了CO2的吸附量。
目前,多孔碳球的制备方法有模板法、气相沉积法、热解法、和水热法等。其中水热法具有操作流程简单,可利用碳源来源广泛,不需要强酸强碱,在较低温度下就能进行的优点,近年来被人们大量采用。因此,以蔗糖为碳源、硼酸为掺杂剂,利用水热法和化学活化法制备出硼掺杂多孔碳球(boron-doped porous carbon spheres,B-PCS),利用B-PCS对废水中的Cd(Ⅱ)进行吸附研究,随后采用动力学、热力学以及等温线方程对B-PCS吸附Cd(Ⅱ)的过程及机理进行探讨。
1 实验部分
1.1 试剂与仪器
试剂:蔗糖、硼酸、硝酸、氯化镉、氯化锌、乙醇,所有试剂均为分析纯,实验用水均为超纯水。
仪器:电子天平(FA2004B)、pH测定仪(PHS-3C)、恒温振荡培养箱(EMS-4E)、电热恒温干燥箱(DHG202-0)、多点磁力搅拌器(CJB-5-5D)、循环水式多用真空泵(SHZ-D)、KTF-1700管式气氛炉(KTF-6-17)、原子吸收分光光度计(AA-6880)。
1.2 PCS和B-PCS的制备
准确称量6.4 g蔗糖和6.4 g硼酸溶于80 mL超纯水中,磁力搅拌混合均匀后置于100 mL以聚四氟乙烯为内衬的水热罐中密封,放入190 ℃烘箱中反应12 h,抽滤洗涤,80 ℃干燥6 h后得到黑色固体。按照1∶1的质量比称取所得黑色固体与氯化锌,加入无水乙醇与去离子水混合均匀,静置12 h后105 ℃烘干,置于管式气氛炉内,以5 ℃·min-1的升温速率升温至900 ℃活化1 h,待其冷却后取出,加入稀硝酸溶液,充分搅拌后过滤洗涤至中性,105 ℃烘干,即得到硼掺杂多孔碳球。在相同的实验条件下,利用上述方法也制备了未加入硼酸掺杂的多孔碳球(porous carbon spheres,PCS)。
1.3 不同吸附剂的吸附对比实验
分别称取20 mg的PCS和B-PCS,置于100 mL锥形瓶中,分别加入50 mL浓度为10 mg·L-1的Cd(Ⅱ)溶液,将其密封,置于温度为298 K,转速为130 r·min-1的恒温振荡培养箱内,振荡吸附24 h,待振荡吸附完成后取出过滤,采用火焰原子吸收光谱法测定吸光度,并根据镉标准曲线计算出浓度。并由式(1)、式(2)计算出吸附率和吸附量。
吸附率:
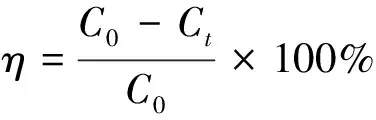
(1)
吸附量:
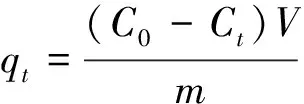
(2)
式中:C0和Ct分别为吸附前和吸附时间t后溶液中Cd(Ⅱ)的浓度,mg·L-1;η为Cd(Ⅱ)吸附率,%;qt为t时刻吸附量,mg·g-1;V为Cd(Ⅱ)溶液的体积,L;m为吸附剂的质量,g。
1.4 B-PCS吸附Cd(Ⅱ)的动力学实验
称取若干份20 mg B-PCS,置于100 mL锥形瓶中,分别加入50 mL浓度为10 mg·L-1的Cd(Ⅱ)溶液,密封后置于温度为298 K,转速为130 r·min-1的恒温振荡培养箱内,振荡吸附10~720 min,过滤,计算吸附量。采用动力学模型对实验数据进行拟合。
1.5 B-PCS吸附Cd(Ⅱ)的热力学实验
称取20 mg的B-PCS,置于100 mL锥形瓶中,分别加入50 mL浓度为10~110 mg·L-1的Cd(Ⅱ)溶液,密封,分别置于温度为298、308、318 K,转速为130 r·min-1的恒温振荡培养箱内振荡吸附12 h,计算吸附量。采用等温线模型对实验数据进行拟合。
2 结果与讨论
2.1 表征分析
2.1.1 掺杂前后扫描电镜对比
图1为未掺杂的PCS和掺杂硼的B-PCS的扫描电镜(SEM)图,可以看出,无论掺杂前后,样品均为内部无杂质的实心球形碳材料,其中未掺杂的碳球表面光滑,粒径较为均一,存在不完全成型和团聚的情况。而掺杂硼元素后的碳球表面光滑度较掺杂前有所下降,表面存在着一些缺陷,这可能是由于硼掺杂和氯化锌活化造成的;且球颗粒直径有所增大,为1~6 μm,团聚现象消失,碳球均匀分散。由能谱仪(EDS)测得B-PCS中碳、硼、和氧的重量百分比分别为90.43%、6.46%和3.11%,说明硼元素成功掺杂到B-PCS样品中,且B-PCS表面存在着丰富的含氧和含硼官能团[2-3]。

图1 碳材料的扫描电镜图Fig.1 The SEM images of carbon materials
2.1.2 掺杂前后XRD对比
图2为PCS和B-PCS的X射线衍射(XRD)图。由图2可以看出,PCS和B-PCS均在26°以及44°左右出现两个明显的大包特征峰,分别对应着石墨材料的(002)和(100)晶面[4],说明实验制备出的PCS和B-PCS材料均为具有一定石墨化结构的无定型碳。
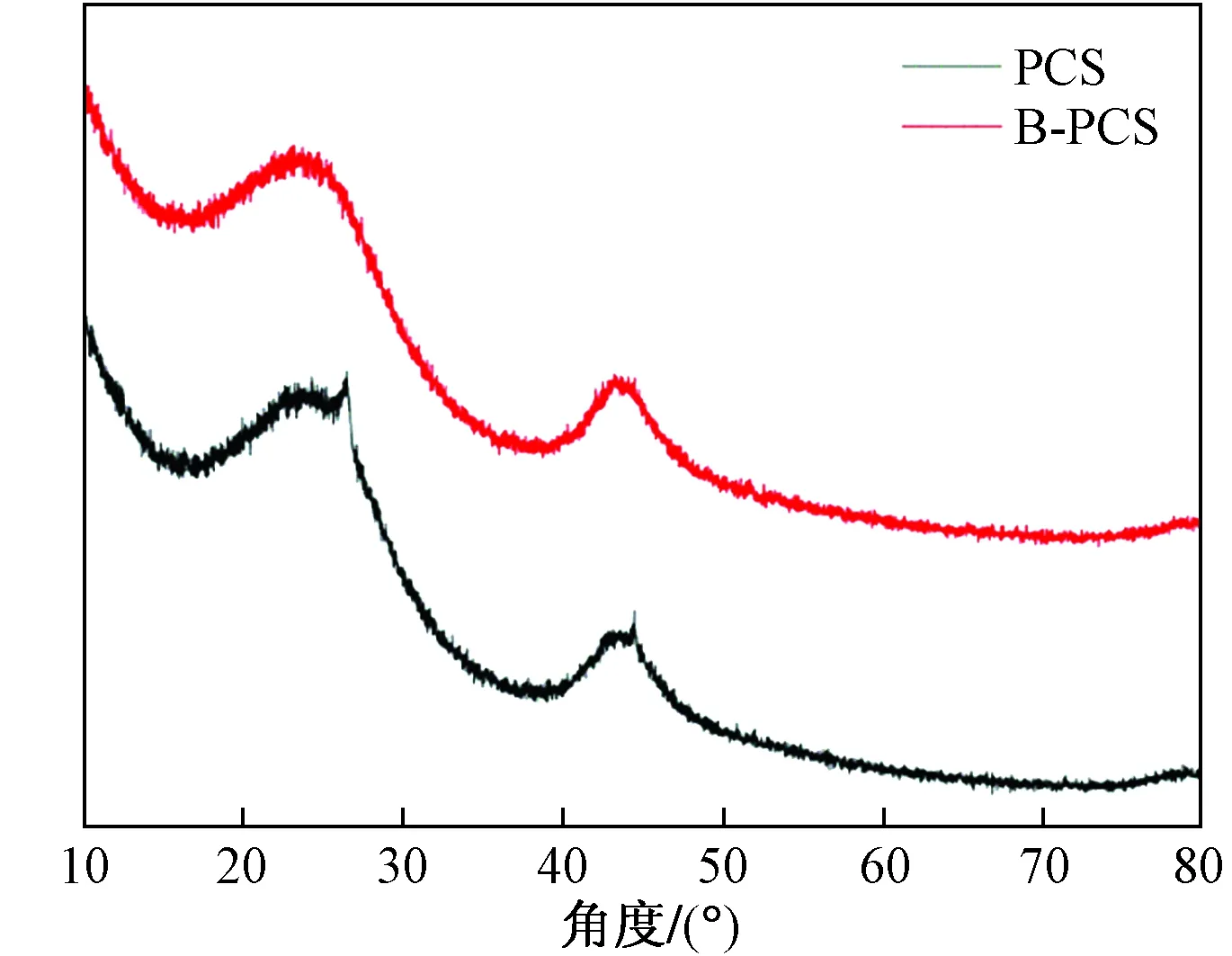
图2 PCS和B-PCS的XRD对比图Fig.2 The XRD patterns of PCS and B-PCS
2.1.3 红外光谱分析
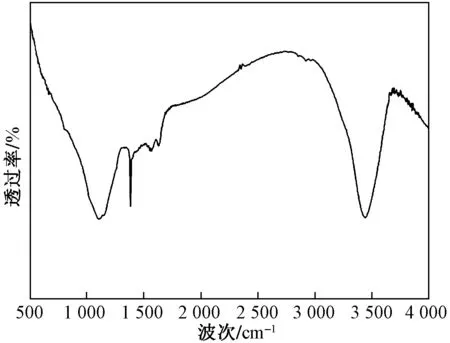
图3 B-PCS的傅里叶红外光谱(FTIR)Fig.3 The FTIR spectrum of B-PCS

2.1.4 比表面积(BET)分析
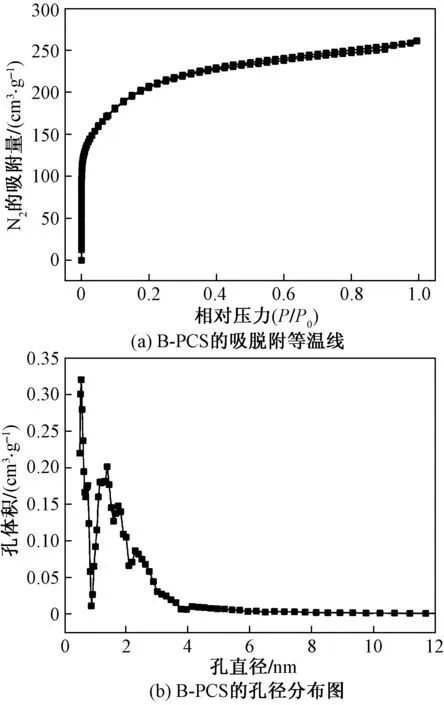
图4 B-PCS的比表面积分析Fig.4 The specific surface area analysis of B-PCS
图4(a)为B-PCS的N2吸脱附等温线,图4(b)为孔径分布曲线。根据IUPAC命名法,B-PCS的吸脱附等温线属于Ⅳ型,当相对压力P/P0=0~0.2时,N2吸附量明显上升,说明B-PCS中存在着微孔;当相对压力P/P0>0.6时,N2气体在孔隙内凝聚,出现了不太明显的滞后现象[6-7],说明B-PCS中还存在着少量的介孔。由BET方法计算得出B-PCS的比表面积达到672.2 m2·g-1,孔体积达到0.356 cm3·g-1。运用DFT方法拟合出B-PCS的孔径分布图,可以看出,B-PCS在0~2 nm之间有两个比较强烈的峰,在2~5 nm之间有一个明显的峰,表明其为典型的微介孔结构,这与吸脱附等温线的结果相吻合。B-PCS典型的微介孔结构可以提供很多的活性吸附位点,有利于对废水中Cd(Ⅱ)的吸附[8]。
2.2 PCS和B-PCS对Cd(Ⅱ)的吸附效果对比
为了对比PCS和B-PCS的吸附效果,采用控制变量法,用未掺杂的PCS和掺杂硼元素的B-PCS对废水中的Cd(Ⅱ)进行静态吸附实验,结果如图5所示,PCS和B-PCS对废水中的Cd(Ⅱ)的吸附率分别为28.5%和56.0%。掺杂硼元素的B-PCS的吸附效果明显高于未掺杂的PCS。分析原因为,一方面掺杂硼元素成功引入新的缺陷,增加了B-PCS表面的官能团,有利于进行化学吸附[5];另一方面B-PCS大的比表面积和独有的微介孔结构为Cd(Ⅱ)的吸附提供了更多的活性位点[8]。两者协同作用,极大地提高了B-PCS对Cd(Ⅱ)的吸附性能。
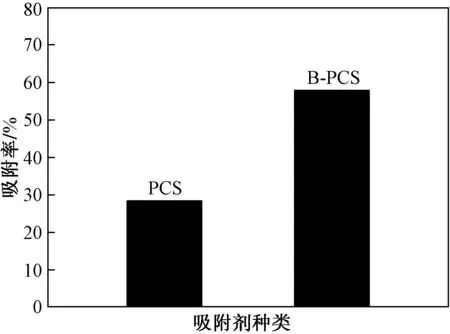
图5 PCS和B-PCS的吸附效果对比Fig.5 The adsorption effect comparison of PCS and B-PCS
2.3 B-PCS对Cd(Ⅱ)的吸附动力学
为了研究B-PCS对Cd(Ⅱ)的吸附动力学特性,更好地了解吸附过程,利用B-PCS对Cd(Ⅱ)溶液进行吸附,计算出吸附量后,基于吸附平衡数据,采用以下模型对实验数据进行拟合[9-11]。
准一级:
ln(qe-qt)=lnqe-k1t
(3)
准二级:
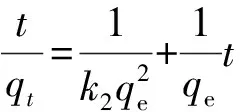
(4)
内扩散:
qt=kpt1/2+C
(5)
Boyd模型:
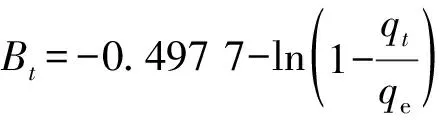
(6)
式中:t为吸附时间,min;k1为准一级动力学常数,min-1;k2为准二级动力学常数, g·(mg·min)-1;kp为粒子内扩散速率常数,mg·(g·min)-1/2;C涉及边界层厚度,界面越大,边界层效应越大;qe为平衡吸附量,mg·g-1。
如图6所示,分别以t、t1/2为横坐标,ln(qe-qt)、t/qt、qt、Bt为纵坐标作图。可看出,准二级动力学模型拟合的数据可以呈现较好的线性关系。对实验数据进行总结,见表1。从表1可以看出,准一级模型拟合的理论吸附量与实验吸附量相差较大,而准二级模型拟合的理论吸附量与实验吸附量相差无几,从相关系数R2也可以看出,准二级的相关系数更接近于1,说明用准二级动力学模型拟合B-PCS对Cd(Ⅱ)的吸附行为是可行的,吸附过程中存在电子的转移,化学吸附起主要作用,其中官能团吸附是B-PCS吸附Cd(Ⅱ)的控速步骤[12]。
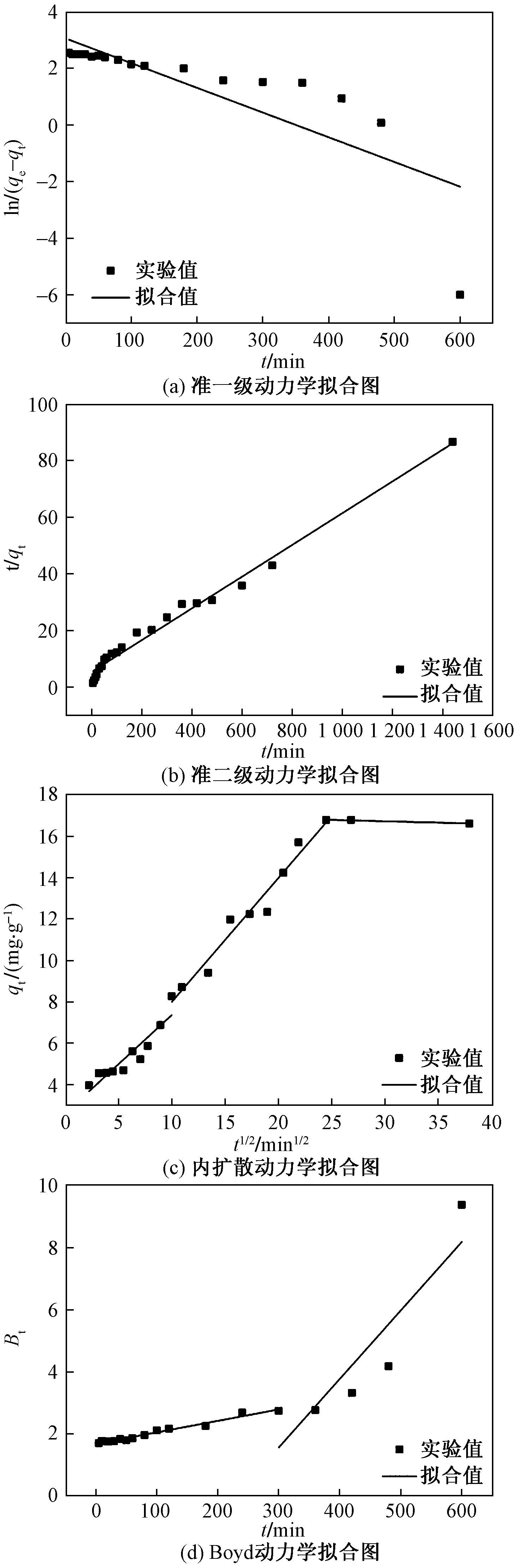
图6 B-PCS对Cd(Ⅱ)的动力学拟合图Fig.6 The dynamics fitting diagrams of Cd(Ⅱ) by B-PCS
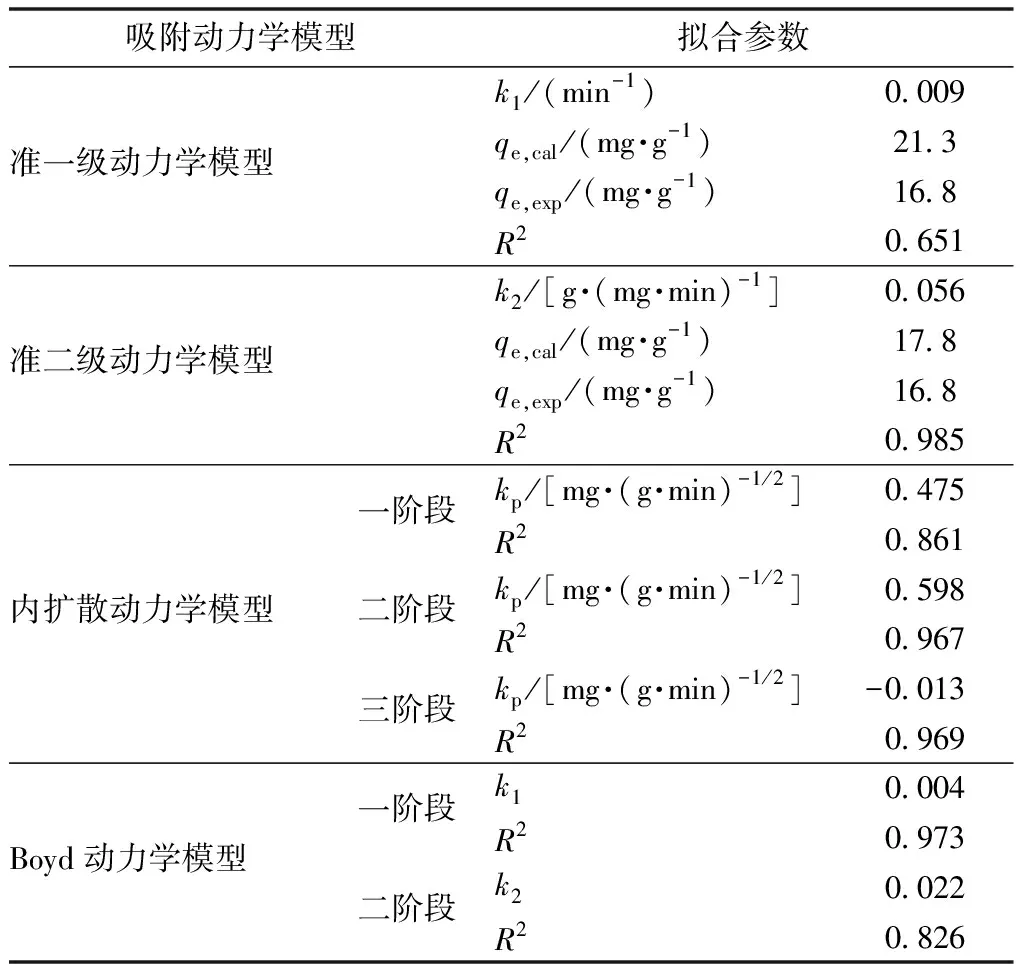
表1 B-PCS对Cd(Ⅱ)的吸附动力学参数Table 1 Adsorption kinetic parameters ofCd(Ⅱ) by B-PCS
从图6(c)可以看出,第二段曲线斜率高于第一段曲线斜率,原因可能是刚开始外表面扩散与外表面吸附起主导作用,第二阶段的时候粒内扩散和外表面扩散与吸附同时作用。在12 h后,曲线斜率趋于平缓,可能是吸附达到平衡之后,外表面扩散与吸附达到饱和,不再进行吸附。图形呈现三段直线,说明在Cd(Ⅱ)的吸附过程中存在粒子内扩散,但三段直线均不经过原点,这说明粒子内扩散不是控制吸附速率的唯一因素[9]。图6(d)更加验证了吸附过程不只是粒子内扩散控制,还有外表面扩散和外表面吸附控制[10]。
2.4 B-PCS对Cd(Ⅱ)的吸附等温线
为了更好地理解B-PCS对Cd(Ⅱ)的吸附热力学,在不同温度条件下(298~318 K),利用B-PCS吸附不同浓度的Cd(Ⅱ)溶液,计算平衡吸附量,基于吸附平衡数据,采用以下模型对实验数据进行拟合[10],结果见图7、表2。
Langmuir模型:
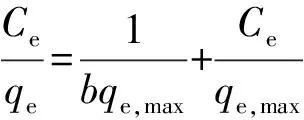
(7)
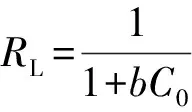
(8)
Freundlich模型:

(9)
D-R模型:
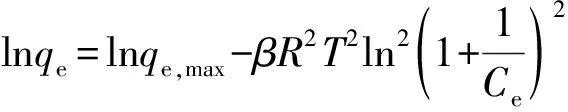
(10)
式中:qe,max为理论最大吸附量,mg·g-1;b为Langmuir吸附平衡常数;RL为常数;KF为待定系数;β为平均吸附自由能系数;R为标准摩尔常数,8.314×10-3kJ·(mol·K)-1;T为反应温度,K;Ce为初始浓度,mg·L-1。
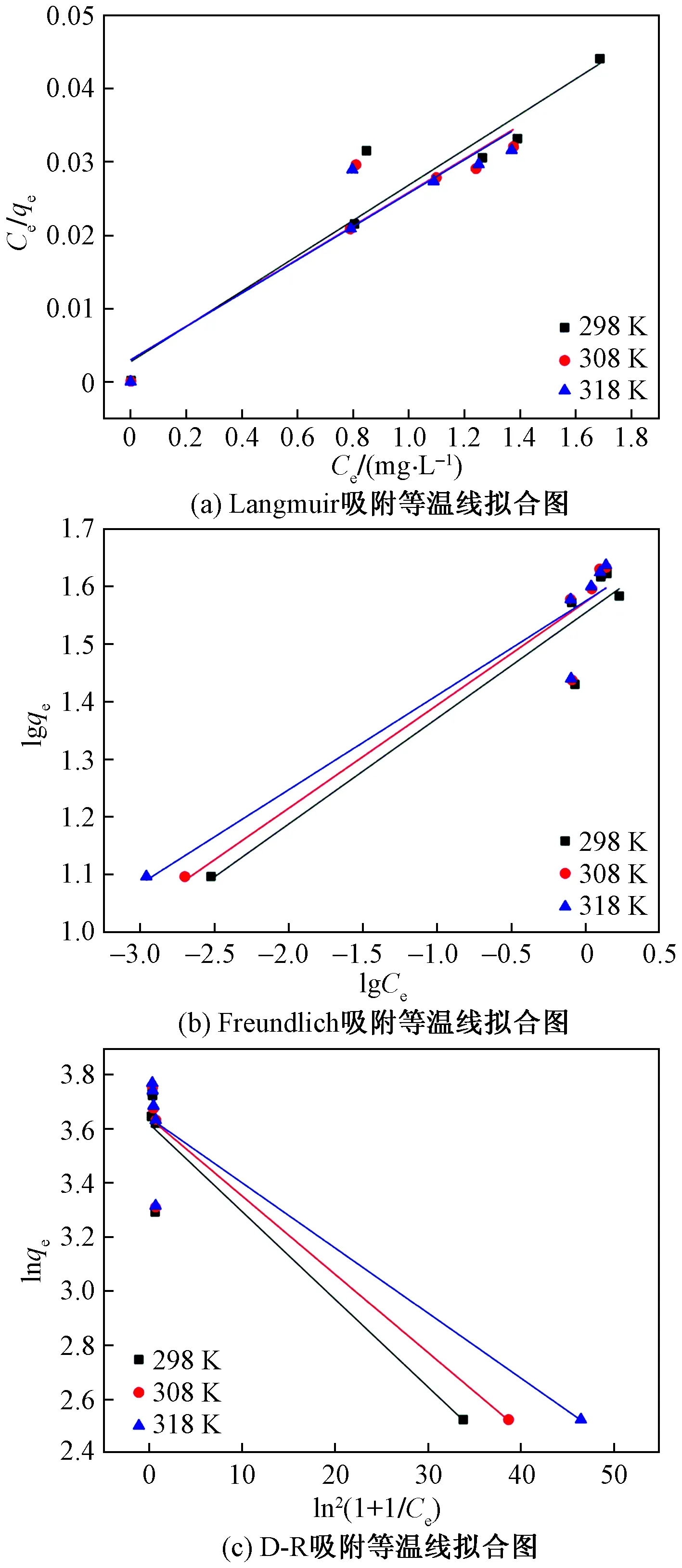
图7 B-PCS对Cd(Ⅱ)的吸附等温线拟合图Fig.7 The adsorption isotherm fitting diagrams ofCd(Ⅱ) by B-PCS
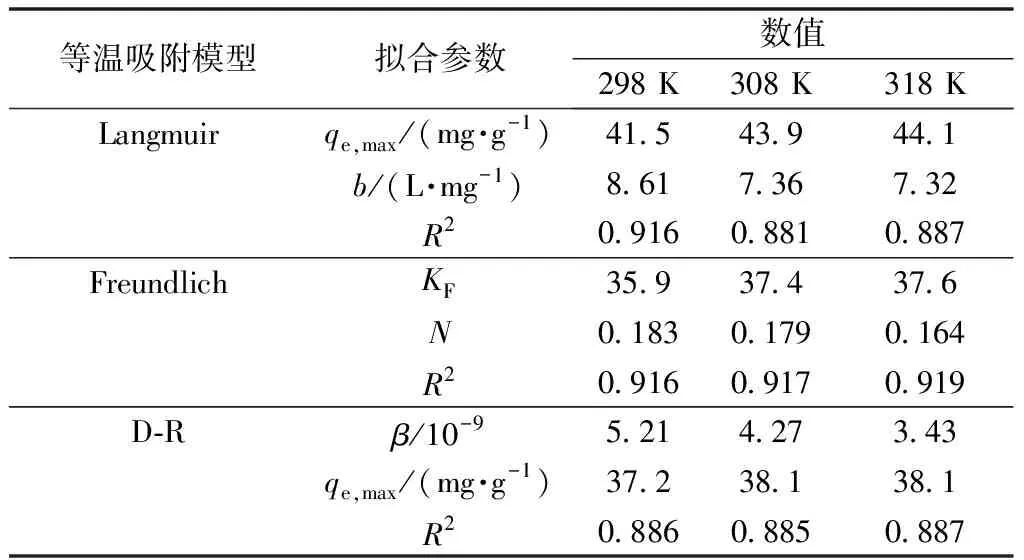
表2 B-PCS对Cd(Ⅱ)的吸附等温线参数Table 2 Adsorption isotherm parameters ofCd(Ⅱ) by B-PCS
如图7所示,分别以Ce、lgCe、ln2(1+1/Ce)为横坐标,Ce/qe、 lgqe、lnqe为纵坐标作图。拟合的实验数据结果如表2所示。由表2可以看出,Langmuir型、Freundlich型、D-R型等温吸附模型都可以准确地拟合B-PCS对Cd(Ⅱ)的等温吸附过程,比较R2的值,可知Freundlich型的相关系数都在0.91以上,相关性较好,按照模型特点进行分析,可知B-PCS对Cd(Ⅱ)的吸附发生在异构的表面,且吸附能力与Cd(Ⅱ)平衡时的浓度无关[11]。由Langmuir模型计算得出,298 K下,B-PCS对Cd(Ⅱ)的最大吸附量可达到41.5 mg·g-1。经计算,实验的RL在0.011~0.013之间,均大于0小于1,说明B-PCS对Cd(Ⅱ)的吸附是有利吸附[13]。
2.5 B-PCS对Cd(Ⅱ)的吸附热力学
为了研究热力学参数,分别在298、308、318 K的温度下用B-PCS对Cd(Ⅱ)溶液进行吸附实验,并对吸附平衡常数(Kd)、吉布斯自由能(ΔG0)、焓变(ΔH0)、熵变(ΔS0)进行计算[9]:
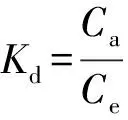
(11)
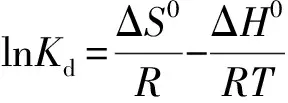
(12)
ΔG=-RTlnKd
(13)
式中:T为绝对温度,K;R为理想气体常数,取R=8.314 J·(mol·K)-1;Ca为吸附剂所吸附Cd(Ⅱ)的浓度,mg·L-1。
根据式(12),ΔH0和ΔS0分别可由1/T对lnKd作图的斜率和截距(图8)计算得到,计算结果如表3所示。
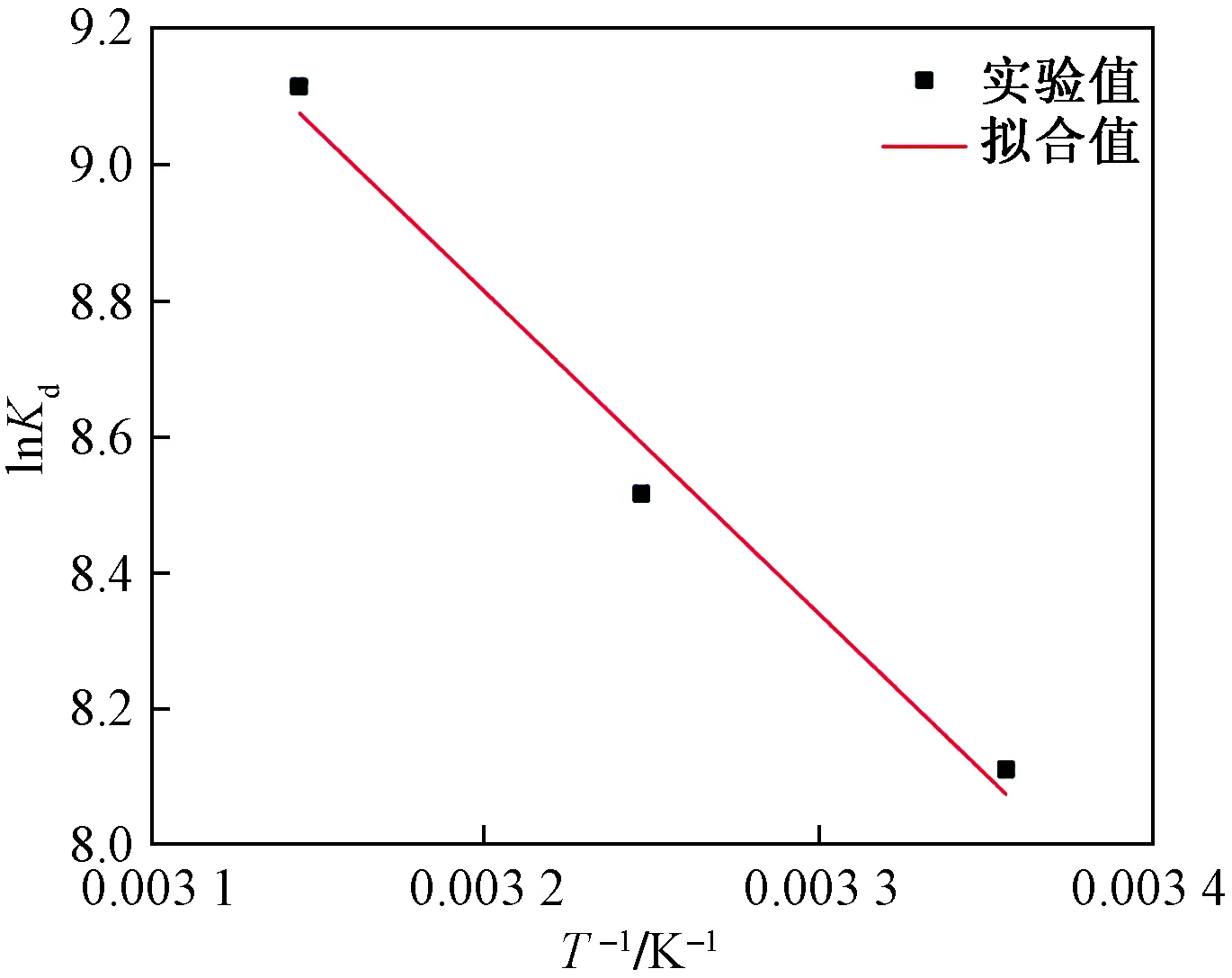
图8 B-PCS对Cd(Ⅱ)的吸附热力学Fig.8 The thermodynamic curve for Cd(Ⅱ)adsorption by B-PCS

表3 不同温度下的热力学数据Table 3 The thermodynamic data at different temperature
由表3数据可知,ΔG0为负值,说明吸附过程是自发的、可行的。ΔH0为正值,说明吸附是吸热过程,温度升高有利于反应的进行,这与吸附等温线相符合,吸附过程的标准焓变为正值,主要是由于溶解于水的Cd2+离子由水溶液向B-PCS表面运动需要克服传质阻力,而克服传质阻力所需要的能量大于阳离子与吸附剂表面结合所放出的能量。ΔS0为正值说明反应增加了固液两相界面的无序度[9]。
3 结论
以蔗糖为碳源,硼酸为掺杂剂,采用水热法和化学活化法制备出B-PCS,并研究其对废水中Cd(Ⅱ)的吸附动力学和热力学,得出如下结论。

(2)准二级动力学模型证实B-PCS对Cd(Ⅱ)的吸附为化学吸附控制过程,并且过程中存在电子的转移,内扩散和Boyd模型表明粒子内扩散不是控制吸附速率的唯一因素。
(3)Freundlich模型可以很好地拟合不同温度下的吸附过程,且吸附发生在异构表面。B-PCS对Cd(Ⅱ)的最大吸附量为41.5 mg·g-1,0 (4)ΔG0范围为-20.1~-24.1 kJ·mol-1、ΔH0=39.4 kJ· mol-1、ΔS0=199.5 J·(mol·K)-1,表明B-PCS吸附废水中的Cd(Ⅱ)为自发、吸热、熵增的过程。
