高效液相色谱法测定烯丙孕素口服液中烯丙孕素的含量
2020-04-08姜淋洁崔志刚娄艳华甄盼盼程雪娇
姜淋洁,崔志刚,杨 雪,娄艳华,甄盼盼,程雪娇
(天津市中升挑战生物科技有限公司,天津300080)
烯丙孕素(Altrenogest)是一种人工合成的甾类促孕激素,属于19-去甲睾酮类化合物[1-2],它可凭借其脂溶性穿透靶细胞,与特定受体结合[3-5]。烯丙孕素已被欧盟和美国批准用于母猪和母马的同步发情,由其制成的口服液已成功上市。在我国兽医临床中,烯丙孕素口服液可用于母猪的同期发情、促进乏情母猪的发情[6-8]。但对于烯丙孕素口服液的质量控制,目前还没有相关的研究报道,本研究建立烯丙孕素口服液中烯丙孕素的含量液相方法检测方法,为烯丙孕素口服液的质量控制研究提供技术支撑。中国兽药典中性激素类药物如丙酸睾酮注射液采用乙醚溶解、甲醇提取后用高效液相色谱法测定丙酸睾酮的含量[9],操作步骤繁琐且对浪费大量有机溶剂。本研究对前处理方法进行改进,采用高效液相色谱法对烯丙孕素进行定性和定量检测,方法经济快速,可以满足日常检测需求。
1 材料与方法
1.1 仪器 安捷伦1260 II 高效液相色谱仪包括包括G7111A四元泵,G7129A自动进样器,AT-330柱温箱,G7115A DAD检测器,C.01.07 SR2(255)色谱工作站,美国安捷伦科技有限公司;ES225SM-DR电子天平,普利赛斯仪器有限公司;超声波清洗器,昆山仪器有限公司;真空泵,ASL仪器有限公司。
1.2 药品与试剂 烯丙孕素对照品(批号1708001,含量99.95%,天津市中升挑战生物科技有限公司),烯丙孕素口服液(批号:1709001,天津市中升挑战生物科技有限公司),正己烷(色谱纯,西陇化工科技有限公司),异丙醇(色谱纯,西陇化工科技有限公司)。
1.3 色谱条件 以氰基键合硅烷为填充剂的Zorbax CN色谱柱(250mm×4.6mm,5μm);以正己烷-异丙醇(98∶2)为流动相;检测波长为235 nm;流速1.0 mL/min,进样量10 μL。
2 结果与分析
2.1 样品溶液制备 精密称取烯丙孕素口服液适量(约相当于烯丙孕素12.5 mg),置25 mL棕色量瓶中,加异丙醇5 mL,超声3 min使溶解,加正己烷稀释至刻度,摇匀,作为供试品溶液。另取烯丙孕素对照品约25.0 mg,精密称定,置50 mL棕色量瓶中,加异丙醇5 mL溶解后,用正己烷稀释至刻度,摇匀,作为对照品溶液。
2.2 系统适应性试验 按照2.1项方法操作,配制1份对照品溶液,连续进样5次。结果显示,主峰峰面积的相对标准偏差为0.21%,主峰保留时间的相对标准偏差为0.60%,主峰的理论塔板数都在15000以上。结果见表1,色谱图见图1。系统适应性试验表明该色谱条件可以满足分析要求。
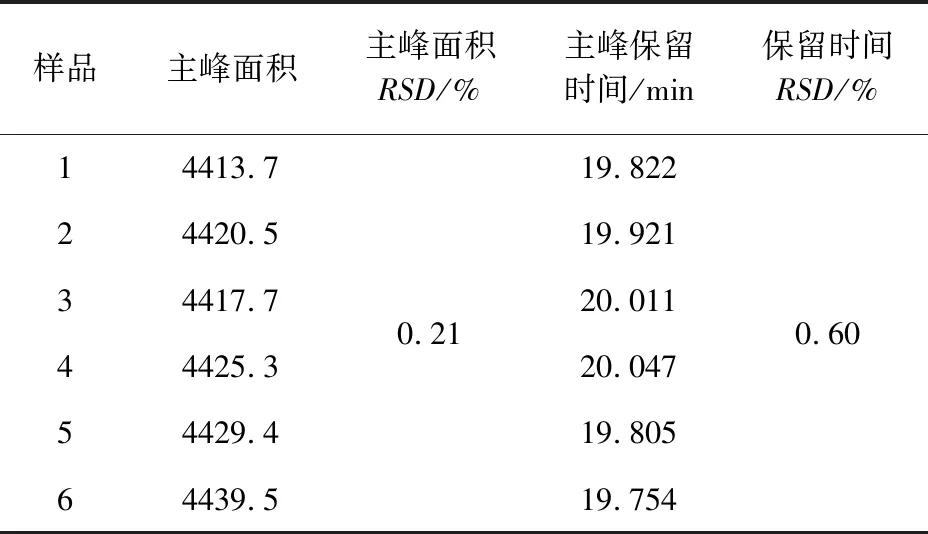
表1 系统适应性试验结果
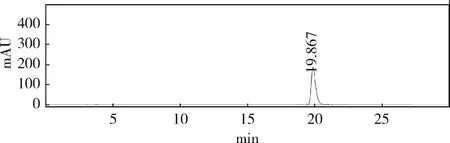
图1 烯丙孕素对照品色谱图
2.3 专属性试验 按照烯丙孕素口服液处方量配制空白制剂样品,按2.1项中制备方法制成阴性对照溶液;另取烯丙孕素口服液按2.1项中制备方法制成供试品溶液;另称取适量烯丙孕素对照品,按2.1项中制备方法制成对照品溶液。按1.3项的色谱条件分别进阴性对照、供试品溶液和对照品溶液,色谱图见图2,结果表明辅料成分不干扰样品中烯丙孕素的测定。

图2 专属性试验色谱图(A、B、C 分别为对照品、供试品、阴性对照)
2.4 线性关系考察 分别精密称取适量烯丙孕素对照品至50 mL容量瓶中,制成0.401、0.451、0.503、0.551、0.601 mg/mL的对照品溶液,按照1.3项色谱条件进样记录峰面积,以峰面积对进样浓度作线性回归,方程为y=8551.6x+101.78 (R=0.9998,n=5),表明烯丙孕素对照品溶液浓度在0.401~0.601 mg/mL范围内时与峰面积呈良好的线性关系。
2.5 回收率试验 按照烯丙孕素口服液处方分别配制9份50 mL空白制剂,然后加入主药烯丙孕素处方量的80%(0.16 g)、100%(0.2 g)、120%(0.25 g)(每个浓度各3份)制备9份回收率样品溶液,按2.1项中制备方法制成供试品溶液;另称取适量烯丙孕素对照品,按2.1项中制备方法制成对照品溶液。按照1.3项色谱条件进样,记录色谱图。计算样品的回收率,结果见表2。
2.6 精密度试验 按照2.1项方法操作,配制6份相同浓度(0.5 mg/mL)的烯丙孕素口服液样品溶液和1份烯丙孕素对照品溶液。按照1.3项色谱条件进样,记录色谱图见图3。计算样品中烯丙孕素的含量,结果见表3。
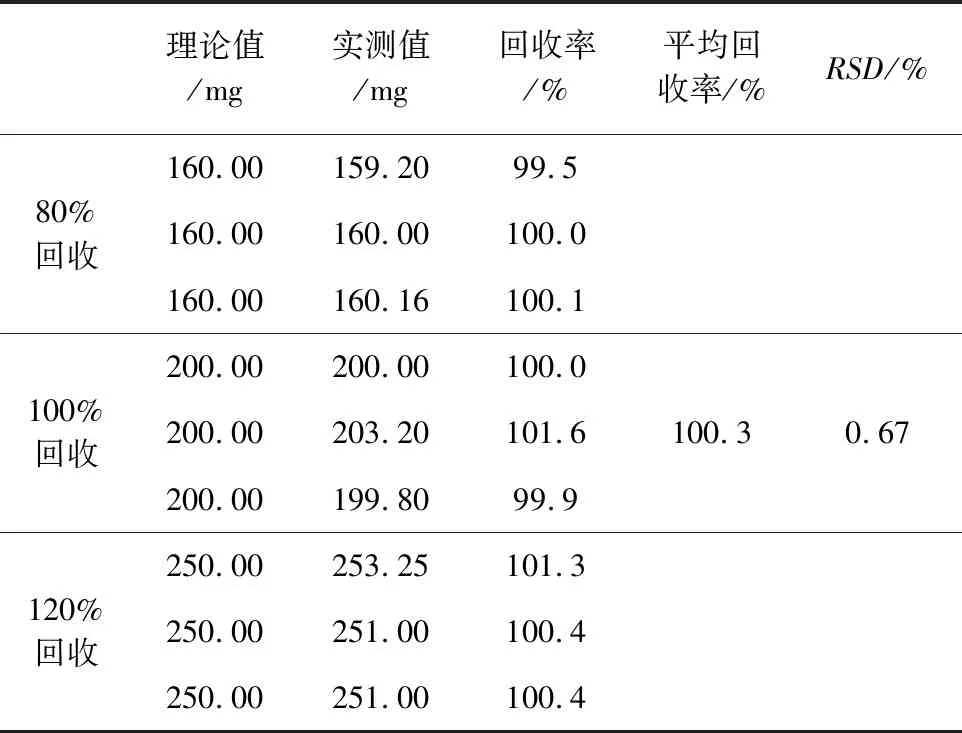
表2 烯丙孕素口服液中烯丙孕素的回收率(%)
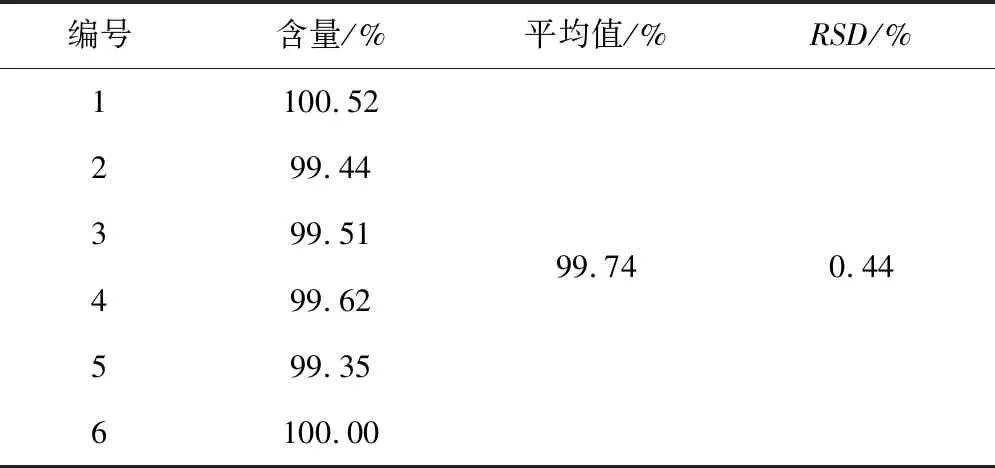
表3 烯丙孕素口服液含量测定精密度试验结果
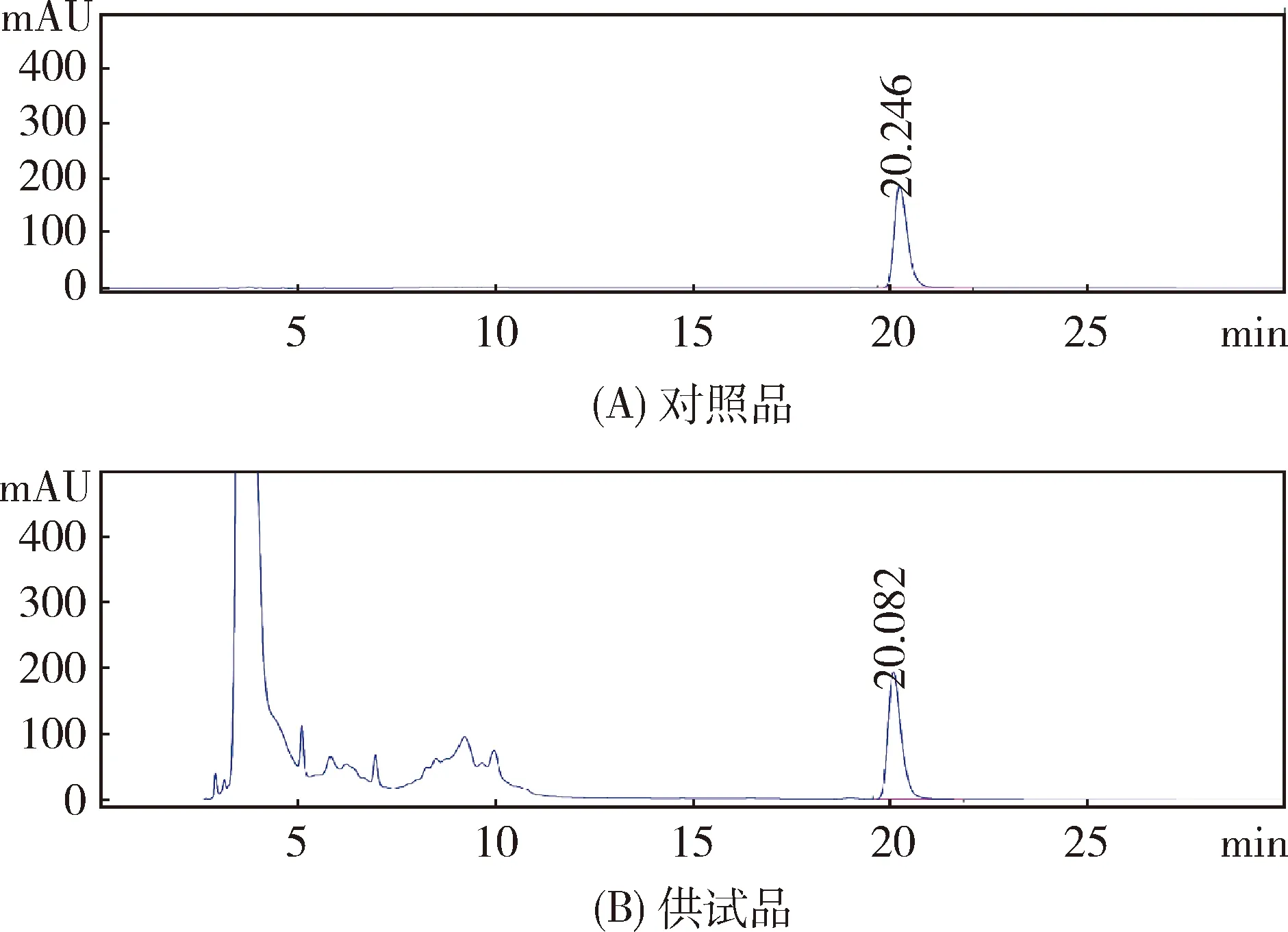
图3 精密度试验色谱图(A、B 分别为对照品、供试品)
2.7 定量限试验 取烯丙孕素对照品约25 mg适量置于50 mL容量瓶中,按2.2项方法操作,得到浓度约为0.5 mg/mL的溶液,然后用正己烷逐步稀释至浓度为804.9 ng/mL,连续测试6次,信噪比平均为10.2,因此,烯丙孕素定量限为804.9 ng/mL。
3 讨论与结论
关于烯丙孕素在动物组织样品中的残留检测国内外有很多报道,Elin Beckman等[10]利用液质联用技术测定烯丙孕素和它的代谢物在马尿液中的残留水平。Martina Rejtharova等报道了利用液质联用技术测定烯丙孕素等六种孕激素在肾脏脂肪中的残留水平[11]。Dan Zhang等利用液质联用技术测定烯丙孕素等在猪肉中的残留水平[12]。Machnik等利用液质联用技术测定烯丙孕素在马血浆和马尿液中残留水平[13]。康海宁等建立了河豚鱼、鳗鱼及烤鳗中烯丙孕素与氯地孕酮残留的同时测定的超高效液相色谱-串联质谱法[14]。林黎明等建立了进出口动物源性食品中孕激素类药物残留量的高效液相色谱串联质谱检测方法[15]。邵兵等建立了动物源食品中激素多残留检测方法液相色谱-质谱/质谱法[16]。贺利民等建立了动物源食品中11种激素残留检测液相色谱-串联质谱法[17]。这些研究者都是将烯丙孕素从组织样品中提取出来,然后运用液质等手段对烯丙孕素进行定量测定,操作过程繁琐且对设备要求比较高。本文建立的烯丙孕素口服液中烯丙孕素的含量测定方法,着重对前处理方法和色谱系统进行改进,以期为企业实际生产中烯丙孕素制剂的质量控制提供依据。
3.1 样品前处理方法的选择 烯丙孕素易溶于甲醇、乙醇等有机溶剂,难溶于水,其在花生油、大豆油等植物油中有较大溶解度,故烯丙孕素口服液常用植物油作为载体辅料。当制剂样品以植物油作为载体辅料进行含量测定时,须先将主药成分提取出来再进行测试,如用乙醚溶解后再用甲醇多次提取[9],不仅需要经过繁琐的步骤,还耗费大量的有机溶剂,而且处理过程过多会造成样品损耗,进而导致测量误差。本研究中采用异丙醇-正己烷(5/20)作为混合溶剂,不但能将主药成分和辅料载体完全溶解,而且操作简单便于控制,避免了复杂的前处理步骤。
3.2 色谱系统的选择 传统的液相色谱系统常用非极性物质(如C18)作为固定相,以甲醇/水或者乙腈/水这些极性大的溶剂作为流动相进行洗脱。在本研究中由于样品前处理过程中用到异丙醇-正己烷(5/20)作为混合溶剂,混合溶剂的极性比较小,须选用极性大的物质(如氰基键合硅胶)为固定相、极性小的物质(如正己烷-异丙醇混合体系)为流动相的正相色谱系统进行分析。
本方法测定烯丙孕素口服液中烯丙孕素的含量,无需复杂的样品处理和特殊试剂,测定方法专属性强、准确度高、试剂成本低,便于生产中的质量检测。
