食品运载体系提高酚类物质生物利用度的研究进展
2020-03-31陈雨露孙婉秋高彦祥毛立科
陈雨露,孙婉秋,高彦祥,毛立科,袁 芳
(中国农业大学食品科学与营养工程学院,北京 100083)
在过去的几十年里,医疗保健费用的提高、大众对高品质生活的向往以及预期寿命的延长使得人们对食品的要求日益提高。饮食习惯和健康状况之间的关系一直受到科学界的广泛关注。生物活性物质具有促进健康的功能,常以注射或口服给药的方式治疗疾病,若将其作为膳食补充剂加入食品中,可赋予食品更多的功能特性。
酚类物质是维管植物的次级代谢产物,广泛存在于水果、谷物和蔬菜中,可作为植物和水果的呈色呈香成分[1],近年来已被证实具有多种生理活性,可作为生物活性物质加入食品工业中。自然界中大多数活性物质可以从植物或者动物体内提取后,直接加入食品中,然而天然酚类物质在水中的溶解度低,易受外界环境(温度、光照、氧气)、食品的加工贮存条件、消化道环境(pH值、酶、其他物质)的影响,这些性质均会降低其在食品和营养保健品中的生物利用度[2]。此外,有些酚类物质本身具有的涩味、酸味会直接影响产品的口感[3]。也有研究发现酚类物质可与食品中的其他成分结合产生不良风味或者降低营养价值[4-5]。因此,如何提高酚类物质的生物利用度、掩盖不良风味、保持其在食品中结构的完整性是近年来研究人员迫切关注的难点问题。
为了解决上述难题,科研人员提出了很多解决方法,如将非生物活性前体和生物活性物质进行连接的化学修饰法[6-8]、协同给药法[9]、运载体包埋法等。但化学修饰法可能改变原物质的生物活性、诱发食品安全问题;协同给药法中协同物质的选择局限性太大,会限制其在食品工业中的应用,所以这两种方法未能被广泛推行。已证实运载体系能有效提高活性物质的水溶性,避免其受光、热、氧的影响[10],并且包埋所用的方法和材料种类可选择性强;因此,近年来利用运载体系对酚类物质进行包埋的方法受到科研人员的青睐。食品工业中常用的运载体系有乳液、脂质体、微胶囊、纳米颗粒等。因选用包埋的材料均是食品级,且制备过程多利用分子间的相互作用,因此这种方法具有较高的安全性。本文介绍了酚类物质的功能性质和评价生物利用度的常见方法,针对应用现有运载体系提高酚类物质生物利用度的研究现状进行综述,最后对未来酚类物质运载体系的研究重点提出合理的建议,为推动健康中国策略献智献力。
1 酚类物质的功能活性
根据芳香环及芳香环上羟基的个数,可将酚类物质分为10 000多种不同的化合物[11],也可按照类别将其分为黄酮类、酚酸类、香豆素类、木质素类、单宁类[12]等(表1)。酚类物质具有清除活性氧自由基及抗氧化等多种生理活性[11]。其中花青素可以进入金黄色葡萄球菌、肠炎沙门氏菌和副溶血性弧菌的内膜抑制其碱性磷酸酶、酸性磷酸酶、超氧化物歧化酶的活性,从而抑制病原体的生长繁殖;黄酮类多酚通过调节一氧化氮-环磷酸鸟苷(nitric oxide-cyclic guanosine monophosphate,NO-cGMP)通路、抑制血管紧张素转换酶的生成起到促进血管舒张、保护肝脏的作用,可降低患心血管疾病及患高血压的风险[13-14]。此外,酚类物质可以参与癌细胞中不同酶的复制、转录、翻译过程,通过阻断各过程的信号通路抑制癌细胞的生长繁殖[15-17]。因此若将酚类物质作为生物活性物质加入食品中,可使产品具有预防糖尿病、肥胖症、心血管病和治疗癌症的作用。

表 1 常见酚类物质结构、生物活性及其常用运载体系Table 1 Structures and bioactivities of major phenolic compounds and commonly used delivery systems for them
2 评价酚类物质生物利用度的方法
生物利用度是指活性成分经口腔、胃、肠消化后通过小肠上皮细胞进入血液中并体现生理功能的量[26],同时生物利用度也是设计酚类物质运载体系过程中的重要参考因素[27]。用于评价酚类物质运载体系生物利用度最有效的方法是动物体内和人体内实验,但体内实验过程复杂、费时费力,对实验样品要求高,有时还因涉及潜在的有害物质受到道德伦理的约束[28-29];因此需要建立体外模型来模拟人类消化过程中发生的物理化学变化[29]。本文针对近年来体外消化模型的研究进展进行综述。
体外消化模型是一类评价运载体在口腔及胃肠道模拟消化过程中的物理化学变化以及释放效果的工具[30]。能否准确测量酚类物质运载体系生物利用度取决于消化模型在模拟人类胃肠道中复杂的物理化学反应和生理条件的有效性[31]。在过去的20 年里,研究人员设计了大量胃肠消化模型用于模拟食物消化过程,主要包括静态模型、动态模型和细胞培养模型等。
2.1 静态消化模型
静态消化模型是用来评价运载体系生物利用度最多的消化模型[31],它通过设置不同的初始条件(pH值、酶的种类和浓度、胆盐浓度、生化过程等)对人体口腔、胃、肠道消化进行模拟。通过调节消化液的化学组成成分可设计合理的静态消化模型[32],静态消化模型的设计见图1。
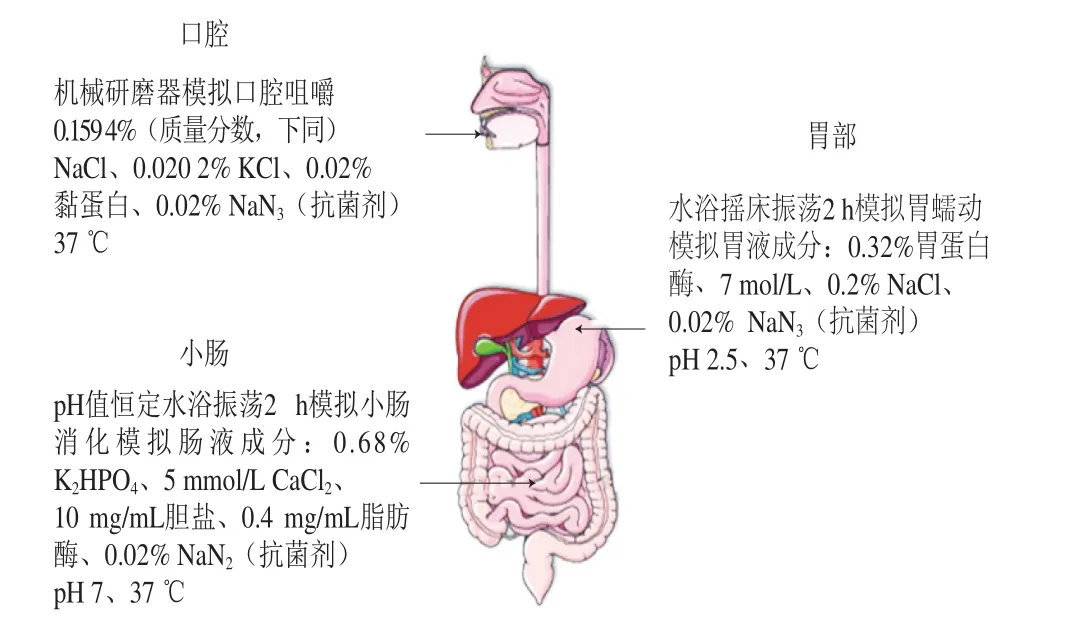
图 1 静态消化模型[32]Fig. 1 Static digestion model[32]
静态消化模型用于模拟局部消化过程中的化学作用,可用来研究包埋后酚类物质的溶解性和生物利用度。这种方法的优点是成本低、简单高效,现已广泛应用于评价食品运载体系中活性物质的释放状况。缺点是该模型不能提供胃肠蠕动、胃排空、肠道转运等机械力[33],忽略了胃肠消化中pH值变化和消化液分泌这一动态过程[34],因此静态消化模型存在一定的局限性,与实际动物体内的实验结果存在较大的差异。
2.2 动态消化模型
胃肠消化过程是一个动态的过程,既有化学作用也有物理作用。食物形态和结构的差异使消化过程中涉及的机械应力和流体流动状态成为不容忽视的影响因素。为了弥补静态模型的缺陷,近年来研究人员研发了单室、双室、多室等多种类型的动态消化模型,通过计算机的控制进行连续的胃肠消化模拟、协调消化液分泌时间、模拟胃肠中的机械应力等操作。
动态胃模型是使用较广的单室动态模型,可与人体胃模拟器结合模拟胃蠕动的振幅和频率,适用于研究食品中活性物质的释放和生物利用度的评价[35]。而双室和多室动态模型多设计为用于追踪食物在各个消化阶段食品成分的变化、模拟不同年龄人群胃肠消化以及食品成分与肠道微生物的关系等。目前,TNO胃肠道模型1是最接近人体胃肠消化的体外双室动态模型[36](图2),可以将该模型所测得结果和动物体内实验结果进行分析比较。
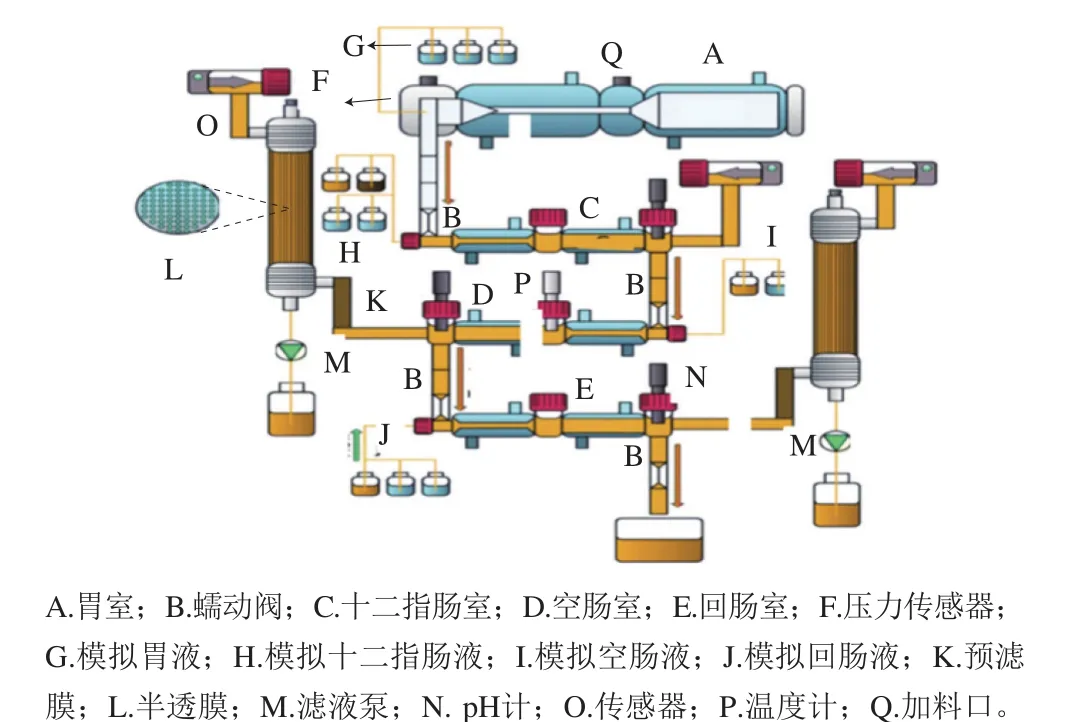
图 2 TNO胃肠道模型1[34]Fig. 2 TNO gastrointestinal model 1[34]
2.3 细胞培养模型
细胞培养模型也是体外消化模型的一部分,常用的细胞培养模型有肠上皮细胞、Madin Darby犬肾细胞系和Caco-2细胞[35]。其中,Caco-2细胞模型已被广泛应用于评价酚类物质及其运载体系的吸收机制和毒性检测中。
Caco-2细胞模型由人结肠腺癌细胞衍生而来,该细胞的结构和功能与分化的小肠上皮细胞接近,其标志酶的功能表达及通透特征也与小肠细胞相似。将其在含10%胎牛血清的醋酸纤维酯膜上进行传代培养后与经胃肠模拟消化后的消化物混合继续培养,一段时间后收集细胞于磷酸盐缓冲溶液中进行超声破碎处理,测定细胞中功能成分的含量,即可模拟计算出小肠上皮细胞对不同运载体系中功能成分的吸收情况,此外,Caco-2细胞膜还可作为检测运载体系毒性的体外细胞模型[37]。
3 常用食品运载体系
封装是将壁材和芯材进行组装的一个过程,在食品研究领域,封装常用于将对外界环境敏感的功能活性物质加入食品运载体系中,设计合理的运载体系可以改善活性物质的水溶性,提高其对光和热的稳定性,延长货架期,改善食品品质,防止聚集、沉淀的产生及提高缓释功效及靶向性[38]。常用的食品运载体系有乳液、脂质体、环糊精包合物、纳米颗粒等(图3)。
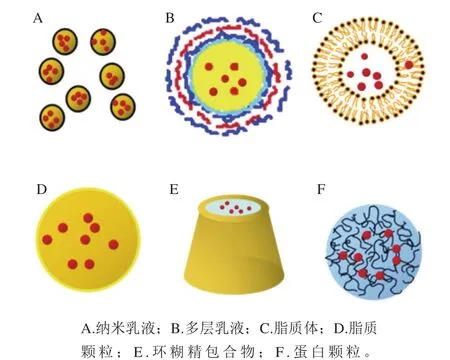
图 3 酚类物质运载体系示意图Fig. 3 Delivery systems for polyphenols
3.1 乳液
乳液是由两种或两种以上不相溶的液体相(油相和水相)混合形成的分散系[39]。可根据油-水两相的相对分散情况将其分为水包油型(O/W)乳液和油包水型(W/O)乳液。评价乳液体系优劣的两个关键因素是体系的稳定性和活性物质的生物利用率。
传统的乳液是将油-水两相混合后添加乳化剂均质而成,按照这种方法得到的乳液是热力学不稳定体系,在贮藏和加工过程中容易出现分层、聚集、破乳等现象[39]。近年来,针对这一问题,研究人员已成功设计多种不同结构和性质的乳液体系用于酚类物质的包埋与传递,如纳米乳液、多层乳液、多重乳液、Pickering乳液等,目前纳米乳液和多层乳液受到广泛的关注。
3.1.1 纳米乳液
纳米乳液的制备方法可分为低能法和高能法[40]。低能法是利用组分或环境条件的变化,从而使油、水、乳化剂的混合体系自发形成微小油滴,但是该方法不利于大规模的工业化生产。而高能法可以摆脱这一限制,该法是利用能够产生强烈破坏力的机械装置来混合和破坏油-水两相,从而形成微小油滴[40]。
纳米乳液是热力学不稳定体系,粒子的直径为20~200 nm,肉眼观察为透明或半透明状[41]。由于粒子直径较小,纳米乳液在贮存期间不易发生沉淀,具有较高的乳化稳定性。此外,在人体消化道内消化时,颗粒减小的同时其比表面积会相应增大,这对提高乳液的消化效率以及酚类物质的生物利用度起到一定的促进作用[42]。
3.1.2 多层乳液
乳液作为传递体系的优点是制备(混合、均质化)简单,但实现控释却很困难,克服这一困难的方法之一就是利用静电作用、氢键和疏水作用将聚电解质、酶、蛋白质等物质对乳液进行逐层(layer-by-layer,LBL)修饰,修饰后的乳液被称为多层乳液[43-44]。多层乳液的制备需要先使用一种乳化剂制备带有表面电荷的初级乳液,接着通过静电相互作用逐步沉积带相反电荷的材料[45-46]。多层乳液的液滴有着复杂的相间界面,其多层界面膜是由液滴所带电荷以及乳化条件所决定的,离子强度(盐浓度)、pH值、溶剂浓度和乳化剂的类型都会不同程度地影响多层乳液界面层形成过程、厚度及稳定性[47]。
3.2 脂质体
脂质体是由极性脂质分子按照细胞膜的排列方式“脚碰脚”组成的中空状、双层球形结构。其形成原理是脂质分子在水中自发有序排列成双分子球状结构,同时将水溶性物质封装在亲水核中,而脂溶性物质封装在磷脂双分子层的疏水尾部[48]。脂质分子被认定是安全(美国食品药品监督管理局)和可生物降解的,它可以通过瞬间改变细胞磷脂双分子层结构实现跨细胞转运,还可以调节细胞旁路改善活性物质的转运[48]。传统的脂质体制备技术包括手摇法、超声法、高压均质法和薄膜水合法等,但这些方法大多数都难以满足大规模的工业化生产且有较多的溶剂残留,因此现在多采用超临界流体萃取法、乙醇注入法和膜接触器法等新型制备方法[49]。
3.3 环糊精包合物
环糊精(cyclodextrin,CD)是由淀粉衍生而来的锥形环状聚合物,通常由6、7 个或8 个葡萄糖通过α-1,4-糖苷键连接而成。CD的结构是由Schardinger在1904年确定,并命名为环状低聚糖。CD是中空圆柱形的立体结构,由于亲脂性的亚甲基(—CH2—)和醚键(—O—)排列在空腔内侧,而亲水性的羟基(—OH)位于空腔的外侧,因此具有“内疏水、外亲水”的结构特征[50]。α-、β-和γ-CD的使用已获得美国食品药物管理局的批准,其中,β-CD由于内部空腔大小适中、生产廉价,应用范围相对广泛[51]。
3.4 纳米颗粒
纳米粒子可以通过氢键和疏水相互作用将酚类物质包埋在纳米粒子中,从而增强其溶解度,抑制其在胃肠道中的氧化分解。纳米颗粒通过诱导细胞内吞[52],直接被小肠上皮细胞摄取,这显著增加了酚类物质的吸收和生物利用度[53]。常用的纳米颗粒有纳米脂质颗粒、纳米蛋白颗粒、多糖纳米颗粒和它们的复合颗粒等。
4 食品运载体系提高酚类物质生物利用度的作用
提高酚类物质的生物利用度是改善其功能特性的主要因素,这也有助于将其应用到功能性食品中。如前所述,低溶解度、胃肠道降解以及低吸收是降低酚类物质利用度的主要影响因素。通过设计合理的食品运载体系对酚类物质进行封装,可有效减少这些因素对酚类物质的损害,还可进一步实现酚类物质的持续和控制释放[54],这是目前提高酚类物质生物利用度最有效的方法之一。以下针对各类体系的特点及其在提高酚类物质溶解度、降低胃肠道降解、提高吸收率等方面的作用进行介绍。
4.1 乳液
4.1.1 纳米乳液
纳米粒子较大的比表面积加快了油-水界面上的生化反应,与传统乳液相比,乳滴中的脂质可以尽快地被消化从而释放活性物质,这有助于抵抗胃肠疾病带来的消化不良[55]。槲皮素纳米乳液比游离的槲皮素更容易进入细胞膜[56]。也有研究证明在体外模拟消化实验中,纳米乳液的包埋可以实现儿茶素在胃肠道环境下的缓慢、持续释放[57]。据报道,纳米乳液在食品和营养学、生物学和药理学领域具有广泛的应用,在生物活性成分的高效包埋和靶向递送的应用中成果显著[58]。但其制备过程中需要大量的表面活性剂和助表面活性剂来稳定乳液,高浓度的表面活性剂不仅会影响酚类物质的溶解和释放,还可能存在潜在的毒性。
4.1.2 多层乳液
多层乳液常用于白藜芦醇与姜黄素的包埋。Acevedo-Fani等[59]制备包载白藜芦醇的乳铁蛋白-藻酸盐-ε-聚-L-赖氨酸3 层乳液,所得乳液短期稳定性较好,且3 层乳液中低浓度白藜芦醇的抗氧化活性高于双层乳液中高浓度的白藜芦醇。Silva等[37]以中链甘油三酯作为油相、以十二烷基硫酸钠(sodium dodecyl sulfate,SDS)作为阴离子乳化剂制备姜黄素纳米乳液,通过使用LBL静电沉积技术连续积聚电解质层到姜黄素纳米乳液上,构建壳聚糖-藻酸盐-壳聚糖多层纳米乳液,动态体外模型消化实验结果显示多层纳米乳液可有效地保护姜黄素免受胃肠道环境变化的影响,减少其在消化过程中抗氧化能力的丧失,Caco-2细胞毒性测试显示该多层纳米乳液没有毒性,甚至含有SDS的纳米乳液的毒性比SDS本身低3.3 倍。
4.2 脂质体
脂质体的包埋是提高酚类物质溶解度和生物利用度的有效方法之一。可消化脂质的存在通常有助于小肠对生物活性物质的吸收[12],有报道称大豆卵磷脂能够增强酚类物质的抗微生物和抗病毒活性[60]。将包埋槲皮素的纳米脂质体与槲皮素纳米乳和槲皮素固体脂质纳米粒进行比较,发现槲皮素纳米脂质体在模拟胃液中的稳定性较好,生物接受性高[61]。Zou Liqiang等[62]基于乙醇注射方法结合动态高压微流化,以吐温-80为表面活性剂、磷脂和胆固醇为材料制备包载表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)的纳米脂质体,结果显示该纳米脂质体具有较高的包埋率(92.1%),体外持续释放性能良好,可减缓体外消化过程中EGCG抗氧化活性的降低速度。与其他传递体系相比,脂质体与细胞结构相似,具有较高的生物相容性。此外,脂质体还具有靶向能力强、水溶性好,可以完成水不溶性和两亲性成分同时递送等优点[63]。
4.3 环糊精包合物
儿茶素微溶于水,对氧、光和pH值敏感,具有让人不愉悦的涩味[64],环糊精可有效掩饰涩味,在食品基质和体外消化模型中环糊精包埋的儿茶素显示出较高的稳定性和消化吸收率[64]。Li Xinpeng等[65]使用α-、β-、γ-CD,羟丙基-β-CD和二甲基(dimethyl,DM)-β-CD包埋姜黄素,体外消化模拟比较不同复合中姜黄素的溶解度、肠道模拟吸收情况,结果显示α-CD和DM-β-CD不会对肠膜产生毒性,可以通过α-CD和DM-β-CD的包埋提高姜黄素的口服吸收,50 mmol/L的α-CD能改变细胞旁路的转运屏障,从而增强小肠细胞对姜黄素的吸收。
在食品工业中,环糊精常用于掩盖活性物质的不良气味,增加其溶解性、稳定性和生物利用度。也有研究表明将脂质体和环糊精结合可显著增强槲皮素的光稳定性和体外消化稳定性[66],因此环糊精的包埋系统具有极大的研究价值。
4.4 纳米颗粒
结肠特异性递送是增强花青素生物利用度的有效途径之一,Wang Yuntao等[67]以几丁质为壁材制备包载花青素的纳米颗粒,发现几丁质与花青素之间的强相互作用使得超过85%的花青素被递送至结肠。壳聚糖作为唯一的碱性天然多糖具有良好的生物相容性和生物降解性,与其他传递体系相比,壳聚糖纳米粒子具有可控释放性强、副作用小、活性物质生物利用度高等优点[68]。壳聚糖纳米粒子作为载体还可以可逆地打开上皮细胞之间的紧密连接,从而促进纳米粒子在细胞旁路的转运[69]。Dube等[70]以小鼠为模型,发现口服EGCG壳聚糖纳米颗粒可有效增加小鼠胃肠中EGCG的浓度,可用于增强EGCG的口服递送治疗的功效。最近研究表明,采用反溶剂沉淀法制备的玉米醇溶蛋白/多糖/表面活性剂三元复合颗粒可有效用于姜黄素的包埋、控释,该三元复合物还有效增强了姜黄素的光稳定性和生物可接受性[71]。因此纳米颗粒在提高酚类物质的稳定性、实现酚类物质的靶向释放方面有广阔前景。
5 结 语
酚类物质具有抗氧化性、抗病菌、抗癌等多种生理活性,但是天然酚类物质溶解度低、稳定性差,很难使人们获益于它们的功能活性。近年来,科研人员基于食品运载体封装技术对其进行包埋,发现此类方法在体外消化模拟中可显著提高酚类的生物利用度、实现靶向释放和转运等,能有效解除上述限制,是一种安全、简便的技术手段。但是目前相关研究中还存在一些问题:1)目前口服的酚类运载体很难精确地实现靶向释放和定点吸收,使酚类功能活性的表达受到限制;2)评价运载体系有效性和生物利用度的体外消化模型标准不统一,缺乏针对性;3)关于运载体的机理研究较多,而关于运载体在食品中的应用研究较少,尚不清楚这些传递体系是否是按照行业需求进行设计、是否存在与食品基质不相容的成分。
基于上述存在的问题,今后关于酚类物质运载体系的研究可侧重于以下几个方面:1)尝试将不同包埋技术结合起来,探究其靶向释放和定点吸收的有效性;2)针对不同的酚类物质、运载体系建立全方位的体外消化模型标准,提高实验结果的参考价值和结果比较的可靠性,此外,还应针对不同患病人群完善体外消化模型系统;3)设计适用于食品工业的传递体系选择方案,探究不同组合物和制备方法对输送体系的影响,以便构建高性能的输送体系,实现多种营养素的同时输送。
