棘白菌素类抗真菌药物的临床应用进展
2020-03-27张诗琪程德云
张诗琪,程德云
(四川大学华西医院呼吸与危重症医学科,成都 610041)
近年来,真菌所致感染的发病率呈逐年升高的趋势。念珠菌是我国深部真菌感染中占比最高的菌种(91%),其中白色念珠菌、热带念珠菌、光滑念珠菌以及近平滑念珠菌占念珠菌总数的 95%,其余较常见的真菌依次为曲霉菌、马尔尼菲篮状菌(原称马尔尼菲青霉)、隐球菌和毛霉菌等[1-2]。近年来,对三唑类抗真菌药不敏感的非白色念珠菌逐渐取代白色念珠菌成为最常见的致病念珠菌属[3]。
目前,临床上可选用的抗真菌药物仍然较少。棘白菌素是一种新型抗真菌药物,目前经美国食品药品管理局(Food and Drug Administration,FDA)批准的棘白菌素类药物有卡泊芬净(美国默沙东药厂研发,2004年在美国上市)、米卡芬净(日本安斯泰来公司研发,2005年在日本上市)以及阿尼芬净(美国 Vicuron 制药公司研发,2006年在美国上市)。国内外于关棘白菌素类抗真菌药物的应用及研发进展已有报道,现对以上药物的作用特点及相关研究进展进行综述。
1 药理学特点
棘白菌素是真菌天然产物经化学修饰所得的一种半合成脂肽大分子(分子量约为1 200 000),其结构特点是含有N-链酰基脂侧链的两亲性六肽环(图1),侧链的位置和构象对药物的抗真菌活性、稳定性及水溶性至关重要,其与真菌细胞膜的磷脂双层嵌插,使棘白菌素通过非竞争抑制β-1-3-D葡聚糖合成酶破坏细胞壁的结构,导致真菌细胞内的渗透压力不平衡,最终致使菌体破裂死亡,菌丝形成也被抑制[4]。β-1-3-D葡聚糖是真菌细胞壁的主要结构成分,其不存在于哺乳动物细胞中,因此该类药物具有低毒高效的特点。棘白菌素的口服生物利用度低(<0.2%),临床上常采用静脉注射给药。药物进入人体后被红细胞吸收转运至肝脏(一部分在肾上腺和脾脏)降解,非活性代谢产物主要通过胆汁-粪便排出体外[5]。棘白菌素不需经肾脏清除,在肾功能不全时不需要调整剂量,这是其主要优势。棘白菌素为浓度依赖性药物,且具有长效抗真菌后效应[5]。每种药物的化学性质及代谢途径的不同也导致其半衰期及药物相互作用不同(表 1)。

卡泊芬净 C52H88N10O15×2C2H4O2 米卡芬净 C56H70N9NaO23S 阿尼芬净 C58H73N7O17
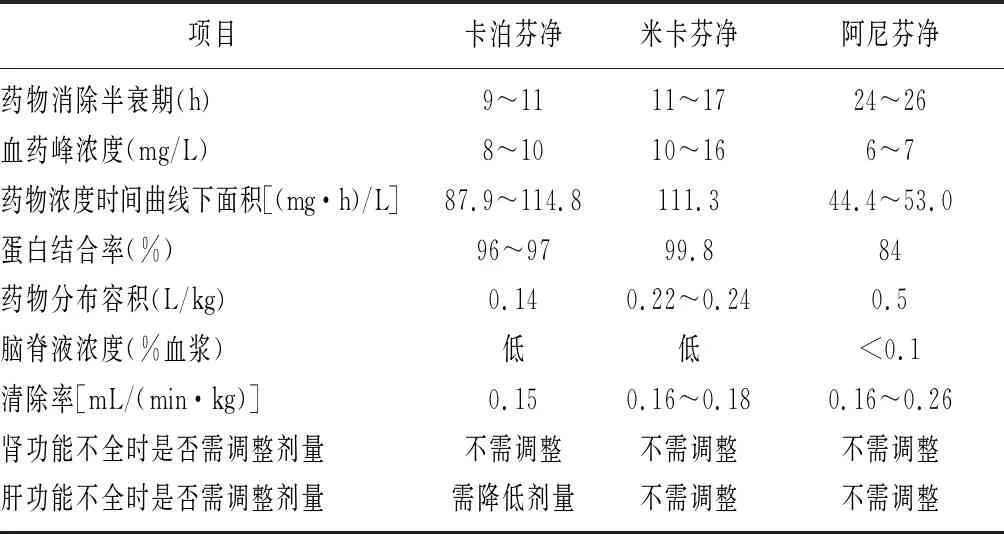
表1 三种药物的药动学特点[4-5]
2 抗真菌谱
卡泊芬净、米卡芬净以及阿尼芬净具有相似的抗菌谱、体外抗菌活性以及体内疗效,对白色念珠菌、光滑念珠菌、热带念珠菌等大部分念珠菌属有抗真菌活性,对多数曲霉菌属有抑菌作用(表 2)[6-7]。美国传染病学会和欧洲临床微生物学与感染病学会均建议将棘白菌素作为侵袭性念珠菌病的一线治疗药物、侵袭性曲霉菌病的二线治疗药物、重症监护病房中疑似念珠菌病的首选经验性治疗药物[8-9]。棘白菌素的抑菌谱有限,对毛霉菌属、隐球菌属和镰刀菌属均无活性。有学者认为,毛霉菌、镰刀菌的1-3-β-D葡聚糖合成酶的活性较低,因此影响了棘白菌素的抑制作用[4];而隐球菌细胞壁中的1-3-β-D葡聚糖被细胞壁外的厚荚膜掩盖,限制了药物发挥作用[4];肺孢子菌只有包囊表达1-3-β-D葡聚糖,而滋养体不表达,因此棘白菌素只能抑制包囊,而不能根治肺孢子菌肺炎[5]。

表2 棘白菌素类药物的抗真菌谱及抗菌活性[6-7]
3 临床应用
棘白菌素类药物的分子量大,蛋白质结合程度高,半衰期较短(需每日给药),通过静脉给药后广泛分布在肝、肾、肺、脾等脏器组织,其在中枢神经系统和眼部的渗透性小,且尿液中也检测不到有效的药物浓度,因此不推荐用于中枢神经系统、尿路或眼部的真菌感染[4-5]。由于不抑制细胞色素P450酶和p-糖蛋白转运系统,棘白菌素与其他药物相互作用较小。棘白菌素类药物虽有着相似的抗菌谱,但因代谢途径、用药剂量和安全性方面的不同而影响了临床用药策略。
3.1卡泊芬净(商品名科赛斯) 卡泊芬净是第一个获得FDA批准的棘白菌素类药物,最初只被批准用于侵袭性曲霉病、念珠菌感染或不能耐受其他抗真菌治疗的真菌感染,2008年被批准用于治疗儿童(3个月至17 岁)念珠菌感染[4],目前也被推荐用于治疗怀疑合并真菌感染的发热性中性粒细胞减少症和侵袭性曲霉病的补救治疗,但暂未批准作为侵袭性真菌感染的预防药物。一项多中心回顾性研究显示,卡波芬净治疗恶性血液病合并未明确病原菌的真菌感染的有效率达65%以上[10]。卡泊芬净可自发降解,也可通过 N-乙酰化进行肝脏代谢,其代谢产物通过粪便清除。
临床推荐卡泊芬净首剂70 mg,次日起每日50 mg 的维持剂量;对于3个月至17岁的患者,建议剂量为每日 50 mg/m2,最高 70 mg,次日开始予以70 mg/m2的负荷剂量;对于重度肝功能障碍者,推荐减少剂量,次日起每日剂量为首日剂量的 50%,这与另外两种棘白菌素药物不同[4]。研究发现,对于肥胖患者需要给予高于推荐剂量的卡泊芬净(150 mg/d)才能达到药动学/药效学指标[11-12]。
3.2米卡芬净(商品名 Mycamine) 米卡芬净是继卡泊芬净后FDA批准的第二个棘白菌素类抗真菌药物,其对成人和儿童真菌感染的临床疗效已通过各种临床试验得到验证,也是临床上唯一经认可的预防造血干细胞移植患者真菌感染的药物,对于造血干细胞移植患儿发热处理上米卡芬净优于卡泊芬净[13]。一项前瞻性多中心研究显示,恶性血液病患儿接受米卡芬净预防侵袭性真菌感染的有效率达76.6%(49/69),且重症监护病房内疑诊侵袭性真菌感染的新生儿使用米卡芬净治疗的有效率达85.7%(12/14)[14]。另有研究显示,急性白血病患者诱导化疗期间使用卡波芬净预防真菌感染的有效率和安全性与伯沙康唑无明显差异[15]。此外,近年来有多项关于尿路念珠菌感染使用米卡芬净治疗有效的案例报道,考虑其有效性与增加的药物剂量或个体差异相关[16-17]。米卡芬净在肝脏通过芳基硫酸酯酶和儿茶酚-O-甲基转移酶途径进行代谢,其代谢产物经粪便和尿液清除。
美国感染病学会推荐的给药方案为每日1次,每次100 mg,无负荷剂量,对于肝肾功能不全、需要透析者不需要调整剂量[9]。一项研究显示,对于体重达115 kg的白色念珠菌感染患者,米卡芬净的推荐剂量为150 mg/d,对于体重超过115 kg者,米卡芬净的推荐剂量为200 mg/d,但针对非白色念珠菌感染的肥胖患者的推荐剂量还需探讨[7]。
3.3阿尼芬净 2006 年,FDA批准阿尼芬净在临床使用,但该药至今仍未在国内上市。阿尼芬净被批准用于成人念珠菌血症、侵袭性念珠菌病和念珠菌性食管炎的治疗。阿尼芬净因较低的肝毒性,更适用于合并症较多的患者[18]。阿尼芬净在儿科中的应用尚未得到批准。阿尼芬净对烟曲霉、土曲霉以及黑曲霉的抑菌活性均强于对黄曲霉的抑菌活性,对新生隐球菌、毛霉、根霉、犁头霉等无抑菌活性。阿尼芬净是唯一一种在血浆中通过化学降解和非特异性肽酶降解,而非经过代谢途径降解的棘白菌素类药物,降解产物经胆汁由粪便排泄[5-6]。目前国外治疗念珠菌感染时建议首日给予负荷剂量200 mg,次日开始转为每日100 mg静脉输入。
3.4棘白菌素的联合用药 棘白菌素独特的作用机制引起了研究者们对联合抗真菌疗法的关注,尤其是在治疗侵袭性曲霉菌病方面。一项随机对照研究纳入了270例侵袭性曲霉菌病患者,伏立康唑单药治疗6周死亡率为27.5%(39/142),而伏立康唑+阿尼芬净治疗6周的死亡率为19.3%(26/135)(P<0.05)[19]。体外研究表明,米卡芬净与艾沙康唑联用治疗黄曲霉、土曲霉以及灰色小克银汉霉病时可产生协同效应,且这种协同效应具有浓度依赖性[20]。此外,关于肺孢子菌肺炎的研究表明,当甲氧苄啶/磺胺甲恶唑作为一线方案治疗失败时,棘白菌素联合甲氧苄啶/磺胺甲恶唑可能是较为理想的挽救治疗方案[21-22]。由此可见,合理地将棘白菌素同其他作用机制的抗真菌药物(三唑类或多烯类)联用可增强治疗效果。因此,真菌感染患者对单药治疗反应不佳或不能根除病原菌时可考虑联合使用抗真菌药物,但需要更多的临床研究来验证。
4 不良反应与临床使用局限
棘白菌素类药物的耐受性较好,但也存在一些不良反应,其最常见的不良反应是转氨酶和碱性磷酸酶升高,但明显低于三唑类和两性霉素B制剂。皮疹、瘙痒、低血压、支气管痉挛以及血管性水肿等不良反应可通过减慢输液速度和提供支持性护理控制[5]。其他潜在毒性主要是心脏毒性,国外有多项关于棘白菌素致心动过缓、低血压、心脏射血分数下降等的报道[23-24],因此应用于危重或血流动力学不稳定的患者时需谨慎,如果需要则应仅用于外周血管通路。目前这3种棘白菌素都被归类于 C类妊娠剂,因此不推荐用于孕妇[25]。
棘白菌素类药物因成本高、缺乏口服制剂而限制了临床应用。关于光滑念珠菌及白色念珠菌对棘白菌素类药物的耐药性也有报道[26]。近年来光滑念珠菌对棘白菌素的耐药性从2%~3%上升到 13%以上,考虑可能与编码β-D-葡聚糖细胞壁合成的FKS基因的突变有关[26]。目前已开发出一种通过聚合酶链反应快速诊断FKS突变的光滑念珠菌的方法[27]。棘白菌素的耐药性突出了药动学/药效学优化剂量及适当的抗真菌治疗的重要性,如果在临床实践中棘白菌素的耐药性增加,该药物的应用将进一步受限。
5 应用前景
5.1在生物膜中的作用 生物膜是附着在非生物或生物表面上的复杂的外聚合化合物,是可嵌入细胞外基质的微生物。生物膜的形成使真菌细胞逃避了宿主的免疫反应及传统抗真菌药物的作用,细菌-真菌相互作用并协同生长。生物膜使病原菌留置在关节滑膜、黏膜或医疗设备(如中心导管)表面,常规抗菌治疗很难将其治愈[28]。念珠菌属是真菌中最易与细菌共同致病的菌属。在白色念珠菌细胞中,β-葡聚糖层被外部甘露蛋白所遮蔽,免疫系统基本无法发挥作用。低浓度的卡泊芬净可使β-葡聚糖层暴露,从而发挥抗菌作用。一项研究表明,一种共价固定的卡泊芬净涂层钛表面能抑制白色念珠菌生物膜的形成[28]。另一项研究表明,用气体等离子体聚合法在12孔板和硅片上涂覆卡泊芬净可使白色念珠菌和热带念珠菌的菌落较对照组减少98%以上[29]。目前此类医疗器械正在研发中。
5.2免疫调节作用 研究发现,棘白菌素除具有抗真菌作用外还具有免疫调节作用,其通过干扰β-1,3-葡聚糖的合成抑制真菌生长,同时通过调控Dectin-1受体、Toll样受体及甘露糖结合凝集素等位点,激活宿主的固有免疫反应,从而达到直接或间接杀灭真菌的效果[30]。一项动物研究发现,预先使用米卡芬净可通过增强巨噬细胞的吞噬能力,延长金黄色葡萄球菌感染的大蜡螟幼虫的寿命[31]。关于棘白菌素在人体内的免疫调节功能还需更多的临床试验来证实。
5.3新型β-葡聚糖抑制剂 目前正在开发新型β-葡聚糖抑制剂,其中包括新型长效棘白菌素CD101[32],CD101由阿尼芬净衍生而来,具有独特的稳定性、较好的安全性和较长的半衰期(>80 h),可实现每周1次静脉给药。据报道,在体内CD101不仅对念珠菌和曲霉属具有活性,同时对FKS突变的白色念珠菌和野生型念珠菌、光肩孢霉、热带毛霉等也具有同卡泊芬净和阿尼芬净一样的活性[33]。目前该药正在进行Ⅱ期临床试验,明确新型棘白菌素在治疗中的地位有助于指导未来的研究及新药开发。
6 结 语
棘白菌素具有良好的药动学和药效学特征,且安全、耐受性好,虽然抗真菌谱较窄,但覆盖了侵袭性真菌感染中最常见的两种病原菌念珠菌和曲霉菌,是极具价值的一类抗真菌药物。近年来关于棘白菌素类药物国内外研究取得许多进展,如该类药物的免疫调节功能、在生物膜中的作用等,目前还需要进一步研究其复杂的耐药机制、矛盾现象、肥胖患者和儿童的剂量,并探索间歇性给药策略的作用,以期为棘白菌素的临床使用提供更好的参考。
在期待具有更广抗菌谱、更低不良反应的新型抗真菌药物的同时,还应严格规范抗菌药物的使用,利用药敏试验、基因型检测等技术手段尽量避免过度治疗和药源性不良反应的发生,并注意联合用药,以期提高真菌感染的治愈率。
