卡泊芬净对16种念珠菌体外抗菌活性研究
2019-09-24于淑颖张京家徐英春
张 丽, 于淑颖, 李 颖, 王 贺, 肖 盟, 张 戈, 张京家, 徐英春
随着糖皮质激素和免疫抑制剂的广泛使用、人类免疫缺陷病毒(HIV)感染的流行以及器官移植的开展等,侵袭性真菌感染的发病率逐年增加,严重感染时可造成血液和全身性感染,给患者的预后和生命安全带来很大威胁。其中念珠菌的感染尤为引人关注[1-2]。目前,念珠菌血症已占医院血源性感染的8%~10%,居医院感染性疾病第四位[3]。念珠菌血症的总体病死率高达40%,在所有医院感染病死率中居于首位,深部真菌感染的人均治疗费用在1998年已超过30 000美元[4]。近年来,随着抗真菌药物大范围预防使用,念珠菌对于唑类药物耐药率也在逐渐上升,棘白菌素类药物成为治疗深部念珠菌感染的重要药物[5]。
卡泊芬净(caspofungin)属于棘白菌素类抗真菌药物,通过非竞争性抑制(1,3)-β-D葡聚糖的合成、破坏真菌细胞壁的完整性而发挥抗菌作用。可用于经验性治疗成人和儿童(3个月及以上)患者中性粒细胞减少、伴发热的可疑真菌感染以及治疗对其他药物无效或不能耐受的侵袭性曲霉病。卡泊芬净对曲霉属(包括烟曲霉、黄曲霉、黑曲霉、构巢曲霉、土曲霉和白曲霉)和念珠菌属均具有体外抗菌活性[6-7]。本研究就江苏恒瑞医药股份有限公司生产的国产卡泊芬净(商品名卡净,以下称国产卡泊芬净)对常见和少见念珠菌的体外药物敏感性,与进口卡泊芬净(默沙东公司,商品名科赛斯,以下称进口卡泊芬净)进行对比,评估国产和进口卡泊芬净体外抗真菌活性的一致性。
1 材料与方法
1.1 材料
1.1.1 菌株来源 菌株来自中国侵袭性真菌监测网(CHIF-NET 2017),均分离自血液、组织、引流液、导管等无菌部位。共16种念珠菌(337株)纳入研究,所有菌株分离自全国29所医院,并且涵盖氟康唑敏感和一定比例的氟康唑耐药菌株,以进行更加全面的评估。337例念珠菌中白念珠菌60株、热带念珠菌50株、近平滑念珠菌复合体85株[包括近平滑念珠菌(Candidaparapsilosissensu stricto)47株、拟平滑念珠菌(Candida orthopsilosis)27株、似平滑念珠菌(Candida metapsilosis)11株 ]、光滑念珠菌54株、克柔念珠菌23株、季也蒙念珠菌32株、菌膜念珠菌4株、葡萄牙念珠菌13株、挪威念珠菌4株、都柏林念珠菌3株、希木龙念珠菌(Candidahaemulonii)3株、平常念珠菌(Candidainconspicua)2株、Candida fabianii2株、Candidavalida2株。质控菌株为近平滑念珠菌ATCC 22019,克柔念珠菌ATCC 6528。
1.1.2 试剂与仪器 氟康唑、伏立康唑、伊曲康唑标准品(中国食品药品检定研究院),泊沙康唑(美国默沙东公司),两性霉素B(中国食品药品检定研究院),国产注射用醋酸卡泊芬净(江苏恒瑞医药股份有限公司),进口注射用醋酸卡泊芬净(美国默沙东公司),注射用米卡芬净钠(安斯泰来制药中国有限公司)。科马嘉显色培养基(法国科马嘉公司),沙保弱培养基(英国OXOID公司)。RPMI1640培养基,含谷氨酰胺不含碳酸氢盐并以酚红为指示剂,使用0.165 mol/ L 3-(N-吗啉基)丙磺酸(MOPS)缓冲液调pH(7.0±0.1)(德国Sigma-aldrich公司);无菌U型96孔板(江苏省海门盛泰实验器材厂),全自动加样仪器Sentititre AIM(赛默飞世尔科技公司)。
1.2 方法
1.2.1 微量肉汤稀释法 药敏试验操作严格按照美国临床和实验室标准化协会(CLSI)2017年M27-A3[8]进行,测试药物包括氟康唑(0.25~256 mg/ L)、伏立康唑(0.015~16 mg/ L)、伊 曲 康 唑(0.015~16 mg/ L)、 泊 沙 康 唑(0.015~16 mg/ L)、米卡芬净(0.008~8 mg/ L)、两性霉素B(0.015~16 mg/ L)、卡泊芬净(进口,0.008~8 mg/ L)、卡泊芬净(国产,0.008~8 mg/L)。
1.2.2 数据分析 根据MIC值计算MIC范围、MIC50、MIC90和几何均数(geometric mean,GM),敏感性判定以CLSI 2017年M60推荐折点为判断标准,比较两种卡泊芬净药敏检测结果的一致性及8种抗菌药物的抗菌活性[9]。两种卡泊芬净的一致性通过分类一致率(categorical agreement,CA)和基本一致率(essential agreement,EA)进行评价,基本一致性指待测药物的MIC值与参考药物相差不超过1个稀释倍 数。
2 结果
2.1 国产卡泊芬净对16种念珠菌的体外抗真菌活 性
国产卡泊芬净对白念珠菌的MIC分布范围、MIC50、MIC90和GM分别为0.03~0.25 mg/L、0.064 mg/L、0.125 mg/L和0.07 mg/L;对热带念珠菌和光滑念珠菌的MIC分布范围、MIC50和MIC90与白念珠菌一致或相差一个梯度,GM相同,为0.11 mg/ L;对近平滑念珠菌复合体和季也蒙念珠菌的MIC50和MIC90相同,分别为0.5 mg/ L和1 mg/ L。分别有1株光滑念珠菌和1株克柔念珠菌对国产卡泊芬净中介,其余菌株均敏感。见表 1。

表1 卡泊芬净和其他抗真菌药物对念珠菌属337株的体外抗真菌活性Table 1 In vitro antifungal activity of domestic caspofungin and other antifungal agents against 337 isolates of Candida isolates
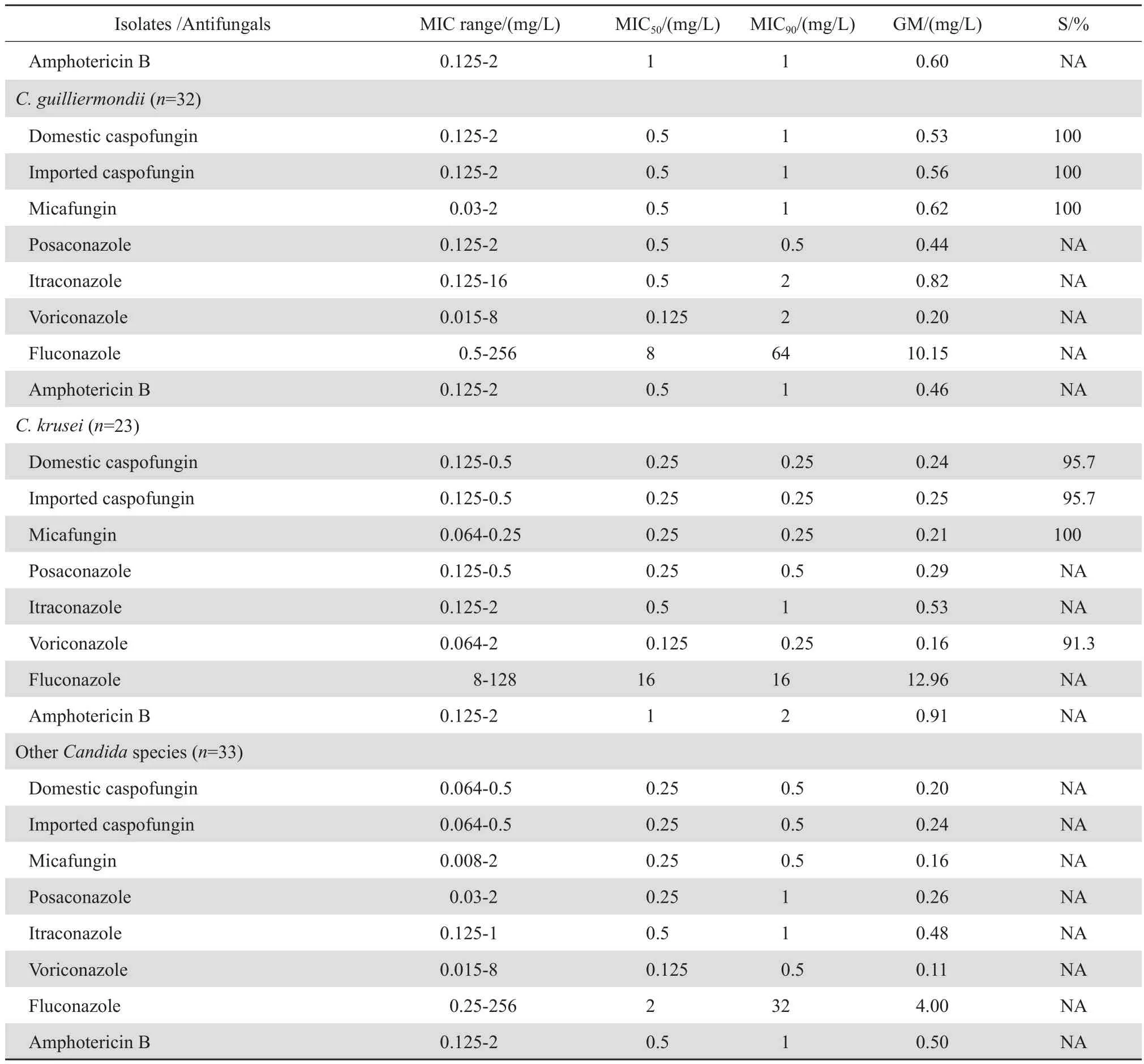
表1(续)Table 1(continued)
2.2 国产卡泊芬净的抗真菌活性与其他抗真菌药物比较
2.2.1 进口卡泊芬净 所有菌种检测结果中,国产和进口卡泊芬净的MIC50和MIC90均一致,MIC分布范围仅热带念珠菌中存在差别,其余念珠菌均一致,见表1。国产与进口卡泊芬净的CA和EA均为100%,所有测试菌株中仅有19株显示国产与进口卡泊芬净的MIC不一致,但均相差在1个浓度梯度内,与进口卡泊芬净相比,国产卡泊芬净对14株念珠菌的MIC低一个梯度、5株念珠菌的MIC高一个梯度。
2.2.2 其他棘白菌素药物 米卡芬净对白念珠菌和热带念珠菌的MIC50、MIC90分别是0.03 mg/L、0.064 mg/L和0.064 mg/L、0.125 mg/L,均比国产卡泊芬净低一个梯度。米卡芬净对光滑念珠菌的MIC50较国产卡泊芬净低2个梯度,对近平滑念珠菌复合体MIC50(0.5 mg/L)与国产卡泊芬净一致,MIC90(2 mg/L)较国产卡泊芬净高一个梯度;对季也蒙念珠菌MIC50(0.5 mg/L)和MIC90(1 mg/L)与国产卡泊芬净一致。
2.2.3 唑类药物 氟康唑敏感和耐药的白念珠菌与热带念珠菌的体外药物敏感性相比较,氟康唑耐药组中其他唑类药物包括伏立康唑、伊曲康唑和泊沙康唑的MIC值均高于氟康唑敏感组。白念珠菌对国产卡泊芬净的敏感性分析显示,氟康唑耐药组的MIC分布范围与敏感组接近,MIC高值低于敏感组1个梯度,氟康唑敏感和耐药组中GM基本一致,分别为0.07 mg/L和0.06 mg/L,且均未检出棘白菌素类药物耐药菌株。对于热带念珠菌,棘白菌素类药物MIC50和MIC90在氟康唑敏感组和耐药组中相同,国产卡泊芬净GM在氟康唑敏感和耐药组中基本一致,分别为0.11 mg/L和0.12 mg/ L。见表2。

表2 卡泊芬净与其他抗真菌药物对氟康唑敏感及耐药念珠菌属的体外抗真菌活性比较Table 2 Caspofungin antifungal activity compared between fl uconazole-susceptible and fl uconazole-resistant C. albicans and C. tropicalis isolates
3 讨论
唑类药物是治疗侵袭性念珠菌感染的一线药物,但随着抗真菌药物的大量和不规范使用,目前念珠菌对唑类药物的耐药率在逐渐上升,并且唑类药物之间交叉耐药现象明显。中国侵袭性真菌耐药监测网(CHIF-NET)连续5年的监测数据显示热带念珠菌对氟康唑的非敏感率从2010年11.2%上升至2014年42.7%,增长显著[10]。对其他常见念珠菌,CHIF-NET数据显示对唑类药物的敏感性也呈下降趋势,给临床治疗带来挑战[9]。棘白菌素类药物成为临床治疗唑类药物不敏感念珠菌的重要选择。
本组337株念珠菌来自全国多中心分离的侵袭性感染念珠菌,覆盖16个菌种,并且包含一定比例唑类药物耐药菌株,测试结果显示国产卡泊芬净对念珠菌呈现良好的体外抗真菌活性,仅有1 株光滑念珠菌和1株克柔念珠菌对国产卡泊芬净中介,未发现对棘白菌素类药物耐药的念珠菌。本研究结果与既往研究结论类似,CHIF-NET 2010-2013年的数据也显示念珠菌对棘白菌素类药物呈较高的敏感率,热带念珠菌和光滑念珠菌对卡泊芬净的敏感率超过99.0%[11]。比较国产和进口卡泊芬净的药敏测试结果,显示两种药物对所有菌种的体外活性CA和EA均为100%。
本研究显示,与其他念珠菌相比,国产卡泊芬净对近平滑念珠菌复合体的MIC50和MIC90值(0.5 mg/ L和1 mg/L)比白念珠菌(0.064 mg/ L和0.125 mg/L)高,这与国际SENTRY真菌监测项目结论相似[12]。在SENTRY 2010-2012年监测项目中,卡泊芬净对近平滑念珠菌复合体的MIC50和MIC90为0.25 mg/L和0.5 mg/L,明显高于白念珠菌(0.03 mg/ L和0.06 mg/L)。目前近平滑念珠菌复合体对棘白菌素类药物MIC偏高的原因尚不明确,Garcia-Effron等[13]研究发现近平滑念珠菌复合体Fks1的660存在一个保守脯氨酸向丙氨酸的自发突变,可能是引起MIC值升高的原因。因此桑福德抗微生物治疗指南中推荐棘白菌素类药物为治疗临床近平滑念珠菌复合体感染的二线用药[14]。
另外,本研究结果显示国产卡泊芬净对唑类药物耐药和敏感的白念珠菌及热带念珠菌的MIC50、MIC90和GM无明显差异。所有唑类药物耐药的白念珠菌和热带念珠菌均对国产卡泊芬净敏感。唑类药物对光滑念珠菌的MIC值较高,克柔念珠菌对氟康唑天然耐药[11],而本研究显示棘白菌素类药物对光滑念珠菌和克柔念珠菌的MIC50、MIC90接近热带念珠菌MIC值分布,均未发现耐药菌株。CHIF-NET 2010-2013年的数据显示光滑念珠菌和克柔念珠菌对卡泊芬净的敏感率分别为99.0%和95.1%,对米卡芬净的敏感率均为100%[11]。因此棘白菌素类药物是治疗唑类药物耐药的白念珠菌或热带念珠菌、光滑念珠菌和克柔念珠菌感染较好的选择。
卡泊芬净对于大多数念珠菌的体外药物敏感性较高,尤其是对唑类药物获得性耐药的念珠菌或天然耐药的念珠菌国产和进口卡泊芬净均有较好的体外抗菌活性,本研究并未发现对棘白菌素类药物耐药的念珠菌属。
