磷酸铜表面修饰富锂层状正极材料的制备及电化学性质
2020-03-25杨玉莹杜勇慧刘文闫周晓明
陈 红, 杨玉莹, 杜勇慧, 张 鑫, 刘文闫, 周晓明
(1. 北华大学 理学院, 吉林 吉林 132013; 2. 北华大学 材料科学与工程学院, 吉林 吉林 132013)
商用锂离子电池正极材料是性能稳定、 安全性较高的过渡金属氧化物材料, 如钴酸锂(LiCoO2)、 磷酸铁锂(LiFePO4)和三元材料等[1-3]. 由于这些正极材料的比容量较低, 与石墨负极组装成电池时限制了电池容量. 因此, 开发具有更高比容量的正极材料对提升电池性能至关重要[3-4]. 其中富锂层状正极材料以其高放电比容量(>250 mA·h/g)和高工作电压(>3.5 V)已引起人们广泛关注[5]. 但富锂材料作为锂离子电池正极材料存在循环过程中电压衰减严重、 循环稳定性及倍率性能较差等缺点[6-7]. 由于电解液在高电压下分解, 分解产物在材料表面形成阻碍电化学反应的表面膜(SEI), 使富锂材料容量衰减, 因此富锂材料的电化学性能较差. 对富锂材料的改性研究表明, 表面修饰层可有效阻止电解液腐蚀电极材料, 保持电极结构完整, 并可抑制电极材料表面过渡金属的溶解, 维持材料结构稳定. 目前, 对富锂层状材料的改性主要集中在氧化物的表面修饰改性, 其改性方法简单、 高效, 可使电化学性能明显提升, 但电解液分解产生的氟化氢(HF)极易腐蚀氧化物, 从而使其失去对电极的保护作用, 且合成氧化物的原料成本较高, 不适合大规模生产应用. 基于此, 本文选择Cu3(PO4)2进行表面修饰, 并研究Cu3(PO4)修饰对富锂层状正极材料电化学性能的影响及其反应机理.
1 实 验
1.1 材料的制备
按目标产物元素的百分数称取相应质量的乙酸锰(Mn(CH3COO)2)、 乙酸镍(Ni(CH3COO)2)和乙酸钴(Co(CH3COO)2), 先将其溶解于200 mL超纯水中, 再分别加入相应质量的碳酸锂(Li2CO3)和柠檬酸(C6H8O7), 在室温下混合搅拌. 用氨水调节混合溶液的pH=7.3, 于60 ℃加热搅拌, 得到固体凝胶, 将固体凝胶研磨成粉末, 先在空气中450 ℃预处理24 h, 再在900 ℃高温烧结24 h, 得到富锂锰氧正极材料, 其化学分子式为Li1.18Ni0.15Co0.15Mn0.52O2.
按Cu和P元素物质的量比为3∶2称取相应质量的硝酸铜(Cu(NO3)2)和磷酸氢二铵((NH4)2HPO4), 先分别溶于超纯水中; 再将两种溶液混合进行室温反应, 形成淡蓝色沉淀, 滴加氨水使溶液中的沉淀溶解, 形成清澈透明的深蓝色溶液, 加入合成的富锂锰氧正极材料; 最后, 将混合溶液在40 ℃缓慢搅拌至水分完全蒸发, 并将烘干后的粉末在空气中450 ℃烧结5 h, 自然降温后得到Cu3(PO4)2表面修饰的富锂层状材料.
1.2 材料表征测试
用DX-2700B型X射线衍射仪(丹东浩元公司)测试材料的晶体结构, 管电压为40 kV, 管电流为40 mA, 采用步进测量, 步进角度为0.02°, 采样时间为0.2 s, 测试角度为10°~80°; 用SU8020型扫描电子显微镜(日本日立公司)观察材料形貌; 用VERTEX 70型Fourier变换红外光谱仪(德国布鲁克公司)测试材料的红外光谱.
1.3 电池制备和性能测试
将制备的初始富锂材料与Cu3(PO4)2表面修饰的富锂层状材料充分研磨, 先分别与导电助剂Super P按质量比为5混合研磨, 使Super P均匀分散在材料中, 再将质量分数为7%的聚偏氟乙烯(PVDF)及N-甲基吡咯烷酮(NMP)混合胶水与干燥后的样品按质量比为1∶0.63混合, 并涂覆在干燥的Al箔上. 自然晾干后, 先将已涂布的Al箔置于120 ℃真空干燥箱中干燥12 h后, 再将Al箔切成8 mm×8 mm的电极片, 在氩气手套箱中组装成2032型扣式电池. 其中负极为直径为16 mm的金属锂片, 电解液为1 mol/L六氟磷酸锂(LiPF6)溶解在碳酸乙烯酯(EC)、 碳酸二乙酯(DMC)和碳酸甲乙酯(EMC)的混合溶液中(其中溶剂为V(EC)∶V(DMC)∶V(EMC)=1∶1∶8), 隔膜为Celgard 2320型隔膜.
用Land 2100型测试仪(武汉蓝电公司)进行恒流充放电测试; 用VSP MPG2电化学工作站(法国Bio-Logic公司)进行循环伏安(CV)及电化学阻抗(EIS)测试.
2 结果与讨论
2.1 材料表征

图1 初始与Cu3(PO4)2表面修饰富锂材料的XRD谱
初始与Cu3(PO4)2表面修饰富锂材料的扫描电子显微镜(SEM)照片如图2所示. 由图2可见, 材料经Cu3(PO4)2修饰后的形貌基本未发生变化. 但初始较光滑的颗粒经修饰后表面出现较多凹陷和凸起, 这是由于在制备过程中Cu3(PO4)2的不均匀沉积所致.

图2 初始(A)与Cu3(PO4)2表面修饰(B)富锂材料的SEM照片
Cu3(PO4)2表面修饰富锂层状材料的元素分布如图3所示. 由图3可见: 富锂材料中过渡金属元素(Ni,Co,Mn)分布均匀, 且P和Cu与过渡金属元素的分布状态基本一致, 表明Cu3(PO4)2均匀分布在初始富锂材料表面, 实现了富锂材料的表面修饰. 由于修饰后材料中P和Cu元素的质量分数相对较低, 因此P和Cu元素比富锂材料中过渡金属元素的分布稀疏. 由图3(E)可见, P元素在局部高亮区域聚集, 表明该缓慢沉积的表面修饰方法未使表面修饰物均匀分布在富锂材料表面, 在局部区域出现大量沉积, 与SEM结果相符.
2.2 电化学性能测试
初始与Cu3(PO4)2表面修饰富锂材料的首圈充放电曲线如图5所示. 由图5可见: 初始与Cu3(PO4)2表面修饰富锂材料具有相近的首圈放电比容量, 表明少量Cu3(PO4)2表面修饰不影响初始富锂材料的插锂量; 初始与Cu3(PO4)2表面修饰富锂材料的首圈充电比容量差异较大, 经Cu3(PO4)2表面修饰富锂材料的充电比容量随Cu3(PO4)2质量分数的增大而逐渐降低, 其首圈库仑效率由77%提高至94%. 表明Cu3(PO4)2表面修饰大幅度降低了富锂材料首圈充电过程中的能量损失, 提升了材料的实用性.

图3 Cu3(PO4)2表面修饰富锂层状材料的元素分布
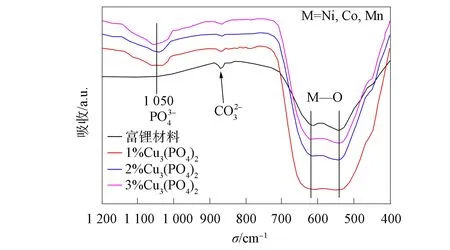
图4 初始与Cu3(PO4)2表面修饰 富锂材料的FTIR光谱
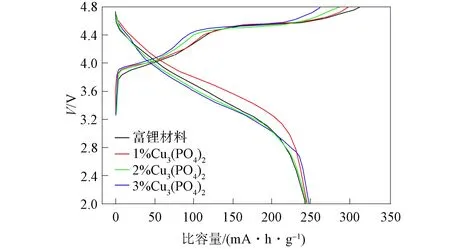
图5 初始与Cu3(PO4)2表面修饰 富锂材料的首圈充放电曲线
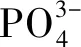
初始与Cu3(PO4)2表面修饰富锂材料的前两圈充放电曲线如图7所示. 由图7可见, 经表面Cu3(PO4)2修饰后的富锂材料在3.0,2.7 V处出现一对区别于初始材料的充放电平台. 初始与质量分数为3%的Cu3(PO4)2表面修饰富锂材料的循环伏安(CV)曲线如图8所示. 由图8可见, CV测试结果与充放电曲线结果一致, 经表面修饰的富锂材料在3.0,2.7 V处出现一对新的氧化还原峰. 表明在充放电过程中富锂材料表面生成了尖晶石相锰氧化物[17].
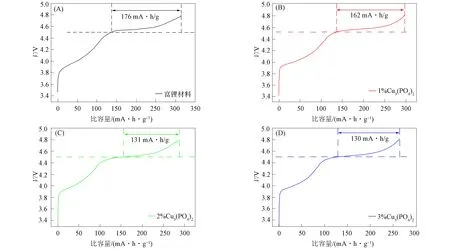
图6 初始与Cu3(PO4)2表面修饰富锂材料的首圈充电曲线

图7 初始与Cu3(PO4)2表面修饰富锂材料的前两圈充放电曲线
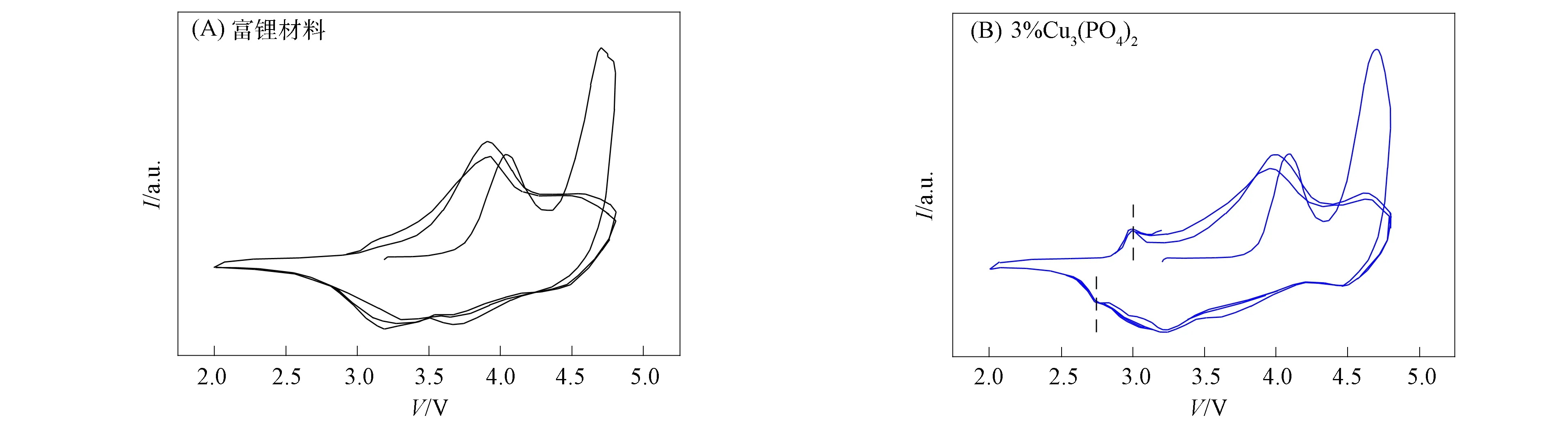
图8 初始与Cu3(PO4)2表面修饰富锂材料的CV曲线
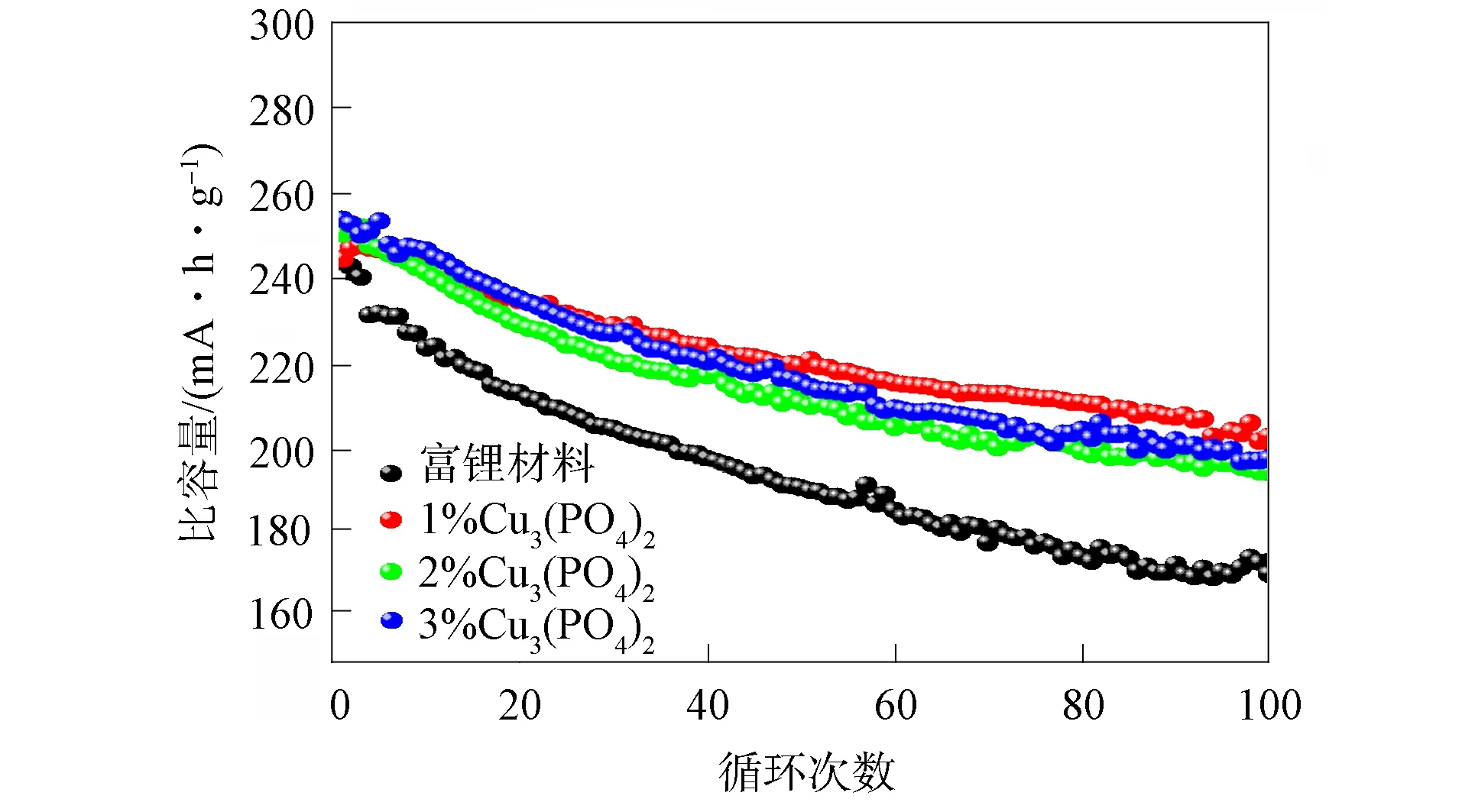
图9 初始与Cu3(PO4)2表面修饰富锂材料 在40 mA/g电流密度下的循环性能
初始与Cu3(PO4)2表面修饰富锂材料在40 mA/g电流密度下的循环性能如图9所示. 由图9可见: 经质量分数为1%的Cu3(PO4)2表面修饰富锂材料的循环性能最好, 当初始放电比容量为244 mA·h/g时, 经100圈循环后可逆比容量为203 mA·h/g, 容量保持率高达83%; 当初始材料的初始放电比容量为244 mA·h/g时, 其100圈循环的容量保持率仅为70%. 这是由于经表面修饰富锂材料表面的Cu3(PO4)2可阻隔电解液接触富锂材料, 避免了电解液腐蚀电极表面, 抑制了结构中过渡金属的溶解, 从而有效抑制了材料在充放电过程中的电压降. 由于Cu3(PO4)2包覆层未被HF腐蚀, 可在电解液中稳定存在, 长期保持对电极材料的保护作用, 因此, 经Cu3(PO4)2表面修饰富锂材料的循环性能得到显著提升.
初始与Cu3(PO4)2表面修饰富锂材料在循环过程中的充放电曲线如图10所示.
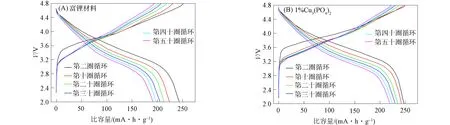
图10 初始与Cu3(PO4)2表面修饰富锂材料在循环过程中的充放电曲线
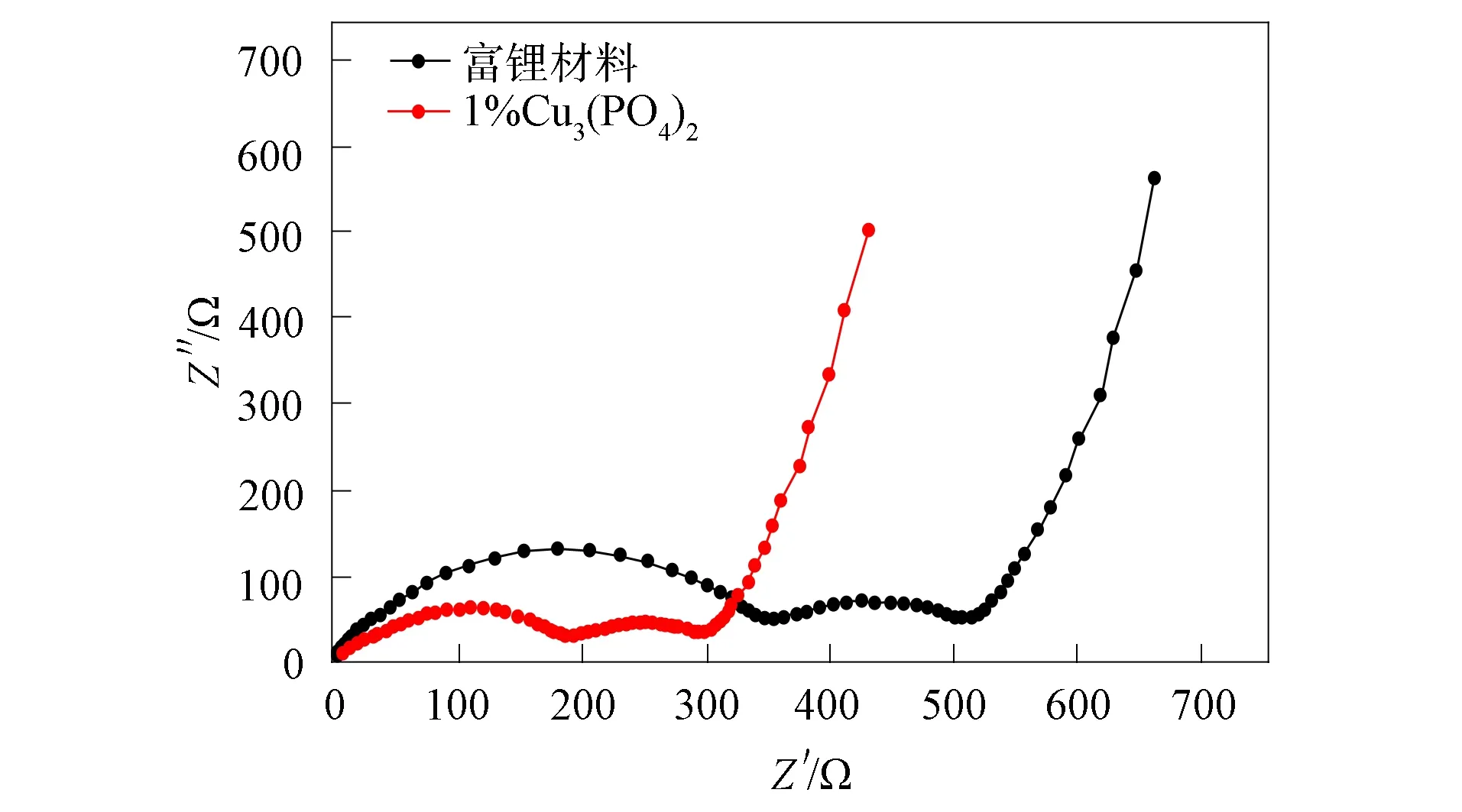
图11 初始与Cu3(PO4)2表面修饰富锂材料的电化学阻抗谱
由图10可见: 经质量分数为1%的Cu3(PO4)2表面修饰富锂材料的第二圈充、 放电比容量分别为249,247 mA·h/g, 库仑效率达99%; 初始材料的充、 放电比容量分别为252,242 mA·h/g, 库仑效率为96%. 表明经表面修饰的富锂材料可有效抑制电解液在高电压下与电极表面发生副反应, 从而避免了充电时材料表面生成固体电解质界面(SEI)膜而消耗电解液中的Li+; 初始材料远大于经质量分数为1%的Cu3(PO4)2表面修饰材料充电比容量的衰减速率. 这是由于原始材料中的电解液在材料表面发生副反应生成SEI膜所致. SEI膜具有较大电阻, 使电池的内阻逐渐增大, 电极间的电压逐渐减小, 导致材料在充电上限电压时的插锂量减小, 电池的可逆充电比容量随循环次数的增加而减小. 经Cu3(PO4)2表面修饰的富锂材料表面存在Cu3(PO4)2保护层可抑制电解液与富锂材料发生副反应, 从而减少了在材料表面形成的SEI膜, 阻止了电池内阻持续增加, 使电池的容量在循环过程中保持稳定. 因此, 经Cu3(PO4)2表面修饰可提高材料的循环稳定性.
初始与Cu3(PO4)2表面修饰的富锂材料在首圈充电到4.5 V时的电化学阻抗谱(EIS)如图11所示. 本文通过等效电路拟合对测试结果进行定量分析. 由图11可见, 两个样品的测试结果均在高频区出现两个半弧, 其中第一个半弧对应材料的表面膜电阻(RSEI), 第二个半弧对应材料的电荷转移电阻(Rct). 初始材料大于经质量分数为1%的Cu3(PO4)2表面修饰富锂材料的表面膜电阻及电荷转移电阻, 表明表面修饰可抑制在电极表面产生界面膜, 促进电荷在电极表面传递, 从而提高材料的电化学性能.
综上, 本文用溶胶-凝胶法实现了Cu3(PO4)2对富锂材料表面的均匀修饰. 结果表明: 经Cu3(PO4)2表面修饰材料的首圈库仑效率显著提升, 由初始材料的77%提高至94%, 大幅度降低了该材料的能量损耗, 提高了富锂材料的实用性, 且循环性能提升明显, 在40 mA/g电流密度下循环100圈后的放电比容量由170 mA·h/g提高至205 mA·h/g, 容量保持率由70%提高至83%; 表面修饰后材料的表面膜电阻及电荷转移电阻均明显减小, 即Cu3(PO4)2表面修饰层可抑制电解液在材料表面反应生成SEI膜, 促进电荷在电极表面的转移.
