清肺益气汤联合GP方案治疗晚期非小细胞肺癌的疗效观察
2020-03-18陈鑫骆洪雁高晶姜晓文齐超张永娟刘东海
陈鑫 骆洪雁 高晶 姜晓文 齐超 张永娟 刘东海
近年来,肺癌的发病率和死亡率逐年上升,癌症发病率在中国城市人口中居第一位[1]。根据肺癌的病理特征,分为小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC)。 其中,NSCLC约占所有肺癌的80%,约70%的NSCLC患者处于晚期诊断阶段,进行根治性手术的机会基本丧失,并且5年生存率非常低,主要采用保守化疗以缓解疾病并延长生存时间[1]。然而,长期的临床实践发现化学疗法过程中存在耐药性和对生活质量的影响。近年来,中医药在肺癌综合治疗方面取得了很大进展,特别是对于一些晚期肺癌患者。加强中药干预与放、化疗相结合,可明显改善患者的临床症状和生活质量,并显示出“带瘤生存”的疗效特点[2]。因此,积极探索中药在改善晚期NSCLC患者临床症状,减轻放、化疗毒副反应,提高治疗耐受性等方面的作用机制,对稳定病情、延长生命周期、提高生活质量、提高生存率等方面具有重要的临床意义[3]。中药在非小细胞肺癌的临床治疗中取得了较好的疗效,有减少不良反应,提高生活质量、延长生存时间的优势[4]。此外,最新研究还证实清肺益气方可有效促进肺癌细胞的凋亡,抑制肿瘤的生长[5]。我们以清肺益气汤联合GP方案治疗晚期NSCLC患者,观察患者临床症状、免疫功能、生活质量评分、毒副反应等指标的变化,研究清肺益气汤药联合GP方案在提高晚期NSCLC患者生活质量、改善机体免疫功能、减轻化疗药物毒副反应、改善预后等方面的作用。
1 资料与方法
1.1 一般资料 选择我院2013年3月至2019年4月收治的晚期NSCLC患者56例,随机分为观察组和对照组,每组28例。观察组:男19例,女9例;年龄53~70岁,平均年龄(59.8±5.6)岁;病理情况:腺癌9例,鳞状细胞癌14例,腺鳞癌3例,大细胞癌2例。临床TNM分期:Ⅲ期15例,Ⅳ期13 例。对照组:男16例,女12例;年龄55~70岁,平均年龄(60.3±5.4)岁;病理情况:腺癌7例,鳞状细胞癌12例,腺癌6例,大细胞癌3例。临床TNM分期:Ⅲ期17例,Ⅳ期11例。2组一般资料比较差异无统计学意义(P>0.05)。本研究获医院医学伦理委员会的批准,并获得患者或家属的知情同意,签署知情同意书。
1.2 纳入与排除标准
1.2.1 纳入标准:①符合《中国常见恶性肿瘤诊治规范》诊断标准;②符合《中药新药临床研究指导原则》[6]诊断标准;③经病理组织学或细胞学确诊为NSCLC,国际分期(TNM)标准属Ⅲ、Ⅳ期者;④病变组织大小及位置可准确测量;⑤营养状况良好,无腹腔积液,胸腔积液等;⑥近期未接受其他抗肿瘤治疗;⑦各脏器功能基本正常;⑧预计存活时间超过3个月。
1.2.2 排除标准:①先天性心脏病和严重肝肾功能不全患者;②近2个月患心脑血管疾病者;③妊娠,哺乳期女性;④卡诺夫斯基(Karnofsky)评分<60分者。
1.3 治疗方法 2组患者均接受水化、止吐药+地塞米松治疗(山东益康药业有限公司,规格:5 ml∶5 mg)+地塞米松磷酸钠注射液(天津药业焦作有限公司,规格:1 ml∶5 mg)治疗。对照组患者第1天给予吉西他滨(商品名泽菲,江苏豪森药业股份有限公司,规格:1 g)1 000 mg/m2,第1~3天给予顺铂注射液(江苏豪森药业股份有限公司,规格:6 ml:30 mg)30 mg/m2,3周重复。观察组患者在对照组基础上加用清肺益气汤:黄芪30 g,炒白术15 g,茯苓15 g,炙鸡内金10 g,天花粉15 g,太子参18 g,女贞子25 g,沙参20 g,麦冬15 g,百部25 g,桑白皮12 g,枇杷叶15 g,鸡血藤30 g,杏仁20 g,瓜蒌 30 g,紫金牛10 g,苦参30 g,五味子9 g,陈皮9 g。水煎服约 200 ml,2次/d。
1.4 观察指标 观察治疗前后2组患者临床疗效,症状改善情况,T细胞免疫功能、凝血状态、毒副反应、肿瘤标志物CEA水平、生活质量及生存时间。治疗前后抽取静脉血,检测活化部分凝血活酶时间(APPT))、纤维蛋白原(FBI)、凝血酶原时间(PT)和D-二聚体(D-D)。观察治疗前后咳嗽、咳痰、痰血、乏力、纳差、胸闷气促症状的变化情况。毒副反应参照《(WHO)急性和亚急性毒副反应分度标准》。生活质量评分标准根据欧洲癌症研究(EQRTC QLQC43)量表制定[7]。 分数越高,生活质量越差。
1.5 疗效评价 按照WHO抗肿瘤药疗效标准[8]进行评价。 完全缓解:病变消失,持续时间>1个月;部分缓解:病变减少值超过50%,无新发或转移性病变,持续时间>1个月;好转:>50%病变减少值≥25%,无新发或转移性病变;稳定:病变减少值<25%,无新发或转移性病变;恶化:病变扩大值≥25%,有新发或转移性病变。 总有效=完全缓解+部分缓解。
2 结果
2.1 2组患者临床疗效比较 观察组总有效率为64.3%明显高于对照组的32.0%,差异有统计学意义(P<0.05)。见表1。

表1 2组患者临床疗效比较 n=28,例(%)
2.2 2组患者临床症状改善情况比较 观察组咳嗽、乏力、纳差症状改善情况明显好于对照组(P<0.05),2组咳痰、痰血和胸闷气促情况差异无统计学意义(P>0.05)。见表2。

表2 2组患者临床症状改善情况比较 n=28,例
注:与对照组比较,*P<0.05

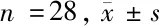

组别CD+3(%)CD+4(%)CD+8(%)CD+4/CD+8观察组 治疗前60.36±6.1237.47±4.0430.44±3.451.16±0.23 治疗后66.17±6.36∗#39.88±4.32∗#28.68±3.28∗#1.41±0.24∗#对照组 治疗前60.15±6.3737.67±4.3330.86±3.611.19±0.23 治疗后61.78±6.1338.02±4.1729.87±3.381.22±0.35
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
2.4 2组患者治疗前后凝血状态比较 2组患者APPT和PT治疗前后差异无统计学意义(P>0.05)。观察组FIB和D-D水平明显低于治疗前及对照组,差异有统计学意义 (P<0.05)。见表4。
2.5 2组患者血常规比较 治疗前,2组血常规结果差异无统计学意义(P>0.05)。治疗后,对照组白细胞、血小板及血红蛋白显著下降,与治疗前比较,差异有统计学意义(P<0.05)。治疗后观察组患者白细胞、血小板及血红蛋白与治疗前比较差异无统计学意义(P>0.05)。见表5。
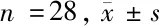

组别APPT(s)PT(s)FIB(g/L)D-D(μg/ml)观察组 治疗前30.91±3.35112.13±1.092.94±0.44241.39±94.36 治疗后30.71±3.6212.21±0.942.59±0.36∗#206.46±89.47∗#对照组 治疗前31.12±3.7311.96±1.232.93±0.51243.87±96.44 治疗后30.79±3.8412.31±1.142.95±0.49241.65±97.69
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
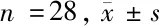

指标观察组治疗前治疗后对照组治疗前治疗后白细胞(×109/L)5.34±0.715.21±0.735.26±0.683.43±0.56∗血小板(×109/L)161.24±46.76158.53±46.64164.29±47.31121.13±47.17∗血红蛋白(g/L) 118.83±8.87116.58±6.71118.67±9.2695.47±7.76∗
注:与治疗前比较,*P<0.05
2.6 2组患者毒副反应比较 治疗后,观察组出现消化道反应(呕吐)9例,出现Ⅱ度呕吐1例,对照组出现消化道反应(呕吐)23例,其中Ⅱ度及以上呕吐患者10例,2组差异有统计学意义(P<0.05);观察组肝功能损害3例,Ⅰ度损害2例,Ⅱ度损害1例,对照组肝功能损害4例,Ⅰ度损害2例,Ⅱ度损害1例,Ⅲ度损害1例;2组差异无统计学意义(P>0.05);观察组肾功能损害2例,Ⅰ度损害1例,Ⅱ度损害1例,对照组肾功能损害3例,Ⅰ度损害1例,Ⅱ度损害2例,2组差异无统计学意义(P>0.05)。见表6。

表6 治疗后2组患者消化系统、肝、肾毒副反应比较 n=28,例
注:与对照组比较,*P<0.05
2.7 2组患者治疗前后生存质量比较 治疗前,2组患者工作与医师关系、家庭生活、情感功能、经济困难评分和总分间差异无统计学意义(P>0.05)。治疗后,观察组工作与医师关系、家庭生活、情感功能评分和总评分较治疗前和对照组明显降低(P<0.05)。见表7。
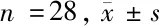

组别家庭生活工作与医师关系经济困难情感功能总分观察组 治疗前24.51±3.1826.32±2.832.88±0.9227.87±2.3681.37±9.15 治疗后21.18±2.61∗#23.28±2.47∗#3.59±0.8325.36±2.48∗#72.69±8.67∗#对照组 治疗前24.69±2.4426.29±2.682.86±0.8927.68±2.5281.19±8.87 治疗后25.91±2.7226.42±2.833.46±099528.21±1.7984.04±7.99
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
2.8 2组患者治疗前后肿瘤标志物CEA水平比较 2组治疗前CEA水平差异无统计学意义(P>0.05)。治疗后,观察组CEA水平明显较治疗前显著降低(P<0.01);对照组患者CEA水平较治疗前降低,差异有统计学意义(P<0.05)。见表8。
2.9 2组患者治疗前后生存时间比较 观察组中位生存期为10.2个月明显长于对照组的7.6个月,差异有统计学意义(P<0.05)。见图1。
3 讨论
营养不良、生存质量下降在晚期NSCLC患者中极常见[9],目前,化疗仍是NSCLC的主要治疗手段,由多药耐药的存在,单纯化疗的临床效果并不十分理想,且其毒副反应使患者营养不良、生存质量低下的状况愈发严重,使许多患者不能长期坚持治疗,故寻找低毒、高效的药物或其他治疗手段,成为了临床治疗晚期于NSCLC 患者亟待解决的问题。清肺益气汤方中黄芪为主要药物,与人参合用,可补虚健脾、益气清肺,改善免疫系统功能;薏苡仁补益肺脾之气、化湿祛痰;黄芩、百合、北梗清肺润燥、化痰止咳;升麻升举阳气、解毒宣肺;甘草补益肺气;贝母清肺化痰、散结消肿。现代药理研究证实,清肺益气汤方剂中的五味子、太子参以及黄芪具有补肺生津、保肺清心、益气养阴等功效;黄芪还具有防止肺组织细胞损伤,增强T细胞、NK细胞和IL-2抗癌活性,有效清除氧自由基,改善抗氧化状态,提高网状内皮系统吞噬功能,增强对肿瘤细胞杀伤力的功效[10]。桑白皮能够固元气、补虚。麦冬可以加速消化道排空, 刺激骨髓造血, 缓解化疗药物引起的各种不良反应[11]。此外,陈皮、瓜蒌具有化痰散结以及宽胸理气的效用;枇杷叶、杏仁能够降逆止呕、止咳化痰[12]。还有研究显示,清肺益气方能够对肿瘤细胞凋亡产生诱导作用,对肿瘤细胞周期产生一定的影响[5]。


组别CEA观察组 治疗前8.27±3.52 治疗后5.75±2.34∗#对照组 治疗前8.07±3.29 治疗后7.29±2.33∗
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05

图1 2组患者生存时间比较
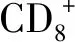
综上所述,清肺益气汤联合GP方案治疗晚期NSCLC患者的近期疗效,纳入病例数较少,为单中心研究,该治疗方法的近期疗效以及肝、肾保护是否优于单纯化疗,尚需更多临床研究予以证实。 在具体疗效上,与对照组比较,观察组趋于好转、稳定,但2组间未见明显差异,清肺益气方能否促进肺癌细胞的凋亡,抑制肿瘤细胞生长有待进一步证实,这可能与较短的治疗周期及较少的样本容量有关。此外,清肺益气方在提高临床疗效、提高免疫力、改善临床症状及降低化疗毒副反应等方面的作用是否与方剂配伍、药物剂量有关有待进一步研究。
