精准医疗狙杀癌症
2020-03-17戴维·H.弗里曼张文智
戴维·H.弗里曼 张文智

| 精准医疗,救人一命 |
对于无数患者来说,精准医疗正在改写他们的癌症故事,52岁的琳达·博伊德即是一例。
博伊德原是一位精力充沛的職业治疗师,有一次她和家人去夏威夷度假,一家人在海滩上玩得不亦乐乎,然而博伊德总是感觉身体疲惫。等她回到俄亥俄州哥伦布市的家里时,身上的皮肤已经发黄。在一位肿瘤专家那里,她被确诊为胆管癌晚期。医生告诉她,化疗或手术已经无济于事了,他所能做的只是让她生命中的最后几个月过得不那么痛苦。
对于这样的诊断结果,博伊德的丈夫无法接受,他在俄亥俄州立大学综合癌症中心找到一位负责研究胃肠道癌实验药物的医生,然后博伊德报名参加了这位医生主持的一项实验。医生对博伊德体内的肿瘤进行了基因测试,结果显示,有一种名为FGFR(细胞表面成纤维生长因子受体)的基因发生了突变,这可能刺激了肿瘤的生长。医生给她服用了一种名为BGJ398的实验药物,以抑制因FGFR突变而产生的负面作用。令人高兴的是,博伊德的症状消失了,肿瘤停止生长,体重也恢复正常。
这已经是三年前的事情了。如今,博伊德每每讲到这些仍然难掩兴奋,“我现在基本上过着正常的生活。”她说,“我刚刚参加了儿子的高中毕业典礼,我觉得自己过去一年做的事情比得病之前那么多年做的还要多。”
随着一些抗癌新药从实验室进入临床试验,与博伊德相似的故事正在美国各地上演。
或许,癌症患者一刀切地接受放疗和化疗的时代将很快成为过去式。医生正在以更加细致的态度来看待药物和疗法,考虑它们具体会在哪位病人、哪种癌症上起效,这种所谓“精准医疗”或曰“个性化医疗”的理念,归根结底就是,医生通过基因检测(既检测病人又检测癌症肿瘤)来确定到底哪种药物或疗法最能见效。

俄亥俄州立大学综合癌症中心内的詹姆斯癌症医院及索罗夫研究所
尽管当下正在进行将精准医疗技术用于多种疾病治疗的培训,不过人们感受最强烈的还是它们在癌症治疗方面的影响力。研究者正在创建一个能够清晰表现肿瘤内的基因及基因突变的清单,且不断更新,然后为病人匹配最能阻止肿瘤生长的药物。目前,被药物作为标靶发起攻击的癌症基因有数十种,研究者还在对另外数百种加紧研究。对于此前被认为实质上宣判患者死刑的一些癌症,治疗前景也已经大为改观:大约一半肺癌患者在接受了一种新型的基因匹配疗法后反应良好,在他们当中,又有一半人没有出现癌症复发的状况。FGFR抑制剂,也就是救了博伊德的那种药物,不仅在治疗胆管癌方面表现出效果,而且对于膀胱癌、肺癌、乳腺癌和子宫癌等也都有疗效。塞米克·罗伊乔德哈里是那位救了博伊德一命的肿瘤学家,他说:“我们现在仅是针对FGFR抑制剂就启动了六项试验,到今年年底会有20项。”
| 人工智能,梳理数据 |
数十年来,精准医疗在癌症研究领域断断续续取得的进步着实令人欣喜,但不要搞错:并没有实现“治愈”癌症,药物甚至连接近击败癌症的效果都没达到。那些被确诊为癌症晚期——即癌细胞已经发生扩散或转移——的患者,只有1/10的人拥有目前已知能使其所患癌症易受新药干扰的基因。“我们的目标是向所有患者提供一种基于基因测试的全新疗法,但在当下,我们还不清楚该如何向接受我们基因测试的那其余9/10的患者提供一种专门疗法。”罗伊乔德哈里说。
绝大多数患者被排斥在这1/10的机会之外。许多医生在这一领域仍然缺乏相关的专业知识,无法进行没准能叩开一项精准疗法大门的基因检测。费用也是一只拦路虎:保险公司没有为类似实验提供足够的理赔保障。美国每年有近200万人被诊断出患有癌症,然而精准医疗最多只能为数个百分点的患者提供帮助,而在全球每年1700万的新增癌症患者中,这个比例就更小了。
为了增加有资格接受基因检测治疗的病人的数量,医生们转而求助于人工智能。基因检测会产生大量数据,以至于一大群博士也不能完全搞明白,而处理这些海量数据却是人工智能的长项。科学家们正把寻找肿瘤弱点的任务委托给《深度学习》软件,这款软件可以对数百万个基因检测结果和患者治疗效果进行梳理,以发现肿瘤基因、癌症生长和特定药物之间的新关系。
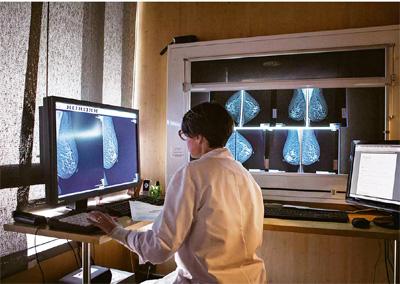
对于此前被认为实质上宣判患者死刑的一些癌症,精准疗法有着较好的治疗前景
每年有9000名癌症患者来到位于洛杉矶市外的希望之城国家医疗中心就诊。为了增加向前来求医者提供治疗方案的可能,该中心计划在两年内对每位患者都进行肿瘤基因检测,从而成为美国首家如此操作的大型医院。希望之城国家医疗中心总裁、医师迈克尔·卡利久里说:“在显微镜下看着都一样的肿瘤,从染色体的角度来看就大不相同了,我们得区别对待它们。”
其他医院纷纷跟风,海量对人工智能有用的数据即将生成。一个典型人类基因组中的两万个基因,包含有30亿个核苷酸或片段信息,它们当中的每一个都会以任何一种方式进行变异、重复或移动,以致产生癌症。人体内的数十亿个细胞,每个都有自己的那份基因组,都会发生各不相同的变异。
不过,DNA只是整幅图景的一部分:DNA是一个型板,而我们细胞内的实际工作是由蛋白质来完成的。这种管理着我们机体中几乎一切的复杂分子,既掌控着一个癌症肿瘤的生长,也掌控着免疫系统与之抗争的工作。在多达600万个碱性蛋白质及其变化形式中,研究人员正在对癌症组织样本中的数千个进行测试,然后把得到的信息提供给《深度学习》程序。
“药物的攻击目标不是基因,而是蛋白质。”得克萨斯州欧文市凯瑞斯生命科学公司的首席科学官戴维·斯皮特尔说。范德比尔特大学医学院院长杰弗里·巴尔瑟则表示,“这是我们在理解癌症方面所取得的最大进步,也将是今后五年我们采集到的最有用信息。”
《深度学习》算法不像科学家那样工作——它们从来不“理解”自己正在分析的癌症背后的生理机能,而是对来自癌症病人组织样本的大量信息进行梳理,然后将这些信息与病人的最终命运联系起来——哪种疗法对谁有效,对谁无效。它是一种不预设目标的连线练习,从人类可能永远也看不到的数据中,电脑能巧妙得出人类想要的东西。

希望之城国家医疗中心内的医生正在检测肿瘤基因。
就拿斯皮特尔的公司来说,该公司正在利用《深度学习》软件来处理蛋白质强化方面的数据。为了梳理17万癌症病人的数据,从中提炼出有用的观点,这家公司运用了数百种不同的《深度学习》算法。
| 病理切片,匹配用药 |
通过解读取自活检的组织切片,人工智能可为如何匹配患者与新药提供关键证据。那些切片通常是由病理学家用显微镜观察后作出解读的,他们根据细胞的外观作出关于癌症的诊断结论。现在,号称《机器学习》的程序开始步入市场。一家名为Nucleai的以色列公司用2000萬数字化的活检切片来“培训”其软件,使其能识别出癌症。目前它的准确率已达97%。
Nucleai的CEO艾维·魏德曼表示,诊断癌症只是个开始,他们现在的目标是,利用人工智能从切片中获取更多信息,比病理学家能够得到的还要多。这些信息可帮助患者匹配新药。魏德曼曾为以色列情报机构工作了20年,三年前他将关注点放到识别癌症上。“医生尝试预测见效的疗法时,来自组织切片的大部分信息都没有被用上。”魏德曼说,“人工智能可以更加高效地分析图片中不同类型的特点,进而发现隐含模式。”比如,他们的软件能识别出患者体内癌细胞与免疫系统细胞“交战”的细微迹象。在几种免疫疗法新药中,癌症是否容易受到某一种的伤害,那些细微迹象提供的证据很是关键。
韩国企业Lunit开发出一款人工智能软件,它能对病理切片进行分析后作出预测。例如,预测哪位患者会在服用名为“检查点抑制剂”这类相对较新的抗癌药物后有所好转,该药物能阻断癌细胞对患者免疫细胞的抑制。Lunit声称,这款软件的准确率比起单纯利用基因数据进行的检测要高出50多个百分点。该公司CEO兼医师徐炳锡说:“这款软件超越了人类肉眼的能力范围,可发现人类识别不了却又具有生物学意义的复杂模式。”
基于人工智能,可解读X光、核磁共振以及其他图像数据的系统也在取得类似进展。“已经有算法可以像训练有素的放射治疗医师那样解读乳腺X光片了,或者像皮肤病学家那样识别出皮肤癌。”休斯顿安德森癌症中心的病理学家池永玉说。那些被用来解读的图像,最终有可能帮助人工智能系统找到一些蛛丝马迹,来揭示患者独有的癌症软肋,从而超越单单诊断癌症这一功能。

韩 国 企 业 Lunit 的 一名科研人员正在将活检切片放入高分辨率扫描仪中。
| 击败癌症,任重道远 |
在当前,尽管研究者和临床医生可以进入包含了25万名癌症患者信息的数据库,但这还不够。一名患者基因组内发生的数以千计各不相同的变异,能勾勒出癌症的发展,并决定哪种疗法能见效。每个癌细胞就是一个移动标靶,它不停地生成新的变异,以帮助它避开免疫细胞和强效抗癌药的攻击。在能够识别一种独特模式之前,人工智能软件需要读取该模式的数千样本,而在数千名患者中,或许总共才发生一种模式独特的变异。如此,若想取得更快的进展,人工智能软件需要访问数百万患者的数据。在加州大学洛杉矶分校的琼森综合癌症中心主持癌症数据科学工作的医师保罗·鲍特罗斯说:“如今我们能够预测肿瘤将如何发展,以及哪种疗法会见效,不过就目前来说,有相当一部分预测是错误的。”
许多此方面的合作机构在研究中心和医院当中涌现,诸如国际癌症基因组联盟、肿瘤研究信息交换网络以及规范基因组联盟等。它们共享患者数据,这些数据能够帮助研究者最终取得所需的关键信息。“我们需要达到这样一种程度,那就是所有这些各不相同的数据网络被连成一个网中网。”希望之城国家医疗中心的卡利久里说,临床医师也需要拥有访问这些数据的权利,以便发现怎样治疗他们正在救治的患者。“在计算机上输入一名患者的癌症信息,就能查看全球范围内与其情况相似的病例。我们应该拥有这样的权利。”他说。
在抗癌药物开发领域的新药测试阶段,招募受试患者是最耽误时间的。研究者不仅需要一组尝试新药的志愿者,还需要另外一个接受常规治疗的“控制组”,以作对比。即便一种精准新药被看好,也要进行数年的临床试验,以证明其对特定群体的病人确实有效。

《深度学习》算法从来不“理解”自己正在分析的癌症背后的生理机能。
为了加快进程,研究者也在利用人工智能。凭借强大的统计数据和电脑模型,他们完全无需招募控制组,而是将此前研究产生的数据进行糅合,以预测一个真实的控制组服药后会怎样。“从虚拟控制组得到的结论,与你从实际招募的控制组病人身上得到的一样可靠。”开发此类统计软件的某公司总裁格伦·德·弗里斯说道。
对于希望用精准疗法降服那些最致命、最凶险癌症的临床医师和研究者来说,上述还不足以消除阻碍试验提速的瓶颈。举例来说,在所有主要癌症当中,胶质母细胞瘤这种最具侵袭性的脑癌,患者确诊后的中位生存期最短:15个月。其病情发展之迅速,以至于让研究者几乎没有时间来检验药物是否有效。
针对这种情况,美国菲尼克斯市巴罗神经学研究所新近创立的艾维脑瘤中心,为其脑癌患者开发出了“加速试验法”。首先将一剂量试验用精准药物分配给一名刚确诊的患者,这些药物的剂量很小,不会对患者造成伤害,却足以对肿瘤产生作用。手术后,医生检测肿瘤,看药物是否起效。如果起效,就给患者加大剂量;如果无效,就要及时进行另外的疗程,用该中心主任纳德·萨纳伊的话说就是,“找到见效的药物,速度是关键”。这种个性化疗法,已经在一位患恶性脑膜瘤(脑癌的一种)的病人身上收到了效果。
所有这些方法加在一起,可能就让我们距离用精准医疗降服大多数癌症的日子又近了一步。
[译自美国《新闻周刊》]
编辑:要媛
