干燥综合征致血小板减少合并急性心肌梗死1 例
2020-03-16余家凤曾川锐刘映峰缪绯
余家凤 曾川锐 刘映峰 缪绯
1 临床资料
患者 男,63岁。因“胸痛、胸闷10余天”于2018年8月28日入住南方医科大学珠江医院。外院平板运动试验阳性,查血小板计数(platelet,PLT)35×109/L。既往有高血压病史,无吸烟史。入院查体:体温36.7℃,脉搏73次/分,呼吸18次/分,血压125/75 mmHg(1 mmHg=0.133 kPa),心率73次/分,心律齐,主动脉瓣听诊区闻及舒张期吹风样杂音。实验室检查示:PLT 20×109/L,低密度脂蛋白胆固醇(low density lipoproteincholesterin,LDL-C)2.01 mmol/L;肌钙蛋白T(troponin T,TnT)0.044 μg/L。心电图示(图1):窦性心律,T波改变。超声心动图示:左心室下壁心肌收缩运动减弱,左心室射血分数(left ventricular ejection fraction,LVEF)50%。颈动脉彩超示双侧颈动脉内膜增粗增厚,多处附壁斑块形成。入院诊断:(1)不稳定型心绞痛;(2)高血压病2级,很高危;(3)颈动脉斑块形成。入院口服氯吡格雷75 mg、每日1次,阿司匹林100 mg、每日1次,硝苯地平控释片30 mg、每日1次,瑞舒伐他汀10 mg、每晚1次。因入院初步实验室检查发现患者PLT低,遂继续完善检查排除肝炎、病毒感染、乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)诱导等因素,查自身抗体,抗核抗体-颗粒型阳性4+,抗SSA抗体3+,抗SSB抗体3+,抗Ro-52抗体3+。骨髓穿刺2次:骨髓增生减低,巨核细胞减少,PLT少见。CT血管造影(CT angiography,CTA)示:左前降支各段多发钙化斑块,管腔轻中度狭窄。考虑目前患者心绞痛症状相对稳定,PLT低,出血风险高,予氯吡格雷单抗。请风湿免疫科会诊后加用重组血小板生成素(特比澳)注射液皮下注射15 000 U,每日1次;甲泼尼龙8 mg,每日1次;硫酸羟氯喹200 mg,每日2次升PLT治疗。治疗第10天患者诉胸痛,心电图示(图2):广泛前壁ST段抬高。心肌损伤标志物示:TnT 0.549 μg/L,肌酸激酶(creatine kinase,CK)404.8 U/L,肌酸激酶同工酶(creatine phosphokinaseisoenzyme-MB,CK-MB)62.6 U/L,N末端B型脑钠肽前体(N-terminal pro-B-type natriuretic peptide,NT-proBNP)977 ng/L,此时PLT 89×109/L。急诊行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)(图3~6):右冠状动脉近段弥漫性狭窄约80%;左前降支近段完全闭塞,左回旋支于钝缘支发出后狭窄约50%,左前降支开通后可见全程弥漫性狭窄。在血管内超声(intravenous ultrasound,IVUS)指导下于左前降支置入3枚支架(近段3.0 mm×28 mm Excel、中段2.75 mm×29 mm Firebird 2、远段2.5 mm×18 mm Firebird 2)。术后加用药物:阿司匹林100 mg、每日1次,酒石酸美托洛尔12.5 mg、每日3次,肝素375 U/h、连续泵入14 h。术后第2天患者诉胸痛,查心电图示(图7):Ⅰ、aVL、V2~V6导联ST段弓背向上抬高0.05~0.4 mV。急诊行PCI(图8~9):左前降支支架内血栓形成,行血栓抽吸术、球囊扩张术。术中应用比伐芦定抗凝[1]。术后调整用药:加用呋塞米10 mg、每日1次,螺内酯10 mg、每日1次;停用特比澳注射液,甲泼尼龙逐渐减量;替罗非班加强抗栓5 ml/h(比伐芦定后),共36 h。此时PLT 187×109/L。第2次术后第2天患者再次诉胸痛,查心电图示(图10):广泛前壁ST段抬高。床旁心肌三项:TnT 8.62 μg/L,CK-MB 59.13 U/L,NT-proBNP 5152.8 ng/L。急诊行PCI(图11~12):左前降支近段完全闭塞,行血栓抽吸术+球囊扩张术及远端药物球囊扩张术。此时PLT 286×109/L。术后再次调整用药:替罗非班3~5 ml/h,共72 h,氯吡格雷改为替格瑞洛90 mg、每日2次。第3次术后用药:替格瑞洛90 mg、每日2次,阿司匹林100 mg、每日1次,酒石酸美托洛尔12.5 mg、每日2次,培哚普利1 mg、每日1次,瑞舒伐他汀20 mg、每晚1次,甲泼尼龙4 mg、每日2次,硫酸羟氯喹200 mg、每日2次,呋塞米10 mg、每日1次,螺内酯10 mg、每日1次。3 d后甲泼尼龙逐渐减至4 mg、每日1次。出院前复查超声心动图示:左心室心尖部、侧壁心尖段室壁瘤形成;室间隔心尖段、左心室心尖部心肌收缩运动减弱,LVEF 37.1%。血常规示:PLT 18×109/L。患者PLT再次降低,与停用特比澳注射液相关。患者升血小板治疗后出现急性心肌梗死,结合患者心功能较差,低PLT下未见明显出血风险,遂未给予升血小板治疗,并于2018年9月27日出院。入院期间PLT及血红蛋白变化情况如图13。出院后患者维持术后用药,于外院监测PLT维持于20×109/L~80×109/L。
2 讨论
2.1 干燥综合征(Sjogren syndrome,SS)与急性冠状动脉综合征(acute coronary syndrome,ACS)
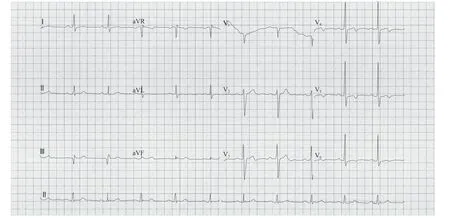
图 1 入院心电图

图 2 第1次急性心肌梗死心电图

图 3 右冠状动脉近段病变

图 4 前降支闭塞病变

图 5 前降支开通后
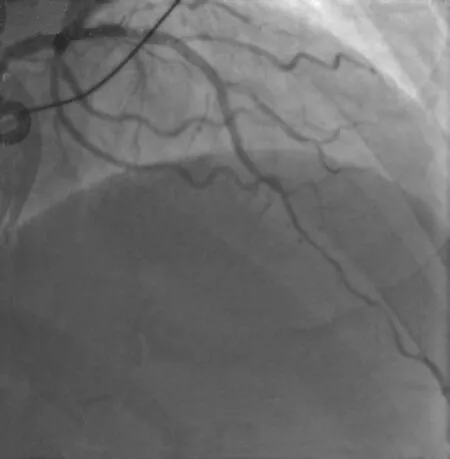
图 6 前降支支架置入术后

图 7 第2次急性心肌梗死心电图

图 8 前降支开口血栓影

图 9 前降支支架内血栓
SS是一种慢性炎症性自身免疫病,分为原发性(primary Sjogren syndrome,pSS)和继发性两类。临床上主要累及外分泌腺体。心血管并发症比较少见,主要为心包炎、左心室舒张功能不全、传导阻滞、肺动脉高压、心脏瓣膜疾病等。一项入选了788例pSS患者的队列研究发现,与对照组相比,pSS患者罹患心肌梗死及卒中的风险升高[2]。在已经发生颈动脉内膜增厚的患者中,pSS患者的心肌梗死及卒中的风险要比其他患者高出2倍[3]。本例患者入院时颈动脉彩超提示双侧颈动脉内膜增粗增厚,多处附壁斑块形成。
血小板在ACS的发病中起着重要作用[4]。凝血瀑布的激活需要生物活性微粒的参与,在合并血小板减少的脑血管病患者以及ACS患者的体内,血小板微颗粒(platelet-derived micro particles,PMPs)水平要明显高于普通人群[5]。
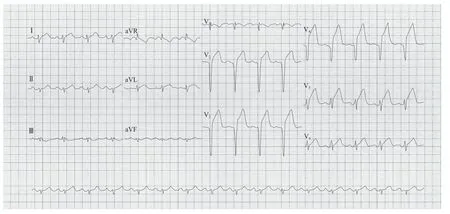
图 10 第3次急性心肌梗死心电图

图 11 血栓累及回旋支

图 12 血栓抽吸术后
2.2 本例患者PLT减少却反复急性心肌梗死的原因分析
患者住院期间,多次依据PLT、患者症状、PCI情况调整抗栓、升血小板药物,但患者仍多次出现急性心肌梗死,分析原因可能如下:(1)支架贴壁不良。因损伤的血管内皮持续暴露于血小板中,引起血小板活性瀑布样激活。但顾虑到术后抗栓治疗困难,第1次PCI中即使用IVUS指导治疗,未见支架贴壁不良表现。(2)特比澳未完全代谢。因使用特比澳维持升血小板治疗10余天,PLT由20×109/L升至384×109/L。文献提示特比澳消除比较缓慢[6],故特比澳未完全代谢使血小板呈持续上升趋势,从而导致血栓。且特比澳是刺激巨核细胞生长及分化的内源性细胞因子,有易栓性[7]。(3)新生血小板活性未被完全抑制。在形成血栓的过程中涉及胶原、腺苷二磷酸、凝血酶、血栓素A2等多种激动剂的诱导[8],而住院期间使用的阿司匹林、氯吡格雷、替罗非班、肝素等抗栓药物只抑制了血栓形成过程中的部分环节。
2.3 SS导致血小板减少且合并ACS的升血小板治疗及抗栓治疗
抗血小板治疗是ACS及PCI的基石,充分的抗血小板治疗是预防心肌梗死及支架内血栓形成等不良事件的有效措施。SS导致血小板减少且合并ACS的患者较为少见,在升血小板治疗、抗栓治疗上也无明确指南。相关文献报道:PLT<30×109/L,禁忌PCI术,需停用抗凝、抗血小板治疗[9]。这使得PLT较低的ACS患者是否接受抗血小板治疗、PCI以及PCI之后如何抗栓成为一大矛盾。通过本病例可知,PCI是ACS患者有效的治疗方法,术前、术后抗栓药物治疗也是必不可少的[10]。但是,在PLT极度减少的情况下合并ACS患者药物治疗或PCI过程中使用抗凝及抗血小板药物是否安全、剂量如何选择以及需联合几重抗栓药物才能抑制血小板活性等都有待考究[11]。抗凝治疗目前已不是急性心肌梗死的常规治疗方案,但对于合并免疫系统疾病时,抗凝是否必要仍不明确。

图 13 入院后血小板及血红蛋白变化情况
