卡马西平致中国不同地区皮肤不良反应与HLA-B*1502等位基因的相关性研究进展
2020-03-15黎红王玉芬张沁丽杨阳李小梅
黎红,王玉芬,张沁丽,杨阳,李小梅
(1.山西省长治市长治医学院研究生学院,山西 长治;2.山西省长治医学院附属和平医院 神经内科,山西 长治)
0 引言
主要组织相容性复合体(major histocompatibility complex,MHC)是一组细胞表面蛋白,其可以与外源分子结合,通过诱导免疫系统,使细胞与外源分子相对应而被识别。MHC高度保守,存在于所有脊椎动物中。在人类中,MHC也被称为人类白细胞抗原(human leukocyte antigen,HLA)复合体,是具有高度多态性的同体异体抗原,基因数量众多。其可分为三个基因亚组:I类、II类和III类。I类基因由HLA-A、HLA-B、HLA-C三个主要基因组成,仅编码I类分子异二聚体的重链,轻链为b2微球蛋白(b2-m),编码基因位于第15号染色体,被CD8+ T细胞识别。II类基因由HLA-DPA1、HLA-DPB1、HLA-DQA1、HLADQB1、HLA-DRA、HLA-DRB1 6个主要基因组成,在复合体中位于近着丝点一端,结构较为复杂,被CD4+ T细胞识别。III类基因位于I类和II类基因之间,主要编码与抗原提呈有关的分子及补体的某些成分[1]。I类基因中的人类白细胞抗原B(HLA-B)基因是一种编码参与呈递抗原至免疫系统的白细胞表面蛋白的基因,目前已鉴定出超过1500个HLA-B等位基因,其中与卡马西平引起皮肤不良反应相关的HLA-B*1502基因就是HLA-B位点的1个基因亚型[2-3]。
1 卡马西平导致的不良反应
卡马西平(carbamazepine,CMZ)是一种电压依赖性钠通道阻滞剂,能够使动作电位兴奋期延长,因此能够抑制丘脑腹前核至额叶的神经冲动的传导。临床上常用于治疗癫痫、三叉神经痛和周围神经痛、躁狂抑郁症等疾病,其常见不良反应主要有头晕、乏力、恶心、呕吐等,偶见皮肤过敏反应、肝损害、血小板减少以及粒细胞减少等,其中卡马西平引起的皮肤过敏反应多表现为重症药疹即皮肤药物不良反应(cutaneous adverse drug reactions,cADRs)。它是一种涉及皮肤、黏膜的全身综合征,通常急性起病,临床表现为全身皮肤黏膜的病损症状。根据临床形态学可将其分为大疱型和非大疱型两类,大疱型cADRs 包括 Stevens-Johnson 综合征( Stevens-Johnson syndrome,SJS) 、中毒性表皮坏死松解症(toxic epidermal necrolysis,TEN) ,而非大疱型 cADRs 包括轻度的斑丘疹( maculopapular eruption,MPE) 和药物超敏反应综合征( drug-induced hypersensitivity syndrome,DIHS)[4];按照表皮剥脱程度分类: 表皮剥脱小于总皮肤表面积 10% 为 SJS; 面积大于 30% 为 TEN[5]。虽然卡马西平致严重皮肤反应发生率较低(约为 1:10000),但其致死率达 30%以上,而 SJS/TEN 的致死率高达40%[6],应引起临床医生高度重视。
2 不同地域间HLA-B*1502等位基因与卡马西平致皮肤不良反应关联性的研究
2004年,Chung等首次报道了卡马西平所致的SJS/TEN与人类HLA-B*1502基因有关,而后中国科研人员相继在自己所在地区对 HLA-B*1502等位基因与卡马西平所致皮肤不良反应间的相关性进行了研究。
2.1 中国大陆
2.1.1 广东地区
2017年,侯蕴祈等[7]报道,通过收集佛山地区 75 例卡马西平致敏性的患者进行回顾性研究,同时纳入健康对照组60例。检测以上患者和未服用过癫痫药物芳香族的30例正常对照者的 HLA-B* 1502 基因分型。结果卡马西平致敏性组中 HLA-B*1502 阳性者72例(占96.00%),阴性者3例(占4.00%),健康组阳性者1例(占1.67%),卡马西平致敏性组中 HLA-B* 1502表达阳性率显著高于健康对照组,差异有统计学意义(P< 0.05) 。结论HLA-B* 1502 的表达与CBZ致敏性具有一定的相关性。
2019年,孔韦东等[8]报道,通过收集当地581例服用卡马西平的癫痫患者,检测以上患者的HLA-B*1502等位基因,结果发现,出现皮肤不良反应的患者共95人,其中有 46 例(48.4%)为HLA-B*1502 阳性,49 例(51.6%)为阴性,未发生皮肤不良反应的患者共486,其中19例(3.9%)为阳性,而467例(96.1%)为阴性,正常组与发生皮肤不良反应组之间 HLA-B*1502 基因阳性率差异有统计学意义(P<0.01),说明皮肤不良反应与该基因具有明显的相关性。
通过以上研究报道,表明广东地区人群HLA-B* 1502 的表达与CBZ致敏性具有一定的相关性。
2.1.2 四川地区
2018年,方登富等[9]报道,通过对2015年6月至2017年2月期间于遂宁市中心医院接受卡马西平治疗的40例癫痫患者(实验组)以及25例健康自愿者(对照组)进行基因检测,发现CBZ致SJS者HLA-B*1502基因型阳性4例,基因频率80.00%;CBZ致SJS/TEN者HLA-B* 1502基因型阳3例,基因频率 75.00%;CBZ 致 TEN 者 HLA-B* 1502 基因型阳性 3 例,基因频率 100.00%; 耐受组HLA-B* 1502 基因型阳性 2 例,基因频率8.33%;对照组HLA-B* 1502基因型阳性 3 例,基因频率12.00%。卡马西平引起的各型重症皮肤过敏反应者 HLA-B* 1502 基因频率均显著高于耐受组与对照组,有统计学意义(P<0.05) 。由此可见卡马西平引起各种重型皮肤不良反应者HLA-B*1502基因频率均保持较高水平。
2.1.3 江西地区
2014年,王蕊艳等[10]报道,通过收集服用卡马西平出现皮肤不良反应的患者和健康人46例,其中Stevens-Johnson综合征(SJS)组13例,轻微皮肤反应(MPE)组19例,对照组(包括耐受者和正常志愿者)14例。检测以上患者的HLA-B*1502等位基因,结果SJS组13例(100%)HLA-B*1502基因均为阳性,MPE组有2例(10.5%)HLA-B*1502基因属于阳性,而对照组只有1例(7.1%)HLA-B*1502基因属于阳性。SJS组分别与MPE组和对照组比较差异具有统计学意义(P<0.05),MPE组与对照组比较差异无统计学意义(P<0.05)。结论江西汉族人群中卡马西平导致的SJS与HLA-B*1502基因具有强相关性,而MPE与之无相关性。
同年,刘藕根等[11]通过研究在具有江西汉族遗传背景人群中,收集CBZ所致SJS/TEN患者19例,以及90例服用CBZ无过敏患者和80例健康对照者,采用序列特异性引物聚合酶链反应法进行HLA-B*1502的基因型测定.观察CBZ所致的SJS/TEN与HLA-B*1502基因型是否存在关联。结果 CBZ所致SJSfrEN组HLA-B*1502基因型携带率为100%,显著高于CBZ耐受组(15.5%)及健康对照组(18.75%),差异均具有统计学意义(P<0.001)。CBZ耐受组 HLA-B*1502基因型携带率与健康对照组比较,差异无统计学意义(P=0.684)。结论:具有江西汉族遗传背景人群中,卡马西平导致的SJS 与 HLA-B*1502 基因具有极强的相关性。
2.1.4 江苏地区
2016年,石建等[12]对苏州市49例服用CBZ致皮肤不良反应的患者进行基因分型,有16例收集到血样,并测定HLA-B*1502等位基因。经检测,只有1例为阴性,阳性率达到93.75%,与Zhang等研究报道的结论一致。
2.1.5 上海地区
2018年,孟琳懿[13]等通过对上海地区140例癫痫患儿HLA-B*1502等位基因分布情况进行研究,发现HLA-B*1502基因阳性者51例(占36.43%),阴性89例(占63.57%),阴性结果明显多于阳性结果,所有阳性患者避免使用卡马西平后,未见发生SJS/TEN者,HLA-B*1502与CBZ诱导的SJS/TEN有很强的相关性。
2.1.6 闽南地区
2016年,李珣等[14]通过选取268例需要服用CBZ的患者和100名健康人,对所有样本进行程序,发现样本中,共有26例HLA-B*1502阳性 ,其中临床诊断为癫痫 、躁郁症及三叉神经痛的样本中HLA-B *1502基因的阳性率分别为8.53% 、9.09%和 8.33%。在100例健康人样本中有3例为HLA-B *1502阳性。通过计算得出:在闽南 地 区,需 服用 卡马 西平 的患 者 中HLA-B*1502的阳性为 8.58%,基因频率为 0.043,而这两项 数据在 健康人中分别为 3.00%与 0.015;在闽南地区总人群 中为7.07%与 0.035。闽南地区人群中HLA-B*1502的基因频率较高。
2.1.7 东北地区
2014年,JXHE等[15]通过对35例CBZ-SJS/TEN患者和125例CBZ耐受患者进行基因检测,结果发现35例CBZ-SJS/TEN患者中有8例(22.9%)属于HLA-B*1502等位基因阳性,125例CBZ耐受患者中的仅有2例携带HLA-B*1502等位基因(OR=18.222,95CI=3.662-90.662,P=0.000)。我们的结果表明,在中国东北地区汉族人群中,监测HLA-B*1502是必要的,但不足以产生CBZ/SJS/TEN。结论 该研究结果与这些研究报道来自中国南部、西南部和中部的个体的HLA-B*1502和CBZ-S/TEN之间有很强的相关性的研究结果不一致。
2.2 香港地区
2014年,Wang等[16]通过对16例 CBZ-SJS/TEN和64例卡马西平耐受者,进行基因检测。结果显示,SJS/TEN组的15名受试者携带HLA-B*1502,其中12例表现为LTG-SJS,1例表现为PB-SJS,而AED耐受组只有4/64例,HLA-B*1502等位基因的带率在各组间差异显着差异(P<0.001)。HLA-B*1502和CBZ-S/TEN之间有相关性,与Man等[17]研究结论一致。
2.3 台湾地区
2011年,CHEN等[18]在中国台湾汉族人群中进行了一项前瞻性基因分型研究,共计筛选2 3个医院4877例使用CBZ的患者,从受试者外周血中纯化的DNA进行了基因型分析,以确定他们是否携带了HLA-B*1502等位基因。发现HLA-B*1502阳性者(占总数的7.70%),并建议他们不要服用卡马西平,并给予替代药物或建议继续服用他们的预研药物;试验阴性者(92.30%)给予服用卡马西平。结果 4.3%的受试者发生了轻度的暂时性皮疹,0.1%的受试者出现了更广泛的皮疹。在接受卡马西平治疗的HLA-B*1502阴性者中,SJS-TEN未出现任何进展。相反,在研究对象中,卡马西平诱发的SJS-TEN的历史发生率估计值(0.23%)将转化为10例左右(P<0.001)。结论 在这些受试者中,识别携带HLA-B*1502等位基因和避免卡马西平治疗的受试者与减少卡马西平引起的SJS-TEN的发生率密切相关。
2014年,Chonlaphat Sukasem等[19],通过检测60 例 CBZSJS/TEN 患者的 HLA-B* 1502 基因,结果 59 例(98.33%)患者的HLA-B* 1502 基因均为 阳性,结论 HLA-B*1502等位基因与CBZ诱导的SJS/TEN有很强的相关性。
根据以上研究报道,中国不同地区人群中HLA-B*1502基因和卡马西平致皮肤不良反应之间的相关性存在差异。其中东北地区研究报道与来自中国南部、西南部和中部的研究结果差异较大。
3 中国不同地区人群中HLA-B*1502基因频率
由于目前关于HLA-B*1502基因频率的研究多为区域性调查,因此在表1中分别总结了中国部分地区人群中HLA-B*1502基因频率的研究结果总结于表1。
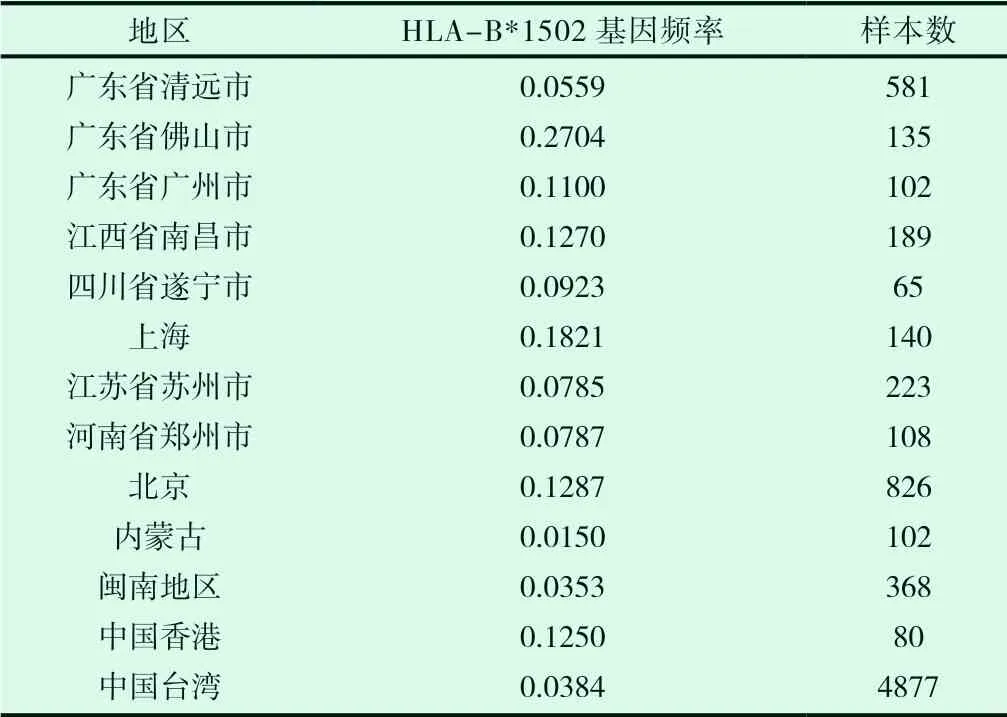
表1 中国部分地区人群HLA-B*1502的基因频率
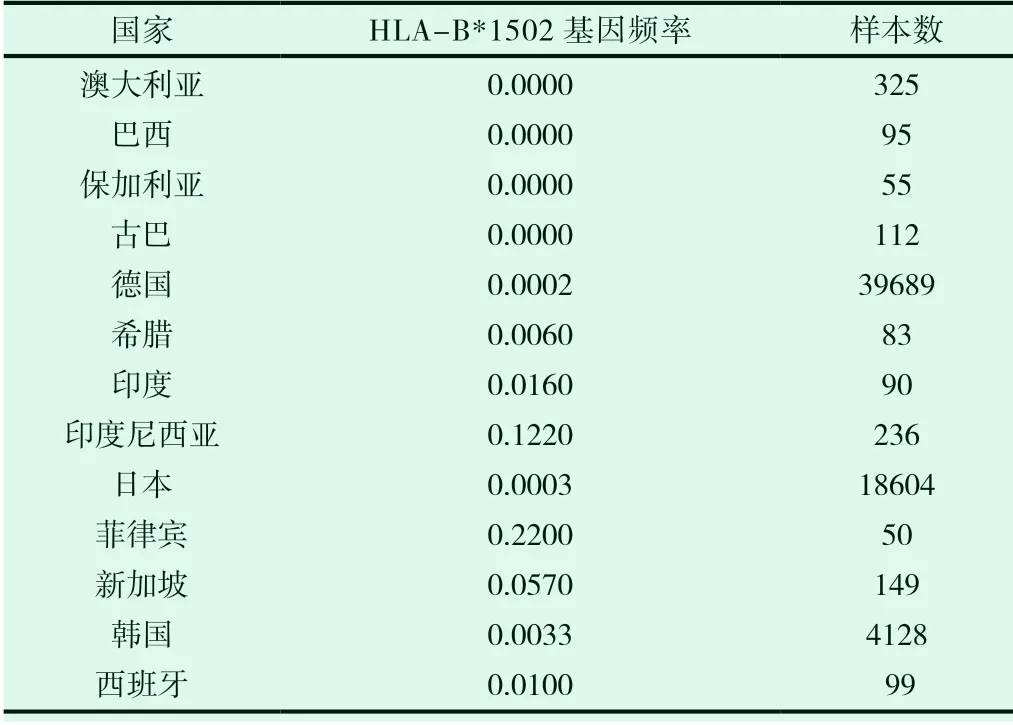
表2 部分国家人群HLA-B*1502的基因频率[14]
经过比较表1和表2可以发现,在不同的国家和不同地区之间HLA-B *1502基因频率是不同的。从世界范围来看,印度尼西亚、菲律宾和中国等亚洲地区HLA-B*1502基因频率较高。从中国范围来看,广东、上海、北京,香港等发达地区HLA-B*1502基因频率较高。
4 HLA-B*1502等位基因与严重皮肤不良反应的药理机制
卡马西平所致的严重皮肤反应(SJS/TEN)主要的临床表现为大面积的角质细胞凋亡及表皮下起疱,有研究表明,导致皮肤不良反应的主要毒素分子与粒溶素关系密切[20-21]。由于SJS/TEN在2~3d内即出现严重症状,是细胞毒性T细胞引发SJS/TEN患者皮肤损害, 而且患者疱液中的T细胞以CD8+ 亚型为主, 说明SJS/TEN的发生主要是CD8+T细胞介导的细胞毒性反应。而药物分子如卡马西平及其代谢物为小的化学分子, 自身不足以引起免疫反应, 因此提出了半抗原的假说, 即某种特定的药物或者其代谢产物作为半抗原与蛋白或多肽共价结合后, 经过细胞处理再呈递给MHC分子, 从而出现HLA特异性的T细胞激活。另一种假说是p- i设想( 药物与免疫受体之间的直接药理作用) , 即药物可以直接与MHC分子匹配的T细胞受体非共价结合。两种假设均提示通过特异性MHC分子、T细胞受体及药物修饰抗原之间的相互作用, 引起皮肤不良反应[22]。
5 利用HLA-B*1502基因合理使用卡马西平
从以上研究可以发现,CBZ-SJS/TEN与 HLA-B*1502之间的相关性存在种族和地区差异,在不同的国家和不同地区之间HLA-B *1502基因频率也是不同的,其中中国汉族人在世界范围内属于基因频率较高人群。如今HLA-B*1502基因虽然被认为是中国汉族人群中CBZ-SJS/ TEN的基因标志物,但由于服用卡马西平发生严重皮肤不良反应的患者较少,且HLA-B*1502基因阳性的患者不一定发生皮肤不良反应,大部分地区尚未对需要服用卡马西平的患者开展HLA-B*1502等位基因的检测。但是通过以上研究可以发现,HLA-B*1502阳性的患者服用卡马西平发生严重皮肤不良反应的发生率较高,且致死率也较高,应该引起临床医生的重视,建议患者在服用卡马西平治疗之前,进行HLAB*1502等位基因的检测,从而预防严重皮肤不良反应的发生,提高临床合理用药。
